Артериальная гипертензия (АГ) является одной из наиболее актуальных проблем здравоохранения как в России, так и во всем мире. Это обусловлено большой распространенностью и высоким риском ее осложнений – ишемической болезни сердца (ИБС), мозговых инсультов, сердечной и почечной недостаточности. Распространенность АГ в экономически развитых странах достигает 25 % [1].
В России у 40 % мужчин и женщин старше 18 лет отмечаются повышенные показатели артериального давления (АД) [2]. Согласно Российским рекомендациям по диагностике и лечению АГ, стратегической целью терапии этого заболевания является максимально возможное снижение риска сердечно-сосудистых осложнений (ССО). Важнейшим условием эффективной антигипертензивной терапии является адекватный контроль АД, т. е. достижение его целевого уровня, за который принимают АД
Вместе с тем в России только у 5,7 % мужчин и 17,5 % женщин с АГ достигаются целевые уровни АД. Если не повысить эффективность терапии, т. е. не увеличить долю адекватно леченых пациентов с АГ, рассчитывать на перелом в снижении ССО не приходится.
В настоящее время возможно использование двух стратегий терапии АГ для достижения целевого АД: монотерапии и комбинированного лечения (см. рисунок). Монотерапия базируется на поиске оптимального для конкретного больного препарата, и переход на комбинированную терапию целесообразен только в случае отсутствия эффекта последнего. Комбинированная терапия уже на старте лечения предусматривает подбор эффективной комбинации препаратов с различными механизмами действия.
Каждый из этих подходов имеет свои достоинства и недостатки. Преимущество монотерапии состоит в том, что в случае удачного подбора лекарственного средства больному не будет необходимо дополнительно принимать еще один препарат. Однако, как правило, при монотерапии удается достигнуть целевого АД в среднем только у 30–40 % больных АГ. Это вполне естественно, поскольку один класс препаратов не в состоянии контролировать все патогенетические механизмы повышения АД: активность симпатической нервной системы и ренин-ангиотензин-альдостероновой системы, объемзависимые механизмы. Кроме того, монотерапия требует от врача кропотливого поиска наиболее оптимального для пациента антигипертензивного средства с частой сменой препаратов и их дозировок, что нередко лишает врача и больного уверенности в успехе и в конечном итоге снижает приверженность лечению. Это особенно актуально для больных с мягкой и умеренной АГ, большинство из которых не испытывает дискомфорта от повышения АД и не мотивировано к лечению.
Недостатком комбинированной терапии является неудобство, связанное с тем, что больному приходится дополнительно принимать еще один, а иногда и несколько препаратов. Однако в большинстве случаев назначение антигипертензивных средств с различными механизмами действия позволяет, с одной стороны, добиваться целевого АД, а с другой – минимизировать количество побочных эффектов. Комбинированная терапия дает также возможность подавлять контррегуляторные механизмы повышения АД. Таким образом, переход к комбинированной терапии, позволяющей эффективно контролировать различные механизмы повышения АД, дает возможность надеяться на повышение эффективности антигипертензивной терапии.
Существуют различные комбинации антигипертензивных средств. Cреди комбинаций двух препаратов эффективными и безопасными считаются: диуретик + бета-адреноблокатор; диуретик + ингибитор АПФ (иАПФ); диуретик + антагонист рецепторов к ангиотензину II (АРА); антагонист кальция дигидропиридинового ряда + бета-адреноблокатор; антагонист кальция + иАПФ; антагонист кальция + диуретик; альфа-адреноблокатор + бета-адреноблокатор; препарат центрального действия + диуретик. Кроме того, возможны комбинации иАПФ, антагониста кальция, АРА и диуретика с агонистом I1 имидазолиновых рецепторов. Наиболее популярной в России является комбинация иАПФ и диуретика. Как показывают результаты исследования Пифагор, почти треть врачей в России отдает предпочтение сочетанию именно этих препаратов [4].
Важнейшим шагом на пути совершенствования стратегии комбинированной терапии стало создание фиксированных комбинаций антигипертензивных препаратов (два компонента в одной таблетке), значительно улучшающие приверженность пациентов терапии. Однако наряду с преимуществами (возможность приема одной таблетки, содержащей два лекарства) такой подход имеет и серьезные недостатки. Так, врач не может варьировать дозы каждого из входящих в комбинацию препаратов, что затрудняет лечение, особенно при появлении побочных реакций, четко связанных с одним из входящих в комбинацию компонентов. Во избежание подобных трудностей приходилось создавать несколько разных дозировочных форм, что может частично облегчить проблему (например, препараты Энап-H и Энап-HL, содержащие разные дозы диуретика), но не решает ее полностью.
В связи с этим интерес представляет создание нефиксированных комбинаций, содержащих два препарата в одном блистере, что позволит при необходимости варьировать дозы каждого из них. Первым в России препаратом подобного типа стал Энзикс – комбинация эналаприла с индапамидом.
Созданию этой формы препарата во многом способствовали результаты многоцентрового исследования ЭПИГРАФ, в котором принимали участие врачи 38 поликлиник из 17 городов России [5]. Всего в исследование было включено 550 больных с АГ II–III степеней (исходное систолическое АД > 160 мм рт. ст.), причем среди них были пациенты не только с эссенциальной, но и с симптоматической АГ. Особенностью данного исследования явилось то, что уже в начале лечения больным назначалась комбинация эналаприла и индапамида. Причем если доза индапамида была постоянной – 2,5 мг, то доза эналаприла варьировалась в зависимости от исходного уровня АД. Вместе с тем врачи имели возможность коррекции доз в зависимости от достижения целевого уровня АД в течение 14 недель. Средняя доза эналаприла в исследовании составила 15,2 мг. В результате лечения больных АГ дифференцированными дозами эналаприла и индапамида удалось добиться существенного снижения как систолического, так и диастолического АД. При этом у 70 % пациентов удалось достичь целевого уровня АД, несмотря на его весьма высокий исходный уровень. Побочные реакции были отмечены лишь у 8,1 % больных, причем у 5,4 % они были обусловлены чрезмерным снижением АД, что может быть устранено при более аккуратном подборе дозировок препаратов.
Главный вывод исследования состоит в том, что эффективность и безопасность комбинации эналаприла с индапамидом в лечении АГ не зависят от пола, возраста и причины, вызвавшей повышение АД (первичная АГ или вторичная АГ почечного генеза). Особенно следует обратить внимание на последнее обстоятельство в связи с укоренившимся мнением, что эффективность антигипертензивной терапии является более низкой у больных симптоматической АГ. Особенно предпочтительным сочетание эналаприла с индапамидом было у женщин, у которых монотерапия иАПФ может быть менее эффективной.
Результаты исследования ЭПИГРАФ позволили отработать наиболее эффективные дозы эналаприла и индапамида для больных АГ различной степени, что стало основой для создания трех видов препарата Энзикс: ЭНЗИКС – 10 мг эналаприла и 2,5 мг индапамида (однократный прием утром) для больных АГ I степени; ЭНЗИКС ДУО – 10 мг эналаприла и 2,5 мг индапамида (утром) + 10 мг эналаприла (вечером) для больных АГ II степени; ЭНЗИКС ДУО ФОРТЕ – 20 мг эналаприла и 2,5 мг индапамида (утром) + 20 мг эналаприла (вечером).
Эффективность и безопасность Энзикса оценивалась в исследовании ЭПИГРАФ-2, которое по дизайну являлось сравнительным рандомизированным многоцентровым, включавшим девять центров в России и один – в Сербии [6]. Всего в исследование было включено 313 больных, рандомизированных в две группы. В группу Энзикса вошли 211 пациентов, в группу контроля – 102 больных. В контрольной группе проводилось лечение другими классами антигипертензивных препаратов (кроме иАПФ и диуретиков). Через 2, 4 и 6 недель лечения в тех случаях, если не удавалось достичь целевого АД (
Все пациенты, рандомизированные в группу Энзикса, были разделены на две подгруппы в зависимости от исходного уровня АД.
В первой подгруппе 118 пациентам с АГ I степени и исходным систолическим АД 140–160 мм рт. ст. была назначена комбинация 10 мг эналаприла и 2,5 мг индапамида (соответствует форме ЭНЗИКС). В процессе лечения 88 (74,6 %) из них продолжали принимать первоначальную дозу, а у 26 (22,1 %) пациентов доза эналаприла была удвоена (10 мг утром + 10 мг вечером) при сохранявшейся дозе индапамида (2,5 мг утром), что соответствовало форме ЭНЗИКС ДУО. Только одному больному с АГ I степени потребовалось назначение комбинации 40 мг эналаприла (20 мг утром + 20 мг вечером) и 2,5 мг индапамида, что соответствовало форме ЭНЗИКС ДУО ФОРТЕ. Трое пациентов не завершили исследование.
Во второй подгруппе 93 пациентам с АГ II степени и систолическим АД 160–180 мм рт. ст. терапия начиналась с 20 мг эналаприла (по 10 мг утром и вечером) и 2,5 мг индапамида (соответствует форме ЭНЗИКС ДУО). В процессе лечения у 46 пациентов эта дозировка была сохранена, а у 45 больных доза эналаприла была увеличена до 40 мг/сут (20 мг утром + 20 мг вечером) при неизменной дозе индапамида 2,5 мг, что соответствовало форме ЭНЗИКС ДУО ФОРТЕ. Еще двум больным исходная доза эналаприла была уменьшена до 10 мг при сохранении исходной дозы 2,5 мг индапамида, что соответствовало форме ЭНЗИКС.
При анализе числа больных, у которых в результате лечения произошла нормализация уровня АД, некоторые преимущества имела группа пациентов, получавших Энзикс (72,5 %), в сравнении с группой контроля (66,7 %). И это, несмотря на то что систолическое АД в “опытной” группе было исходно на 2,7 мм рт. ст. выше, чем в контрольной. Если же суммировать общее число больных, положительно отреагировавших на лечение (число пациентов с нормализацией АД или снижением систолического АД более чем на 20 мм рт. ст. от исходного уровня), то к концу лечения оно достигло 82,4 % в среднем по группе, принимавшей Энзикс, причем среди пациентов с АГ I степени эта величина составляла 89,8 %, а у больных с АГ II степени – 77,2 %.
Таким образом, раннее начало лечения больных с АГ I–II степеней нефиксированной комбинацией эналаприла и индапамида (Энзикс) в сравнении с рутинной антигипертензивной терапией позволяет чаще достигать нормализации уровня АД. Кроме того, в группе Энзикса удалось достоверно уменьшить число пациентов с гипертрофией левого желудочка и протеинурией, улучшить качество жизни, снизить количество госпитализаций и дополнительных визитов к врачу. Помимо всего прочего терапия Энзиксом экономически выгодна.
Очень важное значение в настоящее время придается метаболическим эффектам антигипертензивной терапии. Суть метаболической теории заключается в том, что ряду антигипертензивных препаратов, например диуретикам и бета-адреноблокаторам (особенно неселективным), свойственно ухудшение липидного профиля и усугубление инсулинорезистентности, что может в долгосрочной перспективе повышать риск развития сахарного диабета и снижать эффективность терапии в плане предупреждения развития ССО [7].
Недавно завершенные крупномасштабные исследования подтвердили правомочность метаболической теории. В группах пациентов, принимавших диуретики и бета-адреноблокаторы, частота развития СД была достоверно выше, чем при лечении антагонистами кальция, иАПФ и АРА [8–10]. В связи с этим эффективность антигипертензивной терапии необходимо оценивать не только с точки зрения достижения целевого АД, но и с позиций вероятности метаболических эффектов. Это в полной мере касается и комбинированной терапии. Уместно подчеркнуть, что компоненты препарата Энзикс в этом отношении не вызывают опасений. Эналаприл, как показывают исследования, является метаболически нейтральным, а индапамид занимает особое место среди диуретиков. В рекомендуемых дозах (1,5–2,5 мг в сутки) он не только обеспечивает адекватный антигипертензивный эффект, но также и является метаболически нейтральным. Доказано, что индапамид не вызывает гипокалиемии, изменений в углеводном [11] и липидном профилях [12]. Особенно убедительное свидетельство метаболической индифферентности индапамида получено в результате проведения мета-анализа трех исследований, включивших в общей сложности 1195 пациентов. По итогам лечения ретардной формой индапамида в течение 9–12 месяцев влияния на углеводный и липидный профили, а также уровень мочевой кислоты выявлено не было [13].
Индапамид помимо мочегонного эффекта оказывает вазодилатирующее действие за счет снижения содержания натрия в стенке артерий, регулирования поступления кальция в гладкомышечные клетки сосудов, а также увеличения синтеза простагландина Е2 в почках и простациклина в эндотелии [14]. Таким образом, индапамид, оказывая более выраженное по сравнению с другими диуретиками прямое действие на сосуды, влияет на эндотелиальную функцию. Он оказывает антиоксидантное действие, повышая биодоступность NO и уменьшая его разрушение [15]. В исследовании LIVE доказана способность терапии индапамидом вызывать регресс гипертрофии миокарда левого желудочка [16].
Современная рациональная комбинированная терапия в лечении пациентов с артериальной гипертензией
По данным эпидемиологических исследований, распространенность артериальной гипертензии (АГ) среди взрослого населения в развитых странах мира колеблется от 20 до 40% и увеличивается с возрастом [1]. Повышенное АД обнаруживается более чем у 50% мужчин и женщин старше 60 лет [2]. Актуальность проблемы поддерживается возрастающими процессами урбанизации общества, создающими предпосылки для возникновения факторов риска (ФР), таких как стресс, гиподинамия, ожирение, вредные привычки и нарушенная экология. Повышенное АД является одним из главных ФР развития мозгового инсульта, ишемической болезни сердца (ИБС) и других сердечно-сосудистых заболеваний атеросклеротического происхождения, с которыми связано более 50% всех случаев смерти [3].
Клиническая практика и результаты многих мультицентровых исследований показали [4–6], что применение монотерапии в лечении АГ редко приводит к целевым уровням АД, увеличивает риск развития нежелательных явлений и снижает приверженность пациента к лечению. Применение препаратов в рациональном комбинированном режиме требует соответствия целому ряду обязательных условий: безопасность и эффективность компонентов; вклад каждого из компонентов в ожидаемый результат; разный, но взаимодополняющий механизм действия компонентов; лучший результат по сравнению с каждым из компонентов; сбалансированность компонентов по биодоступности и продолжительности действия; усиление органопротективных свойств; воздействие на универсальные (наиболее частые) механизмы повышения АД; уменьшение количества нежелательных явлений и улучшение переносимости [7–9].
Согласно современным национальным рекомендациям [10], рекомендациям Европейского общества по артериальной гипертонии (ЕОГ) и Европейского общества кардиологов (ЕОК) [11], тактика лечения эссенциальной АГ зависит от уровня АД и степени риска кардиоваскулярных осложнений. Основной целью лечения является максимальное снижение риска развития сердечно-сосудистых осложнений (ССО) и смерти от них. Основными задачами являются нормализация уровня АД, с целью предупреждения осложнений, при отсутствии или минимальном уровне нежелательных лекарственных реакций (НЛР), коррекция всех модифицируемых ФР (курение, дислипидемия, гипергликемия, ожирение), предупреждение, замедление темпа прогрессирования и/или уменьшение поражения органов-мишеней, а также лечение ассоциированных и сопутствующих заболеваний – ИБС, сахарный диабет (СД) и т. д. [10, 11].
При лечении больных АГ величина АД должна быть менее 140/90 мм рт. ст., что является его целевым уровнем. При хорошей переносимости назначенной терапии целесообразно снижение АД до более низких значений. У пациентов с высоким и очень высоким риском ССО необходимо снизить АД до 140/90 мм рт. ст. и менее в течение 4 нед. В дальнейшем, при условии хорошей переносимости, рекомендуется снижение АД до 130/80 мм рт. ст. и менее. У больных ИБС уровень АД необходимо снижать до целевого значения 130/85 мм рт. ст. У больных СД и/или с заболеванием почек целевой уровень АД должен составлять менее 130/85 мм рт. ст. [10].
Разумеется, лечение АГ следует начинать с изменения образа жизни: снижение избыточной массы тела, ограничение потребления поваренной соли и спиртных напитков, увеличение физической активности и др. Ограничение потребления поваренной соли является достаточно эффективным способом снизить АД. Было отмечено, что ограничение потребления поваренной соли усиливает антигипертензивное действие многих антигипертензивных препаратов, в т. ч. блокаторов АТ1–ангиотензиновых рецепторов и β-адреноблокаторов.
Одним из важнейших условий обеспечения адекватного контроля АД и повышения приверженности пациентов к лечению является оптимальный выбор антигипертензивного средства в составе моно- или комбинированной фармакотерапии.
В настоящее время для лечения АГ рекомендованы пять основных классов антигипертензивных препаратов [10]:
1. ингибиторы ангиотензинпревращающего фермента (иАПФ) (каптоприл, эналаприл, периндоприл, лизиноприл, фозиноприл, квинаприл, трандолаприл и др.);
2. блокаторы рецепторов AT1 (БРА) (валсартан, лозартан, телмисартан, кандесартан, ирбесартан и др.);
3. блокаторы медленных кальциевых каналов (БМКК) (нифедипин, амлодипин и др.);
4. бета-адреноблокаторы (БАБ) (карведилол, бисопролол, небиволол, метопролола тартрат, метопролола сукцинат, атенолол и др.);
5. тиазидные и тиазидоподобные диуретики (гидрохлоротиазид (ГХТЗ), индапамид).
В качестве дополнительных классов антигипертензивных препаратов для комбинированной терапии могут использоваться α-адреноблокаторы (празозин, доксазозин), агонисты имидазолиновых рецепторов (моксонидин), прямой ингибитор ренина (алискирен).
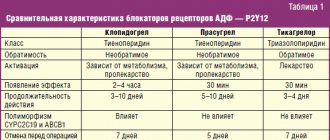
Согласно настоящим национальным рекомендациям [10], выбор антигипертензивного препарата должен быть связан с особенностями его действия, принадлежностью к определенному классу, т. к. в настоящее время результаты клинических исследований, проведенных по правилам доказательной медицины, позволили установить ситуации преимущественного классового выбора препаратов. При выборе антигипертензивного препарата необходимо в первую очередь оценить эффективность, вероятность развития побочных эффектов и преимущества ЛС в определенной клинической ситуации (табл. 1).
На выбор препарата оказывают влияние многие факторы, наиболее важными из которых являются:
- наличие у больного ФР;
- поражение органов-мишеней;
- сопутствующие клинические состояния, поражения почек, МС, СД;
- сопутствующие заболевания, при которых необходимы назначение или ограничение применения антигипертензивных препаратов различных классов;
- предыдущие индивидуальные реакции больного на препараты различных классов;
- вероятность взаимодействия с лекарствами, которые пациенту назначены по другим поводам;
- социально-экономические факторы, включая стоимость лечения.
Начинать лечение необходимо с применения одного ЛС в минимальной суточной дозе (эта рекомендация не касается больных с тяжелой АГ или лиц, у которых предшествующая терапия была неэффективной). Применение новых препаратов следует начинать с использования низких доз, целью каждого очередного этапа лечения должно быть снижение уровня АД на 10–15% [10]. Если АД не снижается до желаемого уровня, дальнейшее лечение осуществляется путем постепенного – шаг за шагом – увеличения доз или присоединения новых ЛС. Неэффективные ЛС (не вызывающие снижения АД на 10–15 мм рт. ст.) и препараты, вызывающие НЛР, следует заменить [12].
Единых рекомендаций относительно того, с каких именно средств следует начинать лечение больного, не существует. Выбор ЛС зависит от возраста, пола и наличия сопутствующих заболеваний.
В настоящее время в лечении большинства пациентов с АГ применяются препараты, изменяющие активность РААС. Это иАПФ, БАБ и блокаторы рецепторов ангиотензина II (БРА). БРА – один из современных и наиболее динамично развивающихся классов антигипертензивных препаратов. БРА подавляют реализацию эффекта ангиотензина II через АТ1-рецепторы. Установлено, что гиперсекреция ангиотензина II ведет не только к развитию АГ, но и повреждению органов-мишеней, являясь одним из основных факторов прогрессирования АГ и ее осложнений, ремоделирования сердца и сосудов. Блокаторы АТ1-ангиотензиновых рецепторов совсем не случайно отнесены к категории основных антигипертензивных средств. Многочисленные контролируемые исследования, такие как LIFE, VALUE, MARVAL, PRIME, IDNT, DETAIL [13] показали, что АТ1-блокаторы являются эффективными и безопасными антигипертензивными препаратами. Особенно эффективными блокаторы АТ1-ангиотензиновых рецепторов оказались в плане предупреждения развития мозгового инсульта. Для профилактики инсульта у больных АГ АТ1-блокаторы могут использоваться как вместо диуретиков или антагонистов кальция, так и вместе с ними. БРА, как и иАПФ, способны также предотвращать развитие СД 2-го типа, снижая риск его возникновения на 20–25% [14]. Поэтому можно предполагать, что блокаторы АТ1-ангиотензиновых рецепторов следует использовать для лечения АГ в первую очередь у больных с высоким риском развития инсульта или СД. Превосходная переносимость – несомненное достоинство АТ1-блокаторов при длительной антигипертензивной терапии. Применение блокаторов АТ1-ангиотензиновых рецепторов позволяет улучшить приверженность больных к длительной терапии, поскольку БРА значительно реже, чем другие антигипертензивные препараты, приходится отменять из-за развития побочных эффектов. В отличие от тиазидных диуретиков, БАБ и иАПФ антигипертензивная эффективность блокаторов АТ1-ангиотензиновых рецепторов не зависит от возраста, пола или расы больных [15].
Ренин-ангиотензин-альдостероновая система (РААС) играет центральную роль как в возникновении АГ, так и в реализации патофизиологических процессов, которые в конечном итоге приводят к серьезным сердечно-сосудистым осложнениям, таким как мозговой инсульт, инфаркт миокарда, сосудистое ремоделирование, нефропатия, застойная сердечная недостаточность и развитие атеросклеротических процессов. иАПФ были первой группой препаратов, действующих непосредственно на РААС, которые широко внедрены в клиническую практику. Длительный период их применения, многочисленные клинические исследования, большой опыт практических врачей по их использованию привели к тому, что в настоящее время в России данные препараты используются чаще других антигипертензивных средств. иАПФ в средних дозах снижают САД несколько в меньшей степени, чем диуретики и антагонисты кальция. Выбор конкретного иАПФ для длительной терапии больных с АГ имеет важное клиническое значение, поскольку эти препараты назначают, по существу, пожизненно. Из иАПФ с доказанной эффективностью наиболее перспективными представляются периндоприл и рамиприл [16, 17].
Клиническая практика и результаты многих мультицентровых исследований показали, что применение монотерапии в лечении АГ редко приводит к целевым уровням АД, увеличивает риск развития нежелательных явлений и снижает приверженность пациента к лечению. Важнейшими условиями повышения приверженности пациентов к лечению являются понимание ими целей, задач, современных методов и принципов лечения, а также правильный выбор варианта антигипертензивного лечения врачом. Тактика использования комбинированной терапии с подбором препаратов разного механизма действия уже в начале лечения дает значительно больше шансов на успешный контроль АД. Низкодозовая комбинированная рациональная гипотензивная терапия может быть мерой первого выбора, особенно у пациентов с высоким риском развития сердечно-сосудистых осложнений, к достоинствам которой можно отнести: простой и удобный режим приема для пациента; облегчение титрации; простота прописывания препарата; повышение приверженности пациентов; уменьшение нежелательных явлений за счет снижения доз применяемых компонентов; уменьшение риска использования нерациональных комбинаций; уверенность в оптимальном и безопасном дозовом режиме; уменьшение цены [17–21].
Следует отметить, что в последних и американских, и европейских рекомендациях подчеркивается необходимость избегать по возможности тактики частой смены лекарств и их дозировок у пациентов. В настоящее время становится очевидным, что эффективность монотерапии препаратами всех основных групп невысокая и сопоставимая: через год лечения даже при почти идеальной приверженности лечению эффект монотерапии не превышает 50% против почти 30% при плацебо. Тактика «последовательной монотерапии» в реальности может потребовать 4–5 смен терапии, каждая из которых может осложниться развитием побочных эффектов. Такая тактика занимает много времени, лишает врача и пациента уверенности в успехе, что в конечном итоге оказывает негативное психологическое воздействие на пациента и ведет к низкой приверженности лечению АГ. Именно недооценка роли комбинированной терапии является одной из частых причин неудовлетворительного контроля АД [17–21].
Комбинированная антигипертензивная терапия имеет много преимуществ:
- усиление антигипертензивного эффекта за счет разнонаправленного действия препаратов на патогенетические механизмы развития АГ, что увеличивает число пациентов со стабильным снижением АД;
- уменьшение частоты возникновения побочных эффектов как за счет меньших доз комбинируемых антигипертензивных препаратов, так и за счет взаимной нейтрализации этих эффектов;
- обеспечение наиболее эффективной органопротекции и уменьшение риска развития и числа сердечно-сосудистых осложнений.
Многочисленные рандомизированные клинические исследования и опыт реальной клинической практики показали все плюсы комбинированной терапии, которые могут быть суммированы следующим образом [22, 23]:
- одновременное использование препаратов двух различных фармакологических групп более активно снижает АД за счет того, что происходит воздействие на различные патогенетические механизмы гипертензии;
- совместное применение более низких доз двух препаратов, действующих на различные регуляторные системы, позволит лучше контролировать АД, учитывая неоднородность реакции больных гипертонической болезнью на антигипертензивные средства;
- назначение второго препарата может ослаблять или уравновешивать запуск механизмов противодействия понижению АД, возникающих при назначении одного препарата;
- устойчивое понижение АД может быть достигнуто меньшими дозами двух препаратов (чем при проведении монотерапии);
- меньшие дозы позволяют избежать дозозависимых побочных эффектов, вероятность которых более высока при большей дозе того или иного препарата (при проведении монотерапии);
- применение двух препаратов может в большей степени предотвращать поражение органов-мишеней (сердце, почки), обусловленное АГ;
- назначение второго препарата может в определенной мере уменьшать (и даже полностью ликвидировать) нежелательные эффекты, обусловленные первым (пусть даже и вполне эффективным) препаратом;
- назначение второго препарата (в частности, мочегонного) позволяет получить быстрый антигипертензивный эффект комбинации лекарств, т. к. большинство антигипертензивных препаратов (иАПФ, БКК, БРА, а отчасти и БАБ) проявляют в полной мере свое действие лишь на 2–3-й нед. приема (и даже позже).
Комбинации двух антигипертензивных препаратов делят на рациональные (эффективные), возможные и нерациональные. Все преимущества комбинированной терапии присущи только рациональным комбинациям антигипертензивных препаратов [24].
К ним относятся [10]:
- иАПФ + диуретик;
- БРА + диуретик;
- иАПФ + дигидропиридиновый БМКК;
- БРА + дигидропиридиновый БМКК;
- дигидропиридиновый БМКК + БАБ;
- дигидропиридиновый БМКК + диуретик;
- БАБ + диуретик;
- БАБ + α-адреноблокатор.
Вопрос комбинирования трех и более препаратов еще недостаточно изучен, поскольку нет результатов рандомизированных контролируемых клинических исследований, изучавших тройную комбинацию антигипертензивных препаратов. Таким образом, антигипертензивные препараты в данных комбинациях объединены вместе на теоретической основе. Однако у многих пациентов, в т. ч. у больных с рефрактерной АГ, только с помощью трех и более компонентной антигипертензивной терапии можно достичь целевого уровня АД [25]. К рекомендуемым комбинациям трех антигипертензивных препаратов относятся:
- иАПФ + дигидропиридиновый БМКК + БАБ;
- БРА + дигидропиридиновый БМКК + БАБ;
- иАПФ + БМКК + диуретик;
- БРА + БМКК + диуретик;
- иАПФ + диуретик + БАБ;
- БРА + диуретик + БАБ;
- дигидропиридиновый БМКК + диуретик + БАБ.
Поскольку комбинированная терапия стала одним из основных направлений в лечении больных с АГ, широкое распространение получили фиксированные комбинации антигипертензивных препаратов, содержащие в одной таблетке два лекарственных средства, что улучшает психологический настрой больного на лечение и дает возможность снизить риск осложнений и побочных эффектов. Оптимальное сочетание компонентов подразумевает отсутствие нежелательной гипотонии, которая может привести, особенно у пожилых пациентов, к повышению сердечно-сосудистого риска. Рациональный подбор компонентов по фармакокинетическому профилю создает предпосылки для однократного использования препаратов, которые в режиме монотерапии требуют двух- или трехкратного применения.
К преимуществам фиксированных (официнальных) комбинаций можно отнести:
- потенциирование антигипертензивного эффекта препаратов;
- простоту назначения и процесса титрования дозы;
- уменьшение частоты побочных эффектов (низкая доза, взаимная нейтрализация НЛР);
- увеличение приверженности пациентов к лечению;
- уменьшение стоимости лечения.
В настоящее время существует достаточно много официнальных комбинированных препаратов: Капозид (каптоприл + ГХТЗ), Ко-ренитек (эналаприл + ГХТЗ), Нолипрел (периндоприл + индапамид), Аккузид (квинаприл + ГХТЗ), Ко-диован (валсартан + ГХТЗ), Гизаар (лозартан + ГХТЗ), Эксфорж (валсартан + амлодипин), Экватор (лизиноприл + амлодипин), Логимакс (метопролол + фелодипин), Тарка (верапамил + трандолаприл) и др. Наиболее часто назначаемой из всех нефиксированных и фиксированных комбинаций ЛС является комбинация иАПФ с тиазидным диуретиком или БРА с тиазидным диуретиком. Высокая эффективность и безопасность данной комбинации при лечении АГ отмечена в рекомендациях ВОЗ, ВНОК, ЕОГ – ЕОК и JNS 7. Действие блокаторов АТ-рецепторов типа 1 специфично, поскольку они в отличие от иАПФ не влияют на активность других нейрогуморальных систем, в частности брадикинина, с которыми связывают характерные побочные эффекты (сухой кашель и ангионевротический отек). Эффект «ускользания» фармакологической блокады РААС от действия иАПФ объясняется синтезом ангиотензина II в некоторых органах и тканях с помощью других ферментов без участия АПФ.
В настоящее время считается, что хроническая стимуляция РААС ведет к активации факторов роста и фиброза на тканевом уровне, что определяет развитие патологических процессов в органах-мишенях, поэтому возможность блокады тканевого звена РААС представляется перспективной для достижения органопротективного эффекта антигипертензивной терапии. В ряде исследований не было выявлено прямой зависимости рено- и кардиопротективного эффекта антигипертензивной терапии от степени снижения АД, что свидетельствует о важности негемодинамических эффектов блокады РААС. При совместном применении тиазидные диуретики не только усиливают, но и удлиняют антигипертензивное действие БРА. Доказано, что совместное применение БРА и мочегонных препаратов приводит к заметному снижению АД у пациентов как с высокой, так и с низкой активностью ренина, и ответ на данную комбинированную терапию составляет около 80% и выше.
Также примером благоприятной комбинации является сочетание БМКК с иАПФ, что приводит к уменьшению выраженности отеков, ассоциированных с применением дигидропиридинов. Кроме того, комбинация недигидропиридинового БМКК с иАПФ может потенциально усиливать положительный эффект последнего в отношении эластических свойств сосудов.
К комбинациям нерациональным, при которых не происходит потенцирования антигипертензивного эффекта препаратов и/или усиливаются побочные эффекты при их совместном применении, относятся сочетания БАБ и препаратов центрального действия, БАБ и БМКК недигидропиридинового ряда и БАБ с иАПФ, БРА, агонистами имидазолиновых рецепторов. Комбинация иАПФ и БРА в настоящее время считается запрещенной.
Заключение
Важнейшими условиями повышения приверженности пациентов к лечению являются понимание ими целей, задач, современных методов и принципов лечения, а также правильный выбор варианта антигипертензивного лечения врачом. Тактика использования комбинированной терапии с подбором препаратов разного механизма действия уже в начале лечения дает значительно больше шансов на успешный контроль АД и риска развития сердечно-сосудистых осложнений. Преимущества комбинированной терапии заключаются в потенцировании антигипертензивного эффекта и уменьшении числа побочных эффектов и присущи лишь так называемым рациональным комбинациям гипотензивных препаратов. Для адекватного лечения АГ целесообразно использовать комбинированную терапию, начиная с низких доз препаратов.
Литература
- Оганов Р.Г., Тимофеева Т.Н., Колтунов И.Е. и др. Эпидемиология артериальной гипертонии в России. Результаты федерального мониторинга 2003-2010 гг // Кардиоваскулярная терапия и профилактика. 2011. № 1. С. 9–13.
- ABC Of Hypertension / edited by D. Gareth Beevers, Gregory H. Lip and Eoin O’Brien. 5th ed. Malden, Mass.: BMJ Books, 2007. p. 88.
- Ezzati M., Lopez A.D., Rodgers A. et al. Selected major risk factors and global and regional burden of disease // Lancet. 2002. Vol. 360(9343). P. 1347–1360.
- Hansson L., Zanchetti A., Carruthers S.G. et al. Effects of intensive blood–pressure lowering and low–dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial // Lancet. 1998. Vol. 351. P. 1755–1762.
- Dahlof B. Sweedish trial in old patients with hypertension (STOP-Hypertension). // Clm. Exp. Hypertens. 1993. Vol. 15. P. 925–939.
- Чазова И.Е., Беленков Ю.Н. РОСА – Российское исследование по оптимальному снижению артериального давления. https://www. cardiosite.ru/ research/article.asp? id=2559.
- Карпов Ю.А.Комбинированная терапия артериальной гипертонии – эффект контроля и успех лечения // РМЖ. 2006. № 20. С. 1458–1461.
- 1999 World Health Organization – International Society of Hypertension Guidelines for the Management of Hypertension // J. Hypertens. 1999. Vol. 17. P. 151–183.
- Кобалава Ж.Д. Эволюция комбинированной антигипертензивной терапии: от многокомпонентных высокодозовых свободных комбинаций до низкодозовых фиксированных комбинаций как средств первого выбора // РМЖ. 2001. № 18. С. 789–794.
- Диагностика и лечение артериальной гипертензии. Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов. Четвертый пересмотр // Системные гипертензии. 2010. № 3. С. 5–26.
- ESH-ESC Guidelines Committee. 2013 guidelines for the management of arterial hypertension // J. Hypertension. 2013. Vol. 31. P. 1281–1357.
- Карпов Ю.А. Новые рекомендации по артериальной гипертензии РМОАГ/ВНОК 2010 г.: вопросы комбинированной терапии // РМЖ. 2010. № 22. С. 1290.
- Полосьянц О.Б. Сартаны в кардиологической практике // РМЖ. 2008. № 11. С. 1593–1597.
- Преображенский Д.В., Пересыпко М.К., Носенко Н.С. и др. Блокаторы АТ1-ангиотензиновых рецепторов: диапазон органопротективных эффектов // Справочник поликлинического врача. 2004. № 1. С. 8–14.
- Matcar D.B., McCrory D.C., Orlando L.A. et al. Comparative Effectiveness of Angiotensin-Converting Enzyme Inhibitors (ACEIs) and Angiotensin II Receptor Antagonists (ARBs) for Treating Essential Hypertension. Comparative Effectiveness Review No. 10. (Prepared by Duke Evidence-based Practice Center under Contract No. 290-02-0025.) Rockville, MD: Agency for Healthcare Research and Quality. November 2007. Available at: www.effectivehealthcare.ahrq.gov/ reports/final.cfm
- Моисеев С.В. Валсартан: от реалий клинической практики к новым возможностям // Клиническая фармакология и фармакотерапия. 2009. № 3. С. 32–43.
- Кириченко А.А., Эбзеева Е.Ю. Дифференцированный подход к лечению артериальной гипертензии // Consilium Medicum. 2006. Т. 4. № 3.
- Преображенский Д.В., Стеценко Т.М. и др. Терапия гипертонической болезни: комбинации ингибитора АПФ и диуретика // Consilium Medicum. 2006. Т. 4. № 7.
- 1999 World Health Organization – International Society of Hypertension Guidelines for the Management of Hypertension // J. Hypertens. 1999. Vol. 17. P. 151–183.
- Gosse P., Sheridan D.J., Zannad F. et al. Regression of LVH in hypertensive patients treated with indapamide SR 1,5 mg versus enalapril 20 mg: the LIVE study // J. Hypertens. 2000. Vol. 18. P. 1465–1475.
- Chalmers J., Castaigne A., Morgan T. et al. Long-term efficacy of a new, fixed, very-low-dose angiotesin-converting enzyme-inhibitor/diuretic combination as first-line therapy in elderly hypertensive patients // J. Hypertens. 2000. Vol. 18. P.1–11.
- Бубнова М.Г. Современные принципы профилактики и лечения артериальной гипертонии. Анализ основных положений международных рекомендаций // Справочник поликлинического врача. 2005. № 4. С. 8–14.
- Преображенский Д.В., Стеценко Т.М. и др. Выбор оптимального препарата для длительной терапии артериальной гипертензии // Consilium Рrovisorum. 2005. № 2. С. 21–23.
- Арутюнов Г.П., Розанов А.В. Фармакотерапия артериальной гипертензии: место фиксированных комбинаций лекарственных препаратов // Артериальная гипертензия. 2003. № 6. С. 218–221.
- Чазова И.Е., Беленков Ю.Н., Ратова Л.Г. и др. От идеи к клинической практике. Первые результаты российского национального исследования оптимального снижения артериального давления (РОСА) // Сист. гиперт. 2004. № 2. С. 18–23.
- Chalmers J., Castaigne A., Morgan T. et al. Long-term efficacy of a new, fixed, very-low-dose angiotesin-converting enzyme-inhibitor/diuretic combination as first-line therapy in elderly hypertensive patients // J. Hypertens. 2000. Vol. 18. P. 1–11.
Антигипертензивная терапия как основа нейропротекции в современной клинической практике
Артериальная гипертензия (АГ) — одна из актуальнейших проблем современной терапии, кардиологии и неврологии. Распространенность АГ в европейских странах, в том числе и РФ, находится в диапазоне 30–45% от общей популяции, с резким возрастанием по мере старения населения. АГ является ведущим фактором риска развития сердечно-сосудистых заболеваний (ССЗ), таких как инфаркт миокарда (ИМ), мозговой инсульт, ишемическая болезнь сердца (ИБС), хроническая сердечная недостаточность (ХСН), а также цереброваскулярных заболеваний (ЦВЗ): хронической ишемии головного мозга (ХИМ), гипертонической энцефалопатии, ишемического или геморрагического инсульта, транзиторной ишемической атаки. АГ является самым частым компонентом коморбидности в практике любого врача, присутствуя в 90% случаев всех возможных сочетаний заболеваний [1, 2]. Наиболее распространенный вариант коморбидности — АГ с атеросклерозом или дислипидемией. Основным осложнением атеросклероза коронарных артерий является ИБС, ИМ и кардиосклероз, ведущий к прогрессирующей ХСН, а поражение магистральных артерий головного мозга проявляется симптомами ХИМ с последующим развитием сосудистой деменции или мозгового инсульта [3, 4]. На сегодняшний день в мире около 9 млн человек страдают ЦВЗ. Все это делает актуальным постоянное изучение проблемы ранней диагностики и коррекции АГ с целью профилактики самых распространенных ССЗ и ЦВЗ [5].
Четырехкомпонентная антигипертензивная комбинация — возможности и преимущества
Ключевым моментом применения антигипертензивной терапии остается эффективный контроль артериального давления (АД) и достижение оптимальных значений, определяемых индивидуально для каждого пациента, с учетом всех имеющихся факторов риска ССЗ и сопутствующих состояний. Сегодня для лечения АГ рекомендованы пять основных классов антигипертензивных препаратов: ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов ангиотензина II (БРА), антагонисты кальция (АК), β-адреноблокаторы (ББ) и диуретики, для которых способность предупреждать развитие сердечно-сосудистых осложнений доказана в многочисленных рандомизированных клинических исследованиях. Все эти классы препаратов подходят для стартовой и поддерживающей терапии, как в виде монотерапии, так и в составе комбинаций. Ранний старт с рациональной комбинированной терапии является новым подходом, рекомендованным современными руководствами по лечению АГ [6, 7]. Рассмотрим, комбинации каких антигипертензивных препаратов являются рациональными, хорошо изученными и наиболее часто назначаемыми в современной терапии. иАПФ — блокируют образование ангиотензина II из ангиотензина I, препятствуя спазму сосудов и обеспечивая поддержание целевых цифр АД. В клинической практике чаще всего применяются такие препараты, как эналаприл, лизиноприл, каптоприл [7]. Эналаприл имеет наиболее обширную доказательную базу по уменьшению общей смертности — 7 исследований (n = 12 791 пациент) [8]. Отдельно нужно подчеркнуть, что в современной терапии именно эналаприлу принадлежит первенство по лечению и профилактике ХСН. Антигипертензивные препараты из группы диуретиков снижают нагрузку на миокард, уменьшая объем циркулирующей крови (ОЦК). Снижение ОЦК под действием диуретиков достигается за счет ускоренного выведения жидкости из организма. Петлевые диуретики снижают реабсорбцию Na+, K+, Cl– в толстой восходящей части петли Генле, уменьшая реабсорбцию жидкости, обладают достаточно выраженным и быстрым действием и, как правило, применяются только для экстренной помощи (для форсированного диуреза при отеке легких, гипергидратации и т. д.). Наиболее известным препаратом в данной группе является фуросемид. Тиазидоподобные диуретики (гипотиазид, индапамид, хлорталидон), уменьшая реабсорбцию Na+ и Cl– в толстом сегменте восходящей петли Генле и в начальном отделе дистального канальца нефрона, снижают реабсорбцию мочи. При их систематическом приеме у больных с АГ снижается риск сердечно-сосудистых осложнений. Представитель тиазидоподобных диуретиков — индапамид не вызывает нарушений липидного и углеводного обменов, в связи с чем широко применяется у пациентов с различными вариантами метаболических нарушений, в отличие от других представителей данного класса. Также возможна комбинация с ББ, которые действуют на сосудистую систему, стимулируя b-адренорецепторы, и широко используются в клинической практике у больных с АГ и сосудистой коморбидностью. ББ снижают частоту сердечных сокращений, удлиняя диастолу и улучшая кровоснабжение миокарда, так как сердце получает необходимые для функционирования вещества из крови только в период диастолы. Независимые рандомизированные исследования подтверждают снижение частоты сердечных сокращений и увеличение продолжительности жизни пациентов при длительном приеме ББ [5]. Наиболее популярные ББ с доказанным улучшением прогноза, в том числе у больных с ИБС, это метопролол, бисопролол, карведиол. Не менее широко, чем ББ, в клинической практике лечения АГ используются АК. Эти препараты блокируют вход кальция в клетки гладкой мускулатуры сосудов и кардиомиоциты. Такая блокада сопровождается вазодилатацией, но, одновременно, и ослаблением сократительной способности миокарда. Кроме того, АК снижают активность синусового узла, а при падении АД — могут вызывать тахикардию. Таким образом, при кратком обсуждении наиболее часто назначаемых классов препаратов в виде моно- или комбинированной терапии, с учетом данных доказательной медицины, дополнительных свойств и, конечно экономической составляющей лечения, получилось выявить лидеров. Так был создан современный низкодозовый нейропротективный комбинированный препарат Гипотэф. В состав Гипотэфа входят эналаприл, индапамид, метопролола тартрат и винпоцетин, он обладает комплексным действием, влияя на все этапы развития повреждений органов-мишеней при АГ, что особенно важно у пациентов с ЦВЗ. Особенностью Гипотэфа является не только уникальная комбинация трех наиболее востребованных антигипертензивных классов, обеспечивающих многогранную органопротективную поддержку и улучшающих прогноз, но и входящий в состав препарата ноотроп — винпоцетин, потенцирующий антигипертензивное действие и обладающий мощной доказательной базой по улучшению состояния мозгового кровообращения [9]. Эффективность винпоцетина была неоднократно подтверждена в широкомасштабных исследованиях, так, было показано, что терапия винпоцетином способствует уменьшению выраженности таких неврологических симптомов, как головная боль, головокружение, шум в ушах у пациентов с АГ, а также достоверное улучшение настроения и памяти. У пациентов после перенесенного ишемического инсульта использование винпоцетина, по сравнению с группой контроля, в большей степени способствовало регрессу речевых, двигательных и расстройств памяти [9]. Гипотэф оказывает равномерный, длительный антигипертензивный эффект с достижением целевых значений АД, сравнимый с действием 20 мг эналаприла или 50 мг метопролола [10]. Плавное снижение АД хорошо переносилось пациентами, без симптомов гипотонии, даже при значительном снижении АД (максимально до –31,3/16 мм рт. ст. за 12 недель лечения) [11]. Сравнительное исследование ФОРСАЖ с современными гипотензивными комбинациями показало такую же органопротективную эффективность Гипотэфа в отношении почек и сердца и более высокую эффективность в отношении уменьшения сосудистого возраста (в 1,5 раза), жесткости артерий (в 1,5 раза) и толщины комплекса интима-медиа (в 1,7 раза) [12, 13]. Гипотэф нормализует суточную вариабельность: в группе Гипотэфа количество «дипперов» выросло на 32%, а в группе, принимавшей другие современные комбинации, только на 25%, при этом в данной группе возросло число пациентов с избыточным ночным снижением АД. При сопоставимом гипотензивном эффекте, Гипотэф хорошо переносился пациентами, не было ни одного случая гипотонии, приверженность пациентов была выше, чем в группах сравнения [11–13]. Возможность эффективного применения препарата Гипотэф у пациента с АГ и высоким дополнительным риском может быть рассмотрена в следующем клиническом примере.
На прием к врачу общей практики в районную поликлинику обратилась пациентка А., 1965 г. р., с жалобами на учащенное сердцебиение, головную боль, частые головокружения, «шум и звон» в ушах, выраженную утомляемость при нагрузке, нарушения памяти.
Наследственность: отец — инсульт, острый коронарный синдром в возрасте 50 лет; мать — АГ, ИБС, сахарный диабет 2 типа, сестра — АГ, сахарный диабет 2 типа.
Анамнез. В течение нескольких лет — повышение АД до maх 200/110 мм рт. ст., в качестве антигипертензивной терапии в настоящий момент получает эналаприл 5 мг 2 раза в день, адаптирована к 150/90 мм рт. ст. Несколько лет назад впервые была выявлена гипергликемия натощак, при проведении теста с 75 г глюкозы — выявлена нарушенная толерантность к глюкозе. С тех пор пациентка соблюдает диету, за весом следит, вес стабильный.
Перенесенные заболевания: частые простудные заболевания, язвенная болезнь 12-перстной кишки.
Эпиданамнез: туберкулез, вирусные гепатиты, сахарный диабет отрицает.
Вредные привычки: курит, алкоголь — не злоупотребляет.
Аллергологический анамнез: капли в нос Пиносол — отек Квинке.
Настоящее состояние: общее состояние удовлетворительное.
При физическом исследовании: рост пациентки 175 см, вес 95 кг, индекс массы тела — 31 кг/м2, окружность талии — 112 см, окружность бедер — 100 см, а соотношение объема талии к объему бедер > 0,95, что свидетельствует об абдоминальном типе ожирения, который, как правило, сочетается с метаболическими нарушениями. Гиперстенического телосложения. Кожные покровы нормальной окраски. Подкожно-жировая клетчатка развита умеренно. Отеков нет. В легких дыхание везикулярное, хрипов нет. ЧДД = 16 в минуту. Тоны сердца ясные, ритмичные, ЧСС = 88 в минуту. АД = 152/90 мм рт. ст. Живот мягкий, безболезненный при пальпации. Печень не увеличена. Симптом поколачивания отрицательный с обеих сторон.
По результатам лабораторно-инструментального обследования изменений в результатах клинических анализов крови и мочи не выявлено. Биохимический анализ представлен в табл. 1.
По данным эхокардиографии: признаки гипертрофии левого желудочка. Фракция выброса левого желудочка — 61%.
Результаты суточного мониторирования АД (табл. 2) подтвердили наличие АГ, несмотря на принимаемую терапию. Среднее систолическое АД (САД) за сутки составило 154 мм рт. ст. (дневное САД — 157 мм рт. ст.), диастолическое АД (ДАД) — 95 мм рт. ст., что превысило нормальные значения. Отмечено нарушение суточного ритма САД по типу non-dipper, т. е. отсутствие достаточного снижения АД в ночное время, особенно неблагоприятное в отношении развития осложнений в виде инсульта, инфаркта, хронической ишемии мозга и когнитивных нарушений.
Диагноз: «Артериальная гипертензия, 1-я степень, риск IV. НК — 0. Гиперлипидемия IIb. Ожирение 1-й степени. Висцеральный тип ожирения. Предиабет: нарушенная толерантность к глюкозе. Нарушенная гликемия натощак. Язвенная болезнь 12-перстной кишки вне обострения».
Получаемая терапия на момент обращения: Энап 5 мг 2 раза/день (утром, вечером); Омез 20 мг 1 раз/день (на ночь).
Была проведена коррекция получаемой терапии:
1) Энап заменен на препарат Гипотэф — 1 таблетка утром и 1 таблетка вечером; 2) к терапии был добавлен препарат питавастатин 4 мг по 1 таблетке вечером после ужина.
При повторном осмотре пациентки через 3 месяца выявлено, что на фоне проводимой терапии состояние пациентки значительно улучшилось: головные боли регрессировали, улучшилось общее самочувствие, повысилась работоспособность, исчезло ощущение «шума и звона» в ушах, а также «провалов» в памяти. Для оценки эффективности терапии было проведено повторное суточное мониторирование АД, результаты подтвердили достижение целевых значений — до 125/80 мм рт. ст. и нормализацию суточного профиля АД (табл. 3). Биохимический анализ показал достижение целевых значений уровней ЛПНП и общего холестерина (табл. 4). Также было отмечено отсутствие ухудшения углеводных нарушений на фоне проводимой терапии.
Таким образом, назначенная пациентке рациональная антигипертензивная терапия в виде низкодозового комбинированного нейропротективного препарата Гипотэф и статинотерапия показали высокую эффективность в короткие сроки. Исчезновение таких симптомов, как головная боль, головокружение, шум в ушах, а также субъективное ощущение улучшения памяти делает пациентку приверженной к данной терапии и дает возможность проведения длительного лечения. Пациентка переносит назначенную терапию хорошо, ей рекомендовано продолжить прием всех назначенных ранее препаратов под контролем уровня липидов и АД.
Учитывая современные рекомендации по лечению АГ и данные по изучению клинической эффективности препарата Гипотэф, представляется возможным говорить о действительно рациональном решении множества проблем у пациента с АГ с помощью одного уникального четырехкомпонентного нейропротективного препарата — Гипотэф, что может значимо повысить качество жизни пациента и избежать небезопасной полипрагмазии.
Литература
- Redon J., Olsen M. H., Cooper R. S., Zurriaga O., Martinez-Beneito M. A., Laurent S. et al. Stroke mortality trends from 1990 to 2006 in 39 countries from Europe and Central Asia: implications for control of high blood pressure // Eur Heart J. 2011; 32: 1424–1431.
- Шишкова В. Н. Нейропротекция у пациентов с артериальной гипертонией: минимизация неблагоприятного прогноза // Терапевтический архив. 2014; 8: 113–118.
- Шишкова В. Н. Когнитивные нарушения как универсальный клинический синдром в практике терапевта // Терапевтический архив. 2014; 11: 128–134.
- Инсульт. Руководство для врачей / Под ред. Котова С. В., Стаховской Л. В. М: Издательство МИА, 2013.
- Шишкова. В. Н., Адашева Т. В., Капустина Л. А. Основы профилактики инсульта в современной клинической практике // Врач. 2018; 29 (7): 3–12.
- Чазова И. Е., Жернакова Ю. В. от имени экспертов. Клинические рекомендации. Диагностика и лечение артериальной гипертонии // Системные гипертензии. 2019; 16 (1): 6–31.
- 2018 ЕОК/ЕОАГ Рекомендации по лечению больных с артериальной гипертензией // Российский кардиологический журнал. 2018; 23 (12): 143–228.
- Корзун А. И., Кириллова М. В. Сравнительная характеристика ингибиторов АПФ. СПб: ВМедА, 2003. 24 с.
- Чуканова Е. И. Современные аспекты эпидемиологии и лечения хронической ишемии мозга на фоне артериальной гипертензии (результаты программы КАЛИПСО) // Неврология, нейропсихиатрия, психосоматика. 2011; 3 (1): 38–42.
- Евдокимова А. Г. и др. Клиническая эффективность комбинированной антигипертензивной терапии в фиксированных дозах: фокус на Гипотэф // Терапия. 2016; 6 (10): 68–78.
- Скотников А. С., Хамурзова М. А. Органопротективные свойства гипотензивной терапии как профилактика развития «сосудистой» коморбидности // Лечащий Врач. 2017; 7: 16–24.
- Скотников А. С., Юдина Д. Ю., Стахнев Е. Ю. Гипотензивная терапия коморбидного больного: на что ориентироваться в выборе лекарственного средства // Лечащий Врач. 2018; 2: 24–30.
- Скотников А. С., Хамурзова М. А. Новые комбинации для комплексного лечения артериальной гипертензии в помощь врачу общей практики // Поликлиника. Кардиолог сегодня. Спецвыпуск. 2017/2018; 1: 47–55.
В. Н. Шишкова, кандидат медицинских наук
ФГБОУ ВО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
Контактная информация
DOI: 10.26295/OS.2019.68.63.015
Антигипертензивная терапия как основа нейропротекции в современной клинической практике/ В. Н. Шишкова Для цитирования: Лечащий врач № 6/2019; Номера страниц в выпуске: 68-73 Теги: антигипертезнизная терапия, органопротективная поддержка, коморбидность, мозговое кровообращение