Статья опубликована на с. 49-52
Изолированный стеноз легочной артерии (ИСЛА) — это врожденная аномалия, характеризующаяся наличием обструкции выходного тракта правого желудочка и нарушением путей оттока крови из него в малый круг кровообращения. Согласно МКБ-10, выделяют Q 25.6 «Стеноз легочной артерии». Первые описания порока принадлежат J.B. De Senac (1749) и G.B. Morgagni (1761).
Частота ИСЛА, по секционным и клиническим данным, составляет среди всех врожденных пороков сердца (ВПС) от 2,4 до 12 %.
Патогенез
У здорового человека давление в правом желудочке и артерии, несущей кровь к лёгким — одинаковое. У клапана легочной артерии строение трёхстворчатое и когда возникает сокращение правого желудочка — все его створки полностью под воздействием тока крови раскрываются и способствуют её свободному поступлению в пространство легочной артерии. Затем происходит расслабление стенок правого желудочка и наполнение его венозной кровью, поступившей от органов и тканей организма, что вызывает смыкание створок клапана и обеспечивает полное смыкание для обратного тока крови и невозможность проникновения биологических жидкостей в обратном направлении — от легочной артерии к правому желудочку.
Патогенез, вызывающий клапанный стеноз легочной артерии
В случае клапанного стеноза за счет частичного сращения створок полное их открытие становится невозможным, возникает стеноз клапана и разница в давлении — в желудочке оно слишком высокое, а в легочной артерии – достаточно низкое для формирования градиента давления. В некоторых случаях клапанный стеноз вызывает выбухание деформированных створок в систолу в просвет ствола в легочную артерию и ускорение систолического потока.
Стенозированный клапан
В результате легочного стеноза для компенсации нарушения гемодинамики правый желудочек вынужден работать сверхусиленно, чтобы протолкнуть кровь через суженный просвет. Это может привести к растяжению, ригидности и гипертрофии (утолщению) стенок, в результате чего увеличивается его полость, нарушается ритм и развивается сердечная недостаточность. Место сужения снижает объем кровяного тока, а недостаточность кровоснабжения легких вызывает частые бронхо-легочные заболевания.
Прогноз
У детей с успешно проведенной баллонной пластикой клапана прогноз для жизни благоприятный. У пациентов с диспластичным легочным клапаном, часто выявляемым при синдроме Нунан, исходы менее благоприятные. Пациенты с успешно проведенной баллонной пластикой редко нуждаются в повторной операции в отличие от пациентов с гипоплазией правого желудочка. Выживаемость у таких детей составляет 60 %. Легкий и умеренный стеноз легочной артерии обычно не прогрессирует, и дети имеют благоприятный прогноз. У больных с тяжелым стенозом с возрастом отмечается прогрессирование порока. Средняя продолжительность жизни при естественном течении порока составляет 25 лет. После операции возможны рестенозирование и клапанная недостаточность легочной артерии. Отдаленный хороший результат после оперативного лечения зафиксирован у 84,3 % больных.
Классификация
В зависимости от места сужения различают:
- клапанный стеноз – наиболее частый случай, когда патологическим изменениям подвержен сам клапан легочной артерии, его створки могут быть недоразвитыми, срощенными между собой комиссурами и даже иметь вид мембраны с отверстием по центру, размером от 1-1,5 мм до нормального;
- надклапанный – при котором сужен ствол легочной артерии выше места расположения клапана;
- подклапанный (инфундибулярный) – при этом произошло чрезмерное разрастание мышечных тканей или фиброзных структур в области выходного отдела правого желудочка препятствует выходу кровяного тока в легочную магистраль;
- периферический – вызван сужением веток легочной артерии, приносящих кровь к правому либо левому лёгкому.
По характеру выраженности болезнь бывает легкой (бессимптомной), средне-тяжелой и критической формы.
Лечение
Лечение вторичной легочной гипертензии направлено на избавление от основного заболевания. Пациентам с тяжелой легочной артериальной гипертензией вследствие хронической тромбоэмболии назначают легочную тромбоэндартериэктомию. Эта операция считается более сложной, по сравнению с экстренной хирургической эмболэктомией. В условиях экстрапульмонального кровообращения организованный васкуляризованный тромб иссекается вдоль легочного ствола. В специализированных центрах процент летальности в ходе и после операции составляет менее чем 10%.
Лечение первичной легочной гипертензии нужно начинать с пероральных блокаторов кальциевых каналов. У меньшинства пациентов с помощью этих препаратов снижается давление в легочной артерии или легочное сопротивление сосудов. Большинство врачей не советуют верапамил, потому что он имеет отрицательный инотропный эффект. Если лечение блокаторами кальциевых каналов эффективно, прогноз благоприятный, нужно продолжать курс. Если ответа на лечение не последовало, врач назначает другие препараты.
Внутривенный эпопростенол (аналог простациклина) часто применяются для лечения легочной гипертензии. Он увеличивает выживаемость пациентов, даже тех, которым не помогают сосудорасширяющие лекарства во время катетеризации. Такое лечение имеет недостатвки, например, потребность в постоянном центральном катетере. Также появляются побочные действия, например, бактериемия и понос. Альтернативными препаратами считаются пероральные (берапрост), ингаляционные (илопрост), подкожные (трепростинил) аналоги простациклина. Но их действия на организм человека пока что изучается, потому они не внедрены широко в медицинскую практику.
Пероральный антагонист рецепторов эндотелина бозентан в части случаев эффективен. В основном его назначают при более легкой форме легочной гипертензии и нечувствительности к сосудорасширяющим препаратам. На стадии исследования на сегодняшний день также находятся L-аргинин и пероральный силденафил.
Трансплантация легкого — опасная процедура, при которой могут возникнуть осложнения, потому что возможно инфекционное заражение и отторжение организмом нового легкого. К процедуре прибегают при сердечной недостаточности четвертой степени (по классификации Нью-Йоркской кардиологической ассоциации), когда у человека даже при минимальной активности появляется одышка, из-за чего он не может активно жить, а постоянно лежит или сидит; и только если в таких случаях нет эффективности аналогов простацикпина.
Многим больным назначают дополнительные лекарственные средства для терапии недостаточности, включая мочегонные средства. Также они должны получать варфарин с целью профилактики тромбоэмболии.
Симптомы
Клиническая картина может значительно отличаться в зависимости от выраженности стеноза и протекать даже бессимптомно, к примеру, если градиент давления между сердцем и артерией не превышает 25 мм рт ст. Таким людям даже не назначаю лечения.
Симптомокомплекс обычно проявляется в виде нарастающе-убывающего шума изгнания, синюшности кожных покровов, развитие «сердечного горба» и различных признаков сердечной недостаточности, включая:
- беспричинные обмороки;
- отечность;
- увеличение печени;
- частые боли и дискомфорт груди («грудная жаба»);
- одышка.
Пороки сердца у детей
Пороки сердца являются нередкой патологией у детей. Частота пороков у детей в последние годы увеличивается. Консультация и осмотр детского кардиолога — детская поликлиника «Маркушка».
Врожденные пороки сердца у детей, ребенка
Частота врожденных пороков сердца (ВПС) у новорожденных детей составляет 0,8 %, они широко варьируют по анатомическим особенностям и тяжести течения. Клинические проявления ВПС у детей разнообразны и определяются тремя основными факторами: анатомическими особенностями порока, степенью компенсации и возникающими осложнениями.
ВПС у ребенка можно заподозрить, если у него выявляются: цианоз или выраженная бледность, гипотрофия, частые простудные заболевания, недостаточная переносимость адекватных по возрасту физических нагрузок (быстрая утомляемость при кормлении грудью, при подвижной игре, появление одышки при подъеме даже на один пролет лестницы и др.), увеличение размеров сердца, изменение тонов сердца, появление шумов в сердце, изменение пульса на руках, слабый пульс на бедренной артерии или его отсутствие, изменение артериального кровяного давления, деформация грудной клетки, нарушения ритма сердца, любые патологические изменения ЭКГ, необычные изменения, выявляемые на рентгенограмме грудной клетки и др.
Врожденные пороки сердца с обогащением малого круга кровообращения
Дефект межпредсердной перегородки (ДМПП) является одним из распространенных ВПС. В 10—20 % случаев ДМПП сочетается с пролапсом митрального клапана.
Гемодинамика при ДМПП определяется сбросом артериальной крови слева направо, что приводит к увеличению минутного объема малого круга кровообращения. В образовании шунта имеют значение разница давления между правым и левым предсердием, более высокое положение последнего, большая растяжимость правого желудочка и площадь правого атриовентрикулярного отверстия, сопротивление, объем сосудистого ложа легкого. Развитие легочной гипертензии и поражение сосудистого русла легких приводят к обратному шунтированию крови и появлению цианоза. При первичных дефектах часто наблюдается митральная недостаточность.
В отличие от дефектов межжелудочковой перегородки, при которых значительный сброс приводит к объемной перегрузке обоих желудочков, при ДМПП сброс крови меньше и влияет только на правые отделы сердца.
При выраженном сбросе у больных наблюдаются отставание в весе и склонность к повторным респираторным заболеваниям и пневмониям в первые годы жизни. Как правило, в этих случаях имеются жалобы на одышку, утомляемость, боли в сердце.
Дефект межжелудочковой перегородки (ДМЖП) является одним из наиболее часто встречающихся ВПС. На его долю приходится от 17 до 30 % случаев сердечных аномалий.
Выделяются три типа развития ДМЖП в зависимости от особенностей гемодинамики порока (величины лево-правого шунта), определяющих клинические проявления и прогноз заболевания.
Первый тип — имеется маленький дефект в перегородке (менее 0,5 см2/м2), малый сброс крови (< 25% ударного объема) не вызывает изменений давления в правом желудочке и малом круге кровообращения, легочная гипертензия не развивается. Клинические проявления отсутствуют. Дети с таким пороком не нуждаются в систематическом лечении.
Второй тип — средней величины дефект (0,5—1 см2/м2) приводит к большему сбросу крови в правый желудочек (< 50 % ударного объема) и среднему повышению давления в малом круге кровообращения. При этом типе ДМЖП мало выражены клинические признаки порока и не возникает проблем с лечением. Могут наблюдаться отставание в физическом развитии, застойная сердечная недостаточность, рецидивирующие нижнедолевые пневмонии. Оперируют таких детей в дошкольном возрасте.
Третий тип — большой дефект (более 1 см2/м2), когда сброс крови в правый желудочек превышает 50 % ударного объема. Характеризуется частыми бронхолегочными заболеваниями, нарушениями роста и признаками сердечной недостаточности, при выраженности которых прибегают к радикальной или паллиативной операции. При высоком легочном сопротивлении могут наблюдаться одышка в покое и при физической нагрузке, боли в груди, цианоз, кровохарканье. Большинство больных умирает в детском и подростковом возрасте.
Большинство дефектов межжелудочковой перегородки имеют малый размер и представляют риск в отношении инфекционного эндокардита.
Открытый аортальный проток у детей, ребенка
Артериальный (боталлов) проток соединяет легочную артерию и аорту непосредственно за левой подключичной артерией. Функциональное закрытие открытого аортального протока у доношенных детей происходит через 10—15 ч. после родов, облитерация протока — через несколько недель жизни. У недоношенных детей ОАП может функционировать от нескольких недель до месяца. У доношенных детей он остается открытым при структурных аномалиях, у недоношенных тем чаще, чем более незрелый ребенок, хотя спонтанное закрытие встречается часто.
При ОАП наблюдается сброс крови из аорты в легочную артерию из-за более высокого давления в аорте, что приводит к переполнению малого круга кровообращения и перегрузке левых камер сердца. При развитии легочной гипертензии присоединяется перегрузка и правого желудочка. Диаметр и длина протока определяют тяжесть сопутствующих гемодинамических нарушений, которые аналогичны таковым при ДМЖП различных размеров.
Обычно клинические проявления порока возникают в конце 1-го или на 2-3-м году жизни. Дети до появления клинических симптомов порока развиваются физически и нервнопсихически нормально, а первая фаза течения порока у части из них протекает легко. Ранние клинические признаки порока возникают при широких протоках.
Полная транспозиция магистральных сосудов у детей, ребенка
Полная транспозиция магистральных сосудов (ТМС) — аорта отходит от правого желудочка, легочная артерия — от левого, при этом образуются два отдельных и независимых друг от друга круга кровообращения. Жизнь ребенка после рождения возможна только при наличии компенсирующих коммуникаций. Этот порок сердца представляет собой основную причину смерти в первые два месяца жизни среди других ВПС.
Врожденные пороки сердца с обеднением малого круга кровообращения
Стеноз легочной артерии (СЛА) обусловлен чаще стенозом клапанов легочной артерии, реже — под- и надклапанным стенозом, стенозом ветвей легочной артерии. Подклапанный стеноз чаще является частью сложного ВПС.
Препятствие оттоку крови из правого желудочка в легочную артерию обусловливает повышение систолического давления и гипертрофию правого желудочка. Величина градиента давления зависит от размера отверстия клапанного кольца.
У большинства детей до года и старше заболевание протекает бессимптомно, хотя в некоторых случаях отмечается небольшая утомляемость.
Незначительный или умеренный СЛА может ничем не проявляться. При выраженном стенозе наблюдаются одышка, боли в сердце, бледность.
Тетрада Фалло
Тетрада Фалло характеризуется большим дефектом межжелудочковой перегородки, расположением аорты над местом дефекта, гипертрофией правого желудочка и стенозом легочной артерии.
Вследствие больших размеров ДМЖП систолическое давление одинаково в обоих желудочках и аорте. Степень обструкции правого желудочка определяет направление и объем сброса крови. В большинстве случаев он достаточно велик, чтобы преодолеть системное сопротивление и вызвать сброс справа налево и развитие цианоза. Размеры ДМЖП имеют второстепенное значение, так как его диаметр в основном равен диаметру устья аорты.
Различаются две основные формы ТФ. При крайнем варианте тетрады Фалло по типу общего ложного артериального ствола легочный ствол не работает, состояние ребенка тяжелое, наблюдается выраженное нарушение гемодинамики. Дети в 80 % случаев погибают на первом месяце жизни без оперативного вмешательства.
При классическом варианте тетрады Фалло имеются стеноз легочной артерии (чаще клапанный и выхода из правого желудочка), дефект межжелудочковой перегородки (мембранозная часть), декстрапозиция аорты (аорта над дефектом межжелудочковой перегородки), вторичная гипертрофия правого желудочка.
Дети отстают в физическом развитии, для них характерны одышка (при кормлении или движении ребенка), цианоз, деформация пальцев рук и ног («барабанные палочки»). Приступы усиливающегося цианоза с углублением дыхания — одышечно-цианотические — развиваются у детей до года и у детей младшего возраста. Прогноз неблагоприятный вследствие развития осложнений цианоза и полицитемии, таких как инсульт и абсцесс головного мозга. Часто развивается инфекционный эндокардит.
Врожденные пороки сердца с обеднением большого круга кровообращения
Коарктация аорты (КА). Сужение наблюдается ниже отхождения от аорты левой подключичной артерии. Хотя сужения могут локализоваться в любом участке, начиная от дуги и заканчивая бифуркацией аорты, в 98 % случаев они находятся в области ответвления артериального протока. При предуктивном стенозе (инфантильная форма) сужение наблюдается до ОАП, эта форма сочетается с другими пороками: ДМЖП, двустворчатым клапаном аорты, транспозицией магистральных сосудов и др.
Клинические проявления порока имеют место уже в период новорождения. Симптомы у детей первого года жизни характерны для сердечной недостаточности. Часто отмечаются затруднения при кормлении и низкий прирост массы тела. У детей старшего возраста заболевание обычно протекает бессимптомно, хотя возможно наличие небольшой утомляемости или слабости в ногах при беге.
Классическими признаками КА являются разные на руках и ногах пульс и артериальное давление: артериальная гипертензия на верхних конечностях и отсутствие или ослабление пульса на артериях ног и значительно более низкое АД на ногах, чем на руках (в норме на ногах АД на 10-20 мм рт. ст. выше, чем на руках). Выражена пульсация сосудов верхней половины тела, определяется приподнимающий левожелудочковый толчок. Границы сердца расширены влево.
Аортальный стеноз у детей, ребенка
Аортальный стеноз (АС) составляет около 5 % от всех ВПС у детей. Чаще распространен клапанный стеноз (около 80 %), реже (20 %) встречаются подклапанный и надклапанный варианты аортального стеноза. Аномалия строения аортального клапана (двустворчатость) относится к основным врожденным порокам сердца у взрослых. Течение и прогноз порока определяются его локализацией и выраженностью, сочетанием с другими пороками сердца и фиброэластозом, сопутствующим поражением миокарда.
При выраженном стенозе уже в грудном возрасте появляются признаки тяжелой левожелудочковой недостаточности, однако в большинстве случаев порок выявляется в школьном возрасте. Больные жалуются на утомляемость, одышку, боли в области сердца, головокружения, обморочные состояния.
Приобретенные пороки сердца у детей, ребенка
Приобретенные пороки сердца — приобретенные морфологические изменения клапанного аппарата, ведущие к нарушению его функции и гемодинамики. Чаще всего они возникают в результате перенесенного ревматизма, инфекционного эндокардита, системных заболеваний соединительной ткани, травмы, пролапса митрального клапана (ПМК).
Недостаточность митрального клапана у ребенка, детей
Недостаточность митрального (двустворчатого) клапана развивается при поражении его створок, а также подклапанного аппарата. Возникает как осложнение ревматизма, инфекционного эндокардита, системных заболеваний соединительной ткани, в результате травмы, ПМК, патологии клапанного аппарата: разрыва хорд, разрыва или дисфункции папиллярных мышц, дилатации митрального кольца или полости левого желудочка и др.
Жалоб дети могут не предъявлять. При длительно существующей недостаточности клапана может сформироваться выбухание левой половины грудной клетки — сердечный горб.
Митральный стеноз может быть первичным (при латентно или подостро текущем ревматизме) или вторичным, возникающим на фоне недостаточности митрального клапана. Врожденный митральный стеноз проявляется сердечной недостаточностью в грудном и раннем детском возрасте.
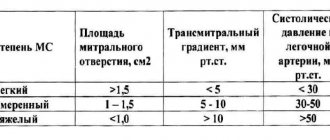
Давление в левом предсердии повышается, развивается его гипертрофия, ускоряется кровоток в левый желудочек из-за сужения митрального отверстия до 1-1,5 см2 (в норме площадь митрального отверстия 4-6 см2). Высок риск инфекционного эндокардита при любом поражении клапанов. При тяжелом митральном стенозе (площадь митрального отверстия <1 см2 давление в левом предсердии превышает 25 мм рт. ст., что приводит к легочной гипертензии и в покое. При развернутой клинической картине дети жалуются на одышку и быструю утомляемость (одышка при нагрузке возникает, когда площадь отверстия клапана уменьшается вдвое (< 2 см2). Мерцательная аритмия, инфекции и инфекционный эндокардит могут при тяжелом митральном стенозе вызвать отек легких.
Недостаточность аортального клапана у детей, ребенка
Чаще всего недостаточность аортального клапана возникает в результате деформации аортальных клапанов при ревматизме (почти всегда сочетается с поражением митрального клапана), вследствие инфекционного эндокардита, миксоматозной дегенерации клапанов, травмы, наследственных заболеваний соединительной ткани, врожденного двустворчатого клапана и др.
При недостаточности аортального клапана часть крови возвращается во время диастолы из аорты в левый желудочек, в результате чего мышечные волокна левого желудочка растягиваются и гипертрофируются.
Больные жалуются на одышку и сердцебиение, возникающие при физической нагрузке, нередко — на боли в области сердца. Кожные покровы бледные, нередко отмечается усиленная пульсация сонных артерий (пляска каротид). Пульс скорый и высокий, реже можно отметить появление капиллярного пульса.
Стеноз устья аорты у детей, ребенка
Чаще всего стеноз устья аорты возникает в результате деформации и развития фиброза и кальциноза двустворчатого аортального клапана, вследствие перенесенного ревматизма (почти всегда сочетается с поражением митрального клапана), изолированного кальциноза аортальных клапанов, инфекционного эндокардита с массивными вегетациями, травмы.
При стенозе устья аорты гемодинамика обусловлена сужением выходного тракта левого желудочка и увеличением нагрузки на левый желудочек (систолическая перегрузка). При легкой степени стеноза площадь отверстия аортального клапана равна 1,2-2 см2, при умеренном стенозе — 0,75-1,2 см2, при тяжелом стенозе <0,75 см2. 15-20 % больных при наличии симптомов стеноза аорты умирают внезапно.
Пролапс митрального клапана у детей, ребенка
Пролапс митрального клапана (ПМК) — это прогибание митральных створок в полость левого предсердия во время систолы левого желудочка. Этот синдром чаще связан с аномалией строения клапана, при которой одна из его створок (чаще задняя) или обе провисают в конце систолы в полость левого предсердия. ПМК может быть первичным (идиопатическим) и вторичным (в результате врожденных или приобретенных заболеваний).
Среди врожденных заболеваний ПМК чаще сочетается с наследственно обусловленными заболеваниями соединительной ткани (синдромы Марфана, Элерса-Данлоса, Холта-Орама и др.). У больных при этом часто наблюдаются астеническое телосложение, сколиоз, плоскостопие, вальгусная деформация стоп, расслабление связок. В возникновении ПМК определенную роль играет состояние подклапанного аппарата — удлинение или аномалии прикрепления хорд, форма створок клапана. ПМК возникает при патологических изменениях его створок и клапанных хорд, дисфункции папиллярных мышц, нарушениях сократимости левого желудочка при ревматизме, неревматическом кардите, бактериальном эндокардите, кардиомиопатиях, ВПС. ПМК часто сопутствует нейроциркуляторной дистонии и функциональной кардиопатии, при которых имеет место преобладание симпатического или парасимпатического отдела вегетативной нервной системы. В генезе его большую роль играет наследственная предрасположенность.
Дети с ПМК особых жалоб не предъявляют, поэтому болезнь обычно выявляется случайно. Иногда отмечаются боли в сердце, головокружение, обмороки (ээг ребенку — поликлиника «Маркушка»), что обусловлено вегетативными сдвигами, часто снижением АД.
Анализы и диагностика
В случае сужения кровевыталкивающих структур сердца или легочной артерии следует обратиться к врачу – кардиологу, который сможет оценить масштаб и характер патологических изменений. При обследовании у больных может быть выявлена:
- гипертрофия правого желудочка при пальпации;
- признаки систолической перегрузки правого желудочка на электрокардиограмме – отклонение электрической оси сердца вправо, смещение сегмент ST на 2-5 мм ниже изолинии и отрицательный глубокий зубец Т, хотя чаще полученные данные в пределах нормы;
- раздвоение второго тона сердца;
- жесткий шум выброса, щелчок и убывающий шум изгнания слышен во втором межреберном при клапанном стенозе или четвертом – при подклапанном стенозе легочного ствола у больных в позиции наклона вперед при использовании стетоскопа;
- шумы становятся более громкими при проведении пробы Вальсальвы и на вдохе, могут удлиняться и усиливаться при прогрессировании стеноза;
- на ЭКГ обычно выявляется гипертрофия стенок правого желудочка;
- при помощи допплерэхокардиографии можно выявить выраженное турбулентное течение крови на уровне легочного клапана и получить изображение сужения, установить тяжесть состояния больного и градиент давления – если он не превышает 35 мм рт ст, то повреждения считаются лёгкими, если в пределах 35-65 мм рт ст – умеренные, свыше 65 мм рт ст – тяжелыми.
Больным может понадобиться периодически проведение УЗИ сердца для отслеживания возможного прогрессирование стеноза (сужения).
Опрос и осмотр пациента
Следует выяснить были ли у пациента эпизоды тромбозов глубоких вен, внезапных отеков ног, тромбофлебиты. У многих больных прослеживается семейный анамнез внезапной смерти, сердечно-сосудистой патологии и повышенной наклонности к тромбообразованию.
Объективным доказательством перенесенной тромбоэмболии легочной артерии (ТЭЛА) становится совпадение по времени клиники тромбоза вен нижних конечностей и появления одышки. В ближайшие месяцы после ТЭЛА у больных можно выявить период, когда состояние остается стабильным и малосимптомным. Это связано с тем, что правый желудочек справляется с нагрузкой и позволяет сохранить хорошую переносимость физических нагрузок до момента развития прогрессирующего ремоделирования легочных сосудов. Практически единственным надежным доказательством перенесенной ТЭЛА могут стать данные перфузионной сцинтиграфии или компьютерной томографии легких, проведенной во время острого эпизода ТЭЛА.
При общем осмотре пациентов с ХТЭЛГ может определяться синюшность (цианоз). При развитии правожелудочковой сердечной недостаточности отмечаются набухшие шейные вены, увеличение печени, периферические отеки, водянка живота.
Стеноз легочной артерии у новорожденных
У новорожденных деток выраженная (критическая) форма стеноза вызывает сердечную недостаточность и синеватый оттенок кожных покровов, вызывает подозрение ярко-выраженный сердечный шум.
Градиент давления может со временем исчезнуть и быть компенсирован внутренними силами организма, однако состояние образовавшихся постстенотических аневризматических расширений мелких сосудов бывает осложнено тромбозом и артериитом, вызывать легочные кровотечения. Тяжелые стенозы могут приводить к летальному исходу, как в младенческом возрасте, так и в последующих периодах жизни.
Диета при стенозе легочной артерии
Диета 10-й стол
- Эффективность: лечебный эффект через 1 месяц
- Сроки: постоянно
- Стоимость продуктов: 1700-1850 руб. в неделю
Стеноз легочной артерии требует соблюдения особой диеты, чаще всего назначают номер 10 со значительным уменьшением содержания солей, обеспечивающая нормальную жизнедеятельность сердечно-сосудистой системы. Кроме этого, она щадит желудочную и мочевыделительную систему . Обычно отдается предпочтение таким продуктам:
- несдобный и цельнозерновой хлеб;
- различные виды диетических супов;
- обязательные овощные гарниры;
- яйца;
- фруктовые соусы и салаты;
- молокопродукты невысокой жирности.
Под запретом пряные, соленые, острые и копченые продукты, а также животные жиры. Напитки, в которых содержится кофеин и алкоголь. Рекомендовано ограничение жиров даже растительного происхождения.