Пульмонолог
Прохина
Мария Егоровна
Стаж 38 лет
Врач-пульмонолог
Записаться на прием
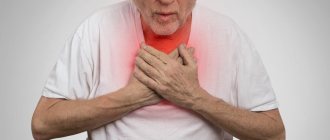
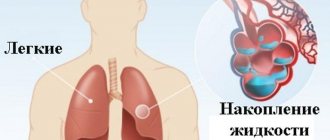
Отек легких – это патологическое, очень серьезное состояние, которое характеризуется выходом транссудата в легочную ткань. В результате нарушается газообмен, что приводит к серьезнейшим последствиям вплоть до летального исхода.
Неотложная помощь при отеке легких – единственное, что может повысить риски пациента на выживание и восстановление здоровья. Человеку в такой ситуации требуется немедленное участие врачей.
Сам по себе отек легких чаще всего является уже осложнением, которое сопутствует серьезным проблемам органов и систем организма, например, сердечно-сосудистой системы, ЖКТ и т.д.
Причины
На самом деле причин отека легких очень много – для разных заболеваний они свои. Назовем для примера несколько общих предпосылок:
- кардиосклероз после инфаркта, острый инфаркт миокарда;
- гипертония, аритмия;
- сердечная недостаточность;
- врожденные либо приобретенные пороки сердца;
- хронический бронхит, крупозная пневмония, бронхиальная астма;
- осложнения на фоне ОРВИ, кори, гриппа, скарлатины, коклюша и других болезней;
- недоношенность у новорожденных детей;
- серьезные проблемы с почками;
- черепно-мозговые травмы, операции на мозге и т.д.;
- вдыхание токсических веществ.
Эти и многие другие причины не являются непосредственными факторами, способствующими развитию отека легких. Но на фоне подобных состояний он может развиваться, что обязательно учитывается при госпитализации со всем вышеперечисленным.
Синдром Дресслера
Развивается данное осложнение на 2-6 неделе после инфаркта миокарда по причине некротического поражения тканей сердечной мышцы. Попавшие в кровь больного токсичные продукты распада вызывают аутоиммунную реакцию организма. Для синдрома Дресслера характерны следующие признаки:
- Острые или давящие боли в груди, часто они отдают в плечо или шею.
- Иногда отмечается повышение температурного фона.
- Пациент жалуется на сильную слабость.
- Могут появиться болезненные ощущения в области расположения легких.
- Возможен сухой кашель с кровью.
- На коже появляются высыпания.
- Отмечается онемение в левой руке.
- При визуальном осмотре – левая часть грудной клетки выглядит опухшей.
Протекать синдром Дресслера может по типу плеврита, перикардита или полиартрита. Это типичный для этого состояния вариант. Атипичная форма выражается в виде кардиоплечевого синдрома, на который указывает высокая температура и изменения в анализе крови.
Разновидности
Есть разные варианты отека легких:
- молниеносный. Он развивается крайне быстро, за несколько минут – исход в данном случае только летальный;
- острый. Симптомы нарастают в течение четырех часов, риск летального исхода очень высокий. Такой отек часто встречается при инфаркте, удушье, черепно-мозговых травмах;
- подострый. Развитие симптомов чередуется то активной, то более спокойной стадиями. Встречается при печеночной недостаточности;
- затяжной. Может развиваться в течение двенадцати часов, даже нескольких суток, и не иметь яркого проявления. Проявляет себя при сердечной недостаточности, а также хронических болезней легких.
Очевидно, что для каждого варианта требуются свои действия. Если пациента еще можно спасти, скорость реагирования тут будет ключевым фактором.
Причины, по которым развивается инфарктная пневмония
Выделяют следующие состояния, провоцирующих развитие тромбов:
- варикозное расширение вен;
- сердечная недостаточность правожелудочковая;
- пороки сердца;
- отрыв тромба или воспаление вены.
При наличии сопутствующих факторов, отягощающих течение основного заболевания, риск развития инфарктной пневмонии в разы увеличивается. Такими факторами выступают:
- венозная недостаточность в хронической форме;
- избыточный вес;
- прием эстрогенов;
- ослабление мышц;
- системные заболевания.
Но даже при таких состояниях тромбофлебит возникает не у каждого больного. Есть несколько причин, приводящих к такому состоянию:
- перелом трубчатой кости;
- мерцательная аритмия;
- долгое нахождение в лежачем положении, например, когда пациент находится в коме;
- плохое кровообращение.
В конечном счете, совокупность вышеперечисленных факторов приводит к отрыву небольших частей тромбов, которые в дальнейшем оседают в сосудах легких, что впоследствии приводит к закупорке артерии. Нарушение кровообращения в легком по причине сужения артерии приводит к инфаркту легкого.
В месте возникновения инфаркта может наблюдаться полное отсутствие поступления крови. При инфицировании такого участка различными бактериями и микроорганизмами наблюдается инфарктная пневмония.
Симптомы
Описывать симптомы отека легких можно только общими моментами, поскольку отдельные виды патологии протекают со смазанными характеристиками. К признакам относятся такие моменты:
- сильная слабость;
- поверхностное, очень частое дыхание;
- сухой кашель;
- сухие свистящие хрипы;
- выраженная одышка;
- одутловатость лица и шеи;
- клокочущее дыхание и влажные хрипы;
- пена изо рта с розовым оттенком;
- заторможенность, спутанность сознания;
- поверхностное дыхание;
- нитевидный пульс.
Некоторые признаки отека легких противоречат друг другу по той причине, что начинаться все может с одного состояния, а заканчиваться другим. Например, в течение нескольких минут или часов наблюдается учащенное дыхание, а затем оно ослабевает. При быстрых и наиболее опасных формах отека смерть пациента наступает от удушья (асфиксии).
У вас появились симптомы отека легких?
Точно диагностировать заболевание может только врач. Не откладывайте консультацию — позвоните по телефону
Диагностика
Если симптомы отека легких не выражены, параллельно с неотложной помощью требуются дополнительные исследования:
- биохимический скрининг. Это исследование показателей крови;
- изучение газов крови;
- ЭКГ, УЗИ сердца;
- рентгенография области грудной клетки;
- катетеризация легочной артерии.
Во многих случаях диагностика отека легких возможна сразу же – только по тем признакам, которые проявляются у больного визуально и без дополнительного обследования.
Лечение
Единой программы для лечения отека легких нет и не может быть. Экстренная помощь больному включает мероприятия по уменьшению венозного возврата к сердцу, подаче увлажненного кислорода. Нередко больного переводят на ИВЛ, может выполняться трахеостомия.
Также дополнительно вводятся разные препараты: анальгетики, диуретики, средства, снижающие давление в малом круге кровообращения, препараты для сердца, антибактериальные средства и многое другое. Далее лечение отека легких, если приступ снят, сводится к тому, чтобы лечить основное заболевание, вызвавшее эту патологию.
Прогнозы при отеке очень серьезные. В зависимости от причин отека легких, смертность может составлять от 20 до 90%. Чем раньше будет выявлена проблема, тем выше шансы на выздоровление. Но во многих случаях пациента может спасти только своевременное лечение тех заболеваний, которые способствуют возникновению патологии – такая профилактика отека легких, например, единственная возможность снизить риски молниеносной формы болезни, которая сама по себе уже смертельная и не поддается лечению.
Неинвазивная вентиляция легких при остром инфаркте миокарда
Острая сердечная недостаточность (ОСН) при инфаркте миокарда (ИМ) — неспособность сердца, как насоса, перекачивать необходимый объем крови (минутный объем сердца (МОС) л/мин), адекватный метаболическим нуждам организма (обеспечение основного обмена), которая манифестируется тяжелыми гемодинамическими расстройствами и нарушением газообменной функции легкого. Несостоятельность насосной способности сердца, вследствие ишемического повреждения миокарда левого желудочка, ведет к развитию гипоксемии — раннему и постоянному признаку недостаточности кровообращения, лежащей в основе клинических признаков ОСН. В основе гипоксемического синдрома по механизму снижения насыщения крови кислородом участвуют две составляющие гипоксемии — центральная (кардиогенная — застой крови в легком) и периферическая (циркуляторная — замедление периферического тканевого кровотока).
В зависимости от выраженности клинических проявлений, согласно предложенной классификации T. Killip, J. Kimball, выделяют 4 степени ОСН при ИМ:
I степень — отсутствие клинических проявлений сердечной недостаточности;
II степень — хрипы в легких при аускультации, выслушиваемые на площади менее 50% легочных полей, или наличие тахикардии в сочетании с III тоном при аускультации сердца — систолический ри;
III степень — хрипы в легких при аускультации более 50% легочных полей в сочетании с ри;
IV степень — отек легкого, клиника кардиогенного шока [1].
Стандартная медикаментозная терапия (СМТ) острого инфаркта миокарда (ОИМ), осложненного ОСН, достаточно хорошо разработана и регламентирована. Госпитальная летальность ИМ, осложненного ОСН, составляет 24%, в тяжелых случаях, с необходимостью проведения искусственной вентиляции легких (ИВЛ) с помощью интубации трахеи, по данным отечественных и зарубежных авторов, достигает 52% [2, 3, 4, 6, 7, 8, 9, 12].
В последних фундаментальных работах, включающих метаанализ большого количества исследований ОСН, показана высокая эффективность основных методов неинвазивной (масочной) искусственной вентиляции легких (НИВЛ) при лечении кардиогенного отека легких (КОЛ), рефрактерного к СМТ: постоянное положительное давление в дыхательных путях (СРАР — Continuous Positive Airway Pressure), поддержка повышенным давлением на вдохе (PSV — Pressure Support Ventilation), поддержка повышенным давлением в конце выдоха (PEEP — Positive End-Expiratory Pressure) [13, 15, 19].
Руководство Британского торакального общества рекомендует использовать СРАР у пациентов с сохраняющейся гипоксемией на фоне комплексного медикаментозного лечения ОСН и резервировать использование двухуровневой вентиляции — PSV + PEEP для пациентов, у которых СРАР не принес улучшения [5].
В настоящее время в медицинской литературе представлены единичные сообщения, посвященные применению НИВЛ при лечении КОЛ у пациентов с ОИМ [16, 17, 18]. В этих публикациях было документировано, что сочетание поддержки вдоха с положительным давлением в дыхательных путях в конце выдоха (PSV + PEEP) более эффективно для снижения работы дыхания и уменьшения респираторного дистресса, чем только СРАР [10, 11, 14].
Все вышеизложенное явилось целью настоящей работы — изучение эффективности различных методов НИВЛ у пациентов с ОИМ, осложненным ОСН III–IV степени, рефрактерной к проведению стандартной медикаментозной терапии.
Материалы и методы. В изучаемую группу входили 94 пациента с ОИМ, средний возраст которых составил 67,4 ± 5,5 года. Критериями включения были: крупноочаговый ОИМ, осложненный ОСН III–IV степени по классификации Killip–Kimball, дыхательной недостаточностью и периферической гипоксемией (частота дыхательных движений (ЧДД) в покое > 25 в мин, НвО2 — чрескожно < 90%), сохраняющимися в течение 1 часа на фоне проводимой СМТ.
СМТ включало: кислород через носовые канюли или лицевую маску, дезагреганты и антикоагулянты, петлевые диуретики, нитроглицерин, ингибиторы АПФ, бета-блокаторы; пациентам с ОСН IV степени дополнительно назначали катехоламины.
С целью объективизации эффективности проводимого лечения, всем пациентам проводилось зондирование правых отделов сердца с измерением среднего давления в правом предсердии (ПП), систолического и диастолического давления в правом желудочке (СДПЖ, ДДПЖ), систолического и диастолического давления в легочной артерии (СДЛА, ДДЛА), давления заклинивания легочной артерии (ДЗЛА), с расчетом сердечного (СИ) и ударного индексов (УИ), индекса ударной работы левого и правого желудочка (ИУРЛЖ, ИУРПЖ), общего периферического сосудистого сопротивления (ОПСС), общего легочного сопротивления (ОЛС). До и после 60 мин НИВЛ проводился забор проб крови из легочной и периферической артерии с определением кислотно-щелочного состояния крови (КЩС), концентрации гемоглобина (Нв), напряжения кислорода и углекислого газа (рО2, рСО2), насыщения Нв кислородом (НвО2) и расчетом индекса доставки кислорода (ИДО2), индекса потребления кислорода (ИПО2), процента шунтирования крови в легких (Qs/Qt). НИВЛ проводили на аппарате РВ-7200 (USA) атмосферным воздухом (FiO2 — 21%) в трех режимах: СРАР, PSV и PSV + PEEP. В 85% случаях использовалась лицевая маска, а в 15% — назальная.
В зависимости от проводимого режима НИВЛ больные с ОИМ, осложненным ОСН, были распределены на три группы: группа А-1 масочная CPAP — 19 пациентов (11 мужчин, 8 женщин), средний возраст по группе — 59,7 ± 10,8 года; группа А-2 с режимом вентиляции PSV — 27 пациентов (24 мужчины и 3 женщины), средний возраст составил 68,3 ± 10,9 года; группа А-3 сочетанный режим вентиляции PSV + PEEP — 48 пациентов (34 мужчины и 14 женщин), средний возраст по группе — 60,7 ± 12,5 года. По возрасту пациенты групп А-1, А-2 и А-3 были сопоставимы и статистически не отличались друг от друга (р > 0,05).
В группе А-1 течение ОИМ осложнилось ОСН III степени у 15 пациентов, ОСН IV степени — у 4. В группе А-2 ОСН III степени регистрировалась у 22 пациентов, СН IV степени — у 5. В группе А-3 ОСН III степени отмечалась у 38 пациентов, СН IV степени — у 10. При режиме искусственной вентиляции PSV давление на вдохе в среднем составило 17,0 ± 5,9 см Н2О; при PEEP давление на выдохе в среднем составляло 5,4 ± 1,4 см Н2О; среднее инспираторное давление PSV + PEEP — 17,6 см Н2О.
Дозы и темп введения препаратов СМТ у всех пациентов до и во время НИВЛ были практически одинаковы (р > 0,05). При сравнении исходных показателей гемодинамики и газообмена между группами А-1, А-2 и А-3 не было отмечено достоверных различий (р > 0,05).
Статистическая обработка проводилась с использованием прикладного рабочего пакета статистического анализа Statistica v.6.0, использовались параметрические и непараметрические критерии достоверности.
Результаты лечения и их обсуждение. Динамика показателей центральной гемодинамики и газового состава крови у пациентов ОИМ с ОСН под влиянием различных режимов вспомогательной вентиляции при спонтанном дыхании (группы А-1, А-II, А-III) представлены в
,
,
.
Респираторная поддержка в режиме СРАР от 5,0 до 13 см Н2О приводила к клиническому улучшению у 93% пациентов, что выражалось в уменьшении возбуждения пациентов, снижении тахикардии и одышки, улучшении периферического кровообращения (изменении в положительную сторону цвета, температуры и влажности кожных покровов), при этом существенно уменьшались или полностью исчезали влажные застойные хрипы в легких. Положительная клиническая динамика сопровождалась статистически достоверными снижением преднагрузки (ДЗЛА мм рт. ст.) на 25% и постнагрузки (ОПСС) на 13,5% для левого желудочка на фоне уменьшения частоты сердечных сокращений (ЧСС) на 10,3%, ростом насосной функции левого желудочка (ИУРЛЖ) на 8,3%, снижением индекса работы правого желудочка на 13,3%.
Снижение ДЗЛА косвенно свидетельствовало о разгрузке малого круга кровообращения, что привело к достоверным положительным изменениям показателей газообмена: увеличению оксигенации артериальной (НвО2а, %) на 5,6% и смешанной венозной крови (НвО2ла, %) на 11,2% с статистически достоверным уменьшением шунтирования крови в легких на 43%. Уменьшение процента шунтирования крови в легких, с улучшением оксигенации артериальной крови, сопровождалось достоверным ростом доставки кислорода к исполнительным органам и тканям: ИДО2 увеличился на 6% (р < 0,0005) с достоверным снижением ИПО2 на 12,2% (р < 0,01), что связано с уменьшением работы дыхательной мускулатуры на фоне снижения ЧДД на 23,1%.
Таким образом, суммарно респираторная поддержка в виде СРАР со средним давлением 9,0 ± 0,3 см водного столба приводила к достоверному снижению ЧДД, ЧСС, гидростатического легочного капиллярного давления, шунтирования крови в легких, постнагрузки для левого желудочка и сопровождалась ростом оксигенации артериальной и венозной крови, ударного индекса и доставки кислорода к исполнительным органам и тканям.
Респираторная поддержка с помощью PSV также приводила к быстрому клиническому улучшению и стабилизации состояния пациентов в 91% случаев. Данные гемодинамики и газообмена представлены в .
Поддержка давлением на вдохе приводила к достоверному снижению гидростатического давления в легочном капилляре (ДЗЛА), систолического давления в легочной артерии и правом желудочке соответственно на 19,2%, 20% и 25%, что сопровождалось уменьшением работы правого желудочка на 16,2% и восстановлением эффективности работы левого желудочка сердца на 17,5%. Суммарно эти изменения способствовали достоверному снижению ЧСС на 7,4%.
Респираторная поддержка давлением на вдохе у пациентов группы А-2 приводила к эффективному улучшению показателей газообмена: уменьшению шунтирования крови в легких на 35,1%, восстановлению оксигенирующей функции легкого — нарастанию содержания кислорода в артериальной крови на 4,5%, увеличению доставки кислорода на 12,9% и уменьшению индекса потребления О2 на 7,2%. Статистически достоверное снижение ЧСС на 13,3% косвенно свидетельствует об улучшении газообменной функции легкого, подтверждаемом снижением РСО2 в артериальной крови на 5,6%. В свою очередь, уменьшение ЧДД способствует снижению энергозатрат на работу дыхательной мускулатуры, приводящему к уменьшению ИПО2.
Респираторная поддержка в режиме PSV + PEEP у пациентов группы А-3 также приводила к быстрому клиническому улучшению и стабилизации состояния в 92% случаях наблюдения. Положительная клиническая динамика подтверждалась объективными данными, представленными в .
Из таблицы видно, что НИВЛ в режиме PSV + PEEP сопровождалась достоверным уменьшением ЧСС на 14,2%, снижением гидростатического легочного капиллярного давления на 26%, при увеличении показателя работы левого желудочка на 14,4%, и повышением давления в правом предсердии на 83,3%. Увеличение давления в правом предсердии (показатель центрального венозного давления) обусловлено увеличением внутригрудного давления за счет повышенного давления на вдохе и выдохе дыхательного цикла НИВЛ (в среднем на 17,6 см Н2О), что сопровождается повышением сопротивления притоку крови к правому желудочку. Показатели артериального давления, сопротивлений большого и малого кругов кровообращения, давлений и работы правого желудочка достоверно не изменялись.
Из таблицы следует, что НИВЛ в режиме PSV + PEEP приводила к быстрому уменьшению одышки (ЧДД уменьшилось на 30%), улучшению показателей оксигенации артериальной и смешанной венозной крови соответственно на 6% и 9,8%, снижению степени шунтирования венозной крови в легких на 31,8% и увеличению доставки кислорода к исполнительным органам и тканям на 4%. Улучшение газообменной функции легкого документируется снижением рСО2 в артериальной крови на 7,8%.
При ретроспективном анализе (за один год) историй болезней больных ОИМ, осложненным ОСН, которым проводилась стандартная искусственная вентиляция легкого с помощью интубации трахеи, госпитальная летальность составила 39,6%. В наших исследованиях, в целом по группе больных ОИМ, осложненным ОСН, которым проводилась НИВЛ в различных режимах, госпитальная летальность составила 25,5% (24 пациента).
Заключение
При инфаркте миокарда имеет место нарушение сократительного состояния сердечной мышцы, ведущее к снижению насосной деятельности сердца и, как следствие, к повышению конечно-диастолического давления, в частности, в полости левого желудочка. Физиологически значимое увеличение конечно-диастолического давления левого желудочка или давления в левом предсердии неизменно приводит к ретроградному увеличению давления в сосудах легких и формирует посткапиллярную, пассивную легочную гипертензию. В соответствии с уравнением Старлинга, при повышении гидростатического давления в малом круге кровообращения происходит увеличение скорости фильтрации жидкости через микрососудистый эндотелий в легочном интерстиции. Когда жидкость фильтруется быстрее, чем удаляется лимфатической системой, происходит развитие периваскулярного, интерстициального, а затем и альвеолярного отека легких.
На первом этапе компенсации при повышении интерстициального давления происходит стимуляция J-рецепторов с увеличением объема вентиляции, что способствует увеличению оттока лимфы и, как следствие, минимизирует риск прогрессирующего внутритканевого отека и последующего альвеолярного наводнения.
С механической точки зрения, задержку жидкости в малом круге кровообращения можно представить как рестриктивные расстройства, проявляющиеся изменением легочных объемов, уменьшением эластических свойств легочной ткани за счет отека интерстиция, наводнения альвеол — функциональных единиц, что суммарно ведет к снижению газообменной функции легкого.
Гемодинамический фактор — повышение давления в венозном русле малого круга кровообращения при ОИМ — сопровождается гетерогенными нарушениями вентиляции легкого, носящими ретстриктивный (снижение эластичности легочной ткани) и обструктивный (повышение сопротивления дыхательных путей за счет отечности и спазма бронхов) характеры.
Прогрессивное уменьшение емкости легкого и его растяжимости приводят к росту отрицательного давления в плевральной полости, необходимого для осуществления вдоха; следовательно, к нарастанию «работы дыхания», увеличивая долю от минутного объема сердца, необходимую для энергетического обеспечения механики дыхания.
Все вышеперечисленные изменения ведут к нарушениям вентиляционно-перфузионных соотношений, лежащих в основе кардиогенно-дыхательной гипоксемии, которые усугубляются появлением дополнительных внутрилегочных шунтов кровотока, по объему достигающих более 10% от МОС.
У больных ОИМ, осложненным острой левожелудочковой недостаточностью, «работа дыхания» повышена из-за снижения растяжимости легочной ткани и повышения сопротивления дыхательных путей (интерстициальный и бронхиальный отеки), энергетические затраты на работу дыхания в условиях сниженного СИ достигают 30% от сердечного выброса. Следовательно, снизив энергетические затраты на работу дыхания с помощью НИВЛ, можно уменьшить долю СИ, направленную к дыхательной мускулатуре, перераспределив ее к другим отделам сердечно-сосудистой системы.
НИВЛ при спонтанном дыхании пациента с повышенным давлением в различных режимах (CPAP, PSV PEEP), помимо снижения работы дыхания, способствует «выдавливанию» жидкой части крови из альвеол и интерстиции легочной ткани в кровеносное русло, что обеспечивает более эффективный газообмен и нивелирует отрицательный эффект шунта в легком.
Таким образом, респираторная поддержка в различных режимах — СРАР, PSV и PSV + PEEP — оказалась эффективным методом лечения КОЛ, рефрактерного к стандартной медикаментозной терапии, у пациентов с ОИМ. На фоне НИВЛ наблюдалось клиническое улучшение и положительные изменения показателей не только гемодинамики, но и газообмена. Эффективность различных методик НИВЛ и характер их воздействия на такие показатели, как ЧДД, ЧСС, ПП, СДЛА, ДЗЛА, ИДО2, рО2а, рО2ла и Qs/Qt, оказались сходными. Отличие отмечено при использовании PSV и PSV + PEEP в степени влияния на рост ИУРЛЖ и снижение напряжения СО2 в артериальной крови.
Можно предполагать, что режимы респираторной поддержки с использованием PSV и PSV + PEEP будут более эффективны у пациентов с ОИМ, осложненным ОСН с сопутствующей гиповентиляцией и гиперкапнией.
Хотя оба метода — PSV и СРАР — демонстрируют сходную эффективность, с практической точки зрения СРАР дешевле и доступнее при применении в клинической практике, поэтому именно СРАР можно считать предпочтительным методом у пациентов, переносящих ОИМ с кардиогенным отеком легкого.
По вопросам литературы обращайтесь в редакцию.
А. М. Шилов, доктор медицинских наук, профессор С. П. Грачев, кандидат медицинских наук, доцент ММА им. И. М. Сеченова, Москва
Вопросы-ответы
Из-за чего происходит отек легких?
Факторов, которые способствуют развитию этой патологии, десятки. Они связаны с другими заболеваниями разных систем организма. Клинические рекомендации при отеке легких во многом обуславливаются ситуацией.
Может ли отек легких привести к смерти?
Да, риск летального исхода в случае такой патологии очень высок, а для молниеносной формы он является единственным возможным исходом событий. Это крайне опасное состояние, требующее немедленной профессиональной помощи.
Как лечить отек легких?
Это делают исключительно в медицинских учреждениях, чаще всего в реанимации. Все, что нужно знать про симптомы и лечение отека легких у взрослых либо детей, знают только врачи – патологию невозможно устранить без специальных знаний и навыков.
В чем особенности отека легких у детей?
В отличие от взрослых, у детей эта патология возникает намного реже по причине других болезней. Обычно в основе лежит аллергия или контакт с токсинами. Либо же причиной могут стать врожденные аномалии разных систем организма.
Постинфарктная стенокардия
Приступы сердечных болей чаще проявляются в первые сутки и на протяжении 14 дней после инфаркта. Как показывает статистика, практически каждый четвертый пациент испытывает после инфаркта такие приступы. Они выражаются в сильнейших болях за грудиной. Болезненные ощущения могут распространяться на лопаточную область, нижнюю челюсть, левую руку.
Иногда боли бывают настолько сильными, что купировать их удается только с помощью медикаментозных средств. Приступ стенокардии может спровоцировать даже малейшая физическая нагрузка, не исключается развитие такой симптоматики в состоянии покоя. На фоне ухудшения состояния пациента отмечается повышение либо понижение артериального давления. В редких случаях приступ не сопровождается болью, но тогда отмечается нарушение сердечного ритма. Постинфарктная стенокардия опасна тем, что приступ может спровоцировать рецидив инфаркта миокарда.