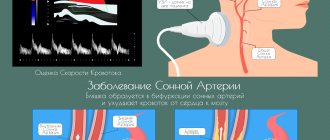
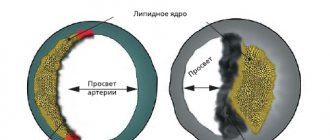
Оставлять без внимания проблему не следует, потому как рассматриваемое вещество считается очень важным электролитом, присутствующим в клетках мышц, работающим вместе с натрием. Именно калий обеспечивает должное сокращение мышц, а его нехватка может приводить к частым судорогам, снижению силового потенциала, дегидратации тканей. Препараты калия представлены достаточно большим количеством для выбора, поэтому особое внимание следует уделить определению наиболее подходящего средства. Здесь нужно учитывать состав, количество и массовую долю компонентов, чтобы достичь максимального эффекта. Калий может быть представлен в виде самостоятельного препарата, а также входить в состав различных препаратов, необходимых для регидратации.
ЗНАЧЕНИЕ КАЛИЯ ДЛЯ ССС
Рассмотрим подробнее влияние калия на работу сердца. Электрическая активность клеток миокарда зависит от трансмембранных ионных градиентов, а также от время- и потенциалзависимых нарушений проведения ионных токов. Электролитные нарушения могут вызывать или облегчать развитие клинически значимых аритмий даже в условиях нормальной сердечной ткани путем модуляции проведения ионов через специфические ионные каналы миокарда. Ток Na+ в клетку при активации Na+-каналов формирует в кардиомиоцитах фазу быстрой деполяризации. По мере нарастания деполяризации проницаемость для Na+ падает вследствие инактивации Na+-каналов, но открываются каналы входящих токов Са++, которые необходимы для формирования фазы плато. Последующая активация калиевых каналов приводит к реполяризации мембраны кардиомиоцитов до уровня ПП. Калий, особенно внеклеточный, – самый важный фактор, определяющий ПП мембраны. Электрофизиологические эффекты калия зависят не только от его внеклеточной концентрации, но и от направленности (гипо- или гиперкалиемия) и скорости ее изменения. Первостепенное значение для регуляции трансмембранного градиента калия имеют калиевые ионные каналы. Калиевые каналы представляют собой трансмембранные белки, избирательно пропускающие ионы калия: калий движется под влиянием электрохимического градиента со скоростью от 106 до 108 ионов в секунду [1]. Существуют потенциалзависимые калиевые каналы и многочисленные каналы, открываемые для ионов калия или блокируемые различными веществами – лигандами соответствующих рецепторов. Такие каналы поддерживают фоновую проводимость мембран для ионов калия и формируют ПП возбудимых и невозбудимых клеток*. Гипокалиемия (<3 ммоль/л) снижает проницаемость мембран для калия [24]. Так, проводимость для входящего (аномального) калиевого тока выпрямления пропорциональна корню квадратному из величины внеклеточной концентрации калия [20, 21]. Зависимость активации задержанного (выходящего) тока выпрямления от внеклеточной концентрации калия помогает понять, почему длительность ПД меньше при высокой концентрации калия и больше – при низкой [31]. Но эффекты калия в отношении ПП мембраны модулируются и одновременно создаваемыми концентрациями Са++. Их взаимодействие таково, что повышенный уровень Cа++ снижает деполяризующий эффект, вызываемый повышенным уровнем калия. В свою очередь, низкий уровень Са++ ослабляет деполяризацию, вызываемую гипокалиемией.
Факторы, стимулирующие трансмембранное перемещение калия:
- из клетки во внеклеточное пространство:
– ацидоз; – стимуляция α-адренорецепторов; – препараты дигиталиса;
- из внеклеточного пространства в клетку:
– алкалоз; – стимуляция β2-адренорецепторов; – инсулин.
Повреждение фосфолипидов мембраны в процессах перекисного окисления липидов (ПОЛ) также приводит к нарушению барьерной функции мембраны и увеличению потерь калия клеткой. Активация ПОЛ происходит при таких патологических состояниях, как дистрофия, воспаление, ишемия миокарда и др.
Как сохранить калий в продуктах
Калий принадлежит к минералам, обладающим относительной стабильностью при хранении свежих продуктов. Незначительные изменения концентрации вещества возможны после длительного хранения пищи. Меж тем, не надо принимать никаких дополнительных мер, дабы «удержать» калий, например, в свежих овощах. А вот при контакте с водой, минерал почти полностью переходит в нее. Сохранить максимальное содержание после термообработки, позволят традиционные правила приготовления блюд: минимум времени на варку и как можно меньше воды. Например, овощи опускать в уже кипящую воду или вместо варки прибегнуть к запеканию.
ЭЛЕКТРОФИЗИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ГИПОКАЛИЕМИИ
Гипокалиемия ведет к увеличению (большему электроотрицательному значению) ПП мембраны и по меньшей мере в период электрической диастолы снижает возбудимость мембран из-за увеличения разницы между ПП и пороговым потенциалом. Предполагается, что внеклеточный калий необходим для открытия каналов задержанного тока выпрямления [31]. Низкий уровень внеклеточного калия снижает задержанный (выходящий) ток калия, приводя к увеличению длительности ПД и замедлению реполяризации. Наиболее важным здесь является нарушение конфигурации ПД, особенно замедление «склона» 3-й фазы реполяризации. Формируется ПД с длинным «хвостом», что приводит к увеличению относительного рефрактерного периода (ОРП) и уменьшению разницы между ПП и пороговым потенциалом в конечную фазу ПД. Поэтому миокард демонстрирует повышенную возбудимость и связанную с этим склонность к эктопической активности в течение значительной части ПД. Проводимость замедляется, поскольку деполяризация начинается в неполностью реполяризованных волокнах. Более того, гипокалиемия приводит к удлинению фазы плато в волокнах Пуркинье, но укорачивает ее в вентрикулярных волокнах [10]. Фаза реполяризации («хвост») ПД в проводящей системе пролонгируется больше, чем в желудочках, что повышает разброс реполяризации. Гипокалиемия ускоряет диастолическую деполяризацию в волокнах Пуркинье, тем самым повышая автоматизм. Суммарно электрофизиологические эффекты гипокалиемии проявляются в снижении скорости проведения, укорочении эффективного рефрактерного периода (ЭРП), удлинении ОРП, повышении автоматизма и ранней постдеполяризации.
ЭКГ-проявления гипокалиемии:
- вследствие изменений реполяризации:
– снижение амплитуды и расширение зубца Т; – заметная волна U; – снижение сегмента ST; – слияние зубцов Т и U (при тяжелой гипокалиемии);
- вследствие нарушений проводимости:
– увеличение длительности комплекса QRS; – атриовентрикулярная блокада; – увеличение амплитуды и расширение зубца Р; – небольшое увеличение интервала P–R; – остановка сердца.
Когда волна U превышает зубец T по амплитуде, уровень калия в плазме составляет <3 ммоль/л (см. рисунок).
Форма выпуска
Таблетки по 500 мг.
По 10 таблеток в контурную безъячейковую упаковку из бумаги с полимерным покрытием или из материала комбинированного пленочного цефлена.
По 10 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой печатной лакированной.
По 30, 40 или 50 таблеток в банки полимерные или во флаконы полимерные. Каждую банку, флакон, или 1, 2, 3, 4 или 5 контурных ячейковых упаковок или контурных безъячейковых упаковок вместе с инструкцией по применению помешают в пачку из картона.
АРИТМОГЕННЫЙ ПОТЕНЦИАЛ И КЛИНИЧЕСКИЕ ПОСЛЕДСТВИЯ ГИПОКАЛИЕМИИ
Вызванное гипокалиемией повышение возбудимости клинически проявляется развитием суправентрикулярной и желудочковой экстрасистолии. Показано, что снижение уровня калия и магния коррелирует с повышением частоты преждевременных желудочковых комплексов [30]. Гипокалиемия способствует развитию феномена reentry (повторного входа) через замедление проводимости на фоне удлинения ОРП, что приводит к повышению разброса рефрактерности. Супрессивное влияние гипокалиемии на работу Na+-K+-насоса ведет к избыточному накоплению Ca++ в клетке, что способствует развитию замедленной постдеполяризации через транзиентный входящий ток. В эксперименте гипокалиемия повышала склонность к фибрилляции желудочков как в нормальном, так и в ишемизированном миокарде [12]. Установлена связь гипокалиемии с фибрилляцией желудочков у пациентов с острым инфарктом миокарда [7, 18]. Гипокалиемия способствует повышению связывания сердечных гликозидов с Na+-K+-аденозинтрифосфатазой (АТФазой), уменьшению скорости элиминации дигоксина и потенцирует токсические эффекты препаратов дигиталиса. Применяя препараты калия, необходимо помнить об одном важном феномене – эффекте Звардемакера–Либрехта (Zwaardemaker–Libbrecht), который развивается в результате быстрого повышения уровня внеклеточного калия от низкого к высокому и проявляет себя кратковременной остановкой пейсмейкерных клеток, уменьшением длительности ПД и гипреполяризацией [13]. Этот феномен подчеркивает тот факт, что скорость внутривенного введения калия с точки зрения аритмогенного действия важнее, чем абсолютное количество введенного калия и конечный уровень внеклеточного калия.
МАГНИЙ
Ионизированный магний стоит на 2-м месте после калия по общему содержанию в клетке. Содержание магния в плазме крови – 0,8–1,5 ммоль/л, в мышечной ткани его содержание в 10 раз больше, чем в плазме. Благодаря такому депо магния в мышцах его уровень в крови может долгое время оставаться стабильным даже при значительных потерях. Значимость нарушений обмена магния до сих пор дебатируется из-за трудностей его измерения и обычной связи этих нарушений с другими электролитными расстройствами [14, 27]. Магний участвует в работе мышц и нервной системы, в регуляции сердечного ритма, обмена холестерина, липидов, фосфора и кальция. Он служит важным кофактором для многочисленных ферментативных реакций, участвующих в обмене нуклеотидов и углеводов, синтезе белков и других процессах, также необходимых для нормальной физиологии ССС. Магний предупреждает повышение АД, усиливает процессы торможения в ЦНС, вызывая седативный, транквилизирующий эффекты и препятствуя проявлениям судорожной активности. Являясь естественным антагонистом Ca++, магний снижает свертываемость крови и тонус сосудов [2, 4]. Суточная потребность взрослого человека в магнии – от 300 до 500 мг. Дефицит магния развивается часто, но его электрофизиологические последствия для миокарда ускользают от ученых даже при самом тщательном исследовании. Известно, что применение препаратов магния (магнезии) в фармакологических дозах полезно для лечения пируэтных тахикардий. Токсические эффекты магнезии наблюдаются редко (исключение – пациенты с нарушениями функций почек). При дефиците магния развиваются нервозность, раздражительность, нарушения сна на фоне мышечной слабости, повышенной утомляемости и парестезий. При хроническом дефиците магния возможны деформации скелета: сколиоз, воронкообразная грудная клетка, плоскостопие.
Способ применения и дозы
Следует принимать внутрь за 1 час до еды или через 4 часа после еды. Взрослым по 250-500 мг 2-3 раза в сутки. Курс лечения длится в среднем 20-30 дней. При необходимости лечение можно повторить через 1 месяц. В исключительных случаях можно увеличить дозу взрослых до 3 г в сутки. Детям — по 10-20 мг/кг массы тела в сутки, разделенные на 3-4 приема (например, если масса тела ребенка 25 кг, то разрешенная доза — от 25 х 10 = 250 мг (1/2табл.) до 25 х 20 = 500 мг (1 табл. в сутки, разделенные на 3-4 приема). Курс лечения 3-5 недель. При сохранении симптомов болезни проконсультируйтесь с врачом
ЭЛЕКТРОФИЗИОЛОГИЧЕСКИЕ ЭФФЕКТЫ И ЭКГ-ПРОЯВЛЕНИЯ ГИПОМАГНИЕМИИ
При очень низких внеклеточных концентрациях кальция магнезия оказывает влияние на трансмембранный ток или токи, которые модулируют длительность фазы плато ПД в желудочках. Установлено, что при нормальных концентрациях кальция дефицит магния имеет незначительное влияние на ПД папиллярной мышцы сердца собак [11]. Однако когда концентрация кальция снижается до 1/10 нормы, полное удаление магния из перфузионного раствора пролонгирует фазу плато ПД, которая уже была удлинена из-за низкой концентрации кальция, от нормальных значений (100–150 мс) до 1000 мс и более. Магний блокирует кальциевые каналы, смещает кривую инактивации быстрых натриевых каналов в направлении гиперполяризации, изменяет эффекты гиперкалиемии и оказывает модулирующее влияние на калиевые токи. В исследовании у здоровых пациентов были отмечены следующие ЭКГ-эффекты внутривенного введения магнезии: значимое удлинение интервала P–R; удлинение интервала проведения от предсердий к пучку Гиса; увеличение времени синоатриального проведения; удлинение ЭРП в атриовентрикулярном узле [16]. Гипермагниемия снижает атриовентрикулярную и внутрижелудочковую проводимость. Ни гипермагниемия, ни гипомагниемия не вызывают каких-либо специфических изменений ЭКГ. Внутривенное введение сульфата магнезии пациентам с увеличенным интервалом Q–T и пируэтной тахикардией, если исходный уровень магния был нормальным или низким, может купировать желудочковую тахикардию. О. Takanaka и соавт. [28] изучали действие магнезии и лидокаина на длительность ПД и индуцированную барием раннюю постдеполяризацию в волокнах Пуркинье собак. Полученные ими данные подтверждают, что гипомагниемия может иметь аритмогенное действие, когда сочетается с гипокалиемией и брадикардией; в этих условиях введение магнезии может подавить триггерную активность, главным образом прямо предупреждая развитие триггерных ПД. Не отмечено специфических электрофизиологических эффектов или аритмий, связанных с изолированным дефицитом магния. Тем не менее магний может повлиять на развитие сердечных аритмий через прямое воздействие или путем модулирования эффектов калия, или действуя в качестве блокатора кальциевых каналов. Известно, что дефицит магния оказывает негативное влияние на нормальное функционирование мембранной АТФазы, замедляя перенос натрия из клетки и калия в клетку. Это нарушает трансмембранное равновесие калия и может приводить к изменению ПП мембраны, изменению трансмембранной проводимости калия и нарушениям фазы реполяризации [9]. Приводятся данные о том, что потребление магния с пищей может иметь умеренную обратную корреляцию с риском развития ИБС, в частности, у мужчин [5].
Симптомы дефицита и избытка в организме
При недостатке калия человек быстро утомляется, постоянно чувствует усталость. У детей может наблюдаться беспричинная плаксивость. Дефицит макроэлемента также проявляется в виде следующих симптомов:
- выпадение волос;
- сухость и шелушение кожного покрова;
- гипертония;
- слабость мышц;
- частые позывы к мочеиспусканию;
- сбои сердечного ритма;
- судороги конечностей, особенно часто наблюдающиеся в ночное время;
- сонливость.
Избыточное поступление калия в организм или его накопление, вызванное различными заболеваниями, может привести к гиперкалиемии. Выявить эту патологию можно по следующим симптомам:
- учащенное сердцебиение, в тяжелых случаях работа сердечной мышцы останавливается;
- онемение конечностей;
- слабость в мышцах;
- головокружение;
- временный паралич;
- проблемы с пищеварением, боли в области желудка.
Чтобы избежать негативных последствий, при приеме высоких доз калия рекомендуется периодически контролировать содержание этого макроэлемента в крови с помощью своевременных анализов.
ПРИМЕНЕНИЕ ПРЕПАРАТОВ КАЛИЯ И МАГНИЯ В КЛИНИЧЕСКОЙ ПРАКТИКЕ
Кратко резюмируя изложенное, необходимо сказать, что калий и магний играют важную роль в регуляции функций ССС и ЦНС, обеспечивают нормальное течение многочисленных обменных биохимических процессов практически во всех тканях и органах, регулируют нервно-мышечную передачу, положительно влияют на фосфорно-кальциевый обмен и поддерживают электролитный баланс в организме. Поэтому препараты этих макроэлементов могут и должны применяться по очень широкому кругу показаний – как в лечении разнообразных патологических состояний, так и с профилактической целью, в первую очередь – для предупреждения гипокалиемии и гипомагниемии у пациентов, принимающих мочегонные средства (тиазидные и, особенно, петлевые диуретики) и (или) сердечные гликозиды (препараты дигиталиса). В практической медицине используются препараты, содержащие один из этих элементов – калий (калия хлорид, калия оротат) или магний (Магне В6, магнерот, магнезии сульфат), а также комплексные препараты, содержащие оба катиона (аспарагинат калия + аспарагинат магния: Панангин, аспаркам, калия и магния аспарагинат БерлинХеми). В этом ряду одним из наиболее эффективных и сбалансированных по составу препаратов аспарагината калия и магния, солидный опыт успешного применения которого накоплен отечественной и мировой медицинской практикой, является Панангин. Сочетанное назначение солей калия и магния дает преимущество потенцирующего эффекта их взаимодействия. Такое сочетание тем более оправдано, что метаболизм калия и магния тесно связан и клинически значимая гипомагниемия обычно развивается на фоне гипокалиемии или осложняет уже имеющуюся гипокалиемию. Входящая в состав Панангина аспарагиновая кислота, являясь естественной аминокислотой, легко проникает в клетку и облегчает поступление в нее калия и магния. Она полезна еще и тем, что входит в состав многих белков, играет важную роль в обмене азотистых веществ, участвует в реакциях переаминирования и в образовании пиримидиновых оснований нуклеиновых кислот. Несмотря на реальные достижения медицинской науки в распознавании этиопатогенеза ССЗ, распространенность их неуклонно растет, они остаются ведущей причиной инвалидизации и смертности населения как в России, так и во всем мире. Поэтому наиболее актуальными показаниями к применению Панангина остаются такие заболевания, как хроническая сердечная недостаточность, ИБС, в том числе инфаркт миокарда, сердечные аритмии, особенно связанные с приемом препаратов дигиталиса, и их сочетания. Панангин является препаратом выбора в профилактике и восполнении дефицита калия и магния и в других клинических ситуациях. В перспективе показания к назначению Панангина будут расширяться. Накапливаются сведения о пользе применения калия и магния для лечения и профилактики нарушений мозгового кровообращения и гипертонической болезни. Так, замена обычной поваренной соли солью, обогащенной калием и магнием, у лиц с нормальным или умеренно повышенным АД привела к значимому снижению потребления натрия и снижению систолического АД [22]. В исследовании А. Ascherio и соавт., в которое были включены более 43 тыс. мужчин в возрасте от 40 до 75 лет, был обнаружен достоверно меньший относительный риск инсульта (0,62) у лиц с высоким потреблением калия (в среднем – 4,3 г/сут), чем у лиц с низким его потреблением (в среднем – 2,4 г/сут) [6]. Выявлена также обратная корреляция потребления магния (но не кальция) с относительным риском развития инсульта. Все указанные корреляции были сильнее выражены у мужчин с артериальной гипертензией, чем у нормотензивных лиц. Авторы заключили, что дополнительный прием препаратов калия может более широко использоваться у пациентов с артериальной гипертензией. Однако эти сведения не могут обосновать огульное назначение препаратов калия всем без разбора, поскольку их бесконтрольный прием может быть опасен. Сообщалось, что потребление магния с питьевой водой статистически значимо предупреждает вероятность смерти от цереброваскулярных заболеваний [32]. Как показало одно из проспективных исследований, повышение потребления калия на 10 ммоль/сут сопровождалось достоверным снижением риска смерти от инсульта на 40% [15]. Этот эффект не зависел от других факторов риска или переменных, включая потребление магния. Недавний метаанализ проспективных исследований обнаружил статистически значимую обратную корреляцию между потреблением калия и риском инсульта, особенно ишемического [17]. При повышении потребления калия на каждые 1000 мг риск инсульта снижался на 11%. Практически одновременно с этой работой в журнале американской коллегии кардиологов был опубликован другой метаанализ, в котором говорится о снижении риска инсульта на 21% на фоне приема препарата калия в суточной дозе 1,42 г и значимом снижении риска коронарных нарушений и сердечно-сосудистых осложнений в целом [8]. Препараты калия и магния находят применение и в хирургической анестезиологии. Р. Soave и соавт. сообщают, что применение магнезии в анестезиологической практике не только дает антиноцицептивный эффект благодаря блокаде NMDA-рецепторов и ассоциированных с ними каналов [33], но и необходимо для коррекции дефицита магния, который в чистом виде наблюдался у 7–11% госпитализированных пациентов, а в сочетании с другими электролитными нарушениями, особенно с гипокалиемией и гипофосфатемией, – у более чем 40% больных [25]. Восполнение дефицита магния в данном случае, по наблюдениям авторов, необходимо для предупреждения роста заболеваемости и смертности в послеоперационном периоде. Назначение калия и магния аспарагината особенно актуально при проведении операций на сердце и крупных сосудах, поскольку значимое снижение уровня калия и магния наблюдается также при экстракорпоральном кровообращении [3]. Если калия и магния аспарагинат не вводился предварительно, гипомагниемия развивалась у 50% пациентов. Таким образом, препараты калия и магния, в том числе Панангин, находят все более широкое применение в повседневной клинической практике.
Литература 1. Вислобоков А.И., Игнатов Ю.Д., Мельников К.Н. Фармакологическая регуляция ионных каналов мембраны нейронов / СПб.: Изд-во СПбГМУ. – 2006; 288 с. 2. Лесиовская Е.Е., Бахтина С.М., Бойко И.Н. Витамины, макро- и микро- элементы / СПб.: изд-во СПбХФА. – 2004; 140 с. 3. Трекова Н.А., Андрианова М.Ю., Толстова И.А., и др. Применение рас- твора калия и магния аспарагината для поддержания баланса калия и магния при кардиохирургических вмешательствах в условиях искусственного крово- обращения // Анестез. и реаниматол. – 2008; 5: 17–21. 4. Шестакова С.А., Долгодворов А.С., Кубынин А.Н. Нарушения водно- электролитного обмена и их фармакологическая коррекция / СПб.: Изд-во СПбГМУ. – 2005; 91 с. 5. Al-Delaimy W., Rimm E., Willett W. et al. Magnesium intake and risk of coronary heart disease among men // J. Am. Coll. Nutr. – 2004; 23 (1): 63–9. 6. Ascherio A., Rimm E., Hernan M. et al. Intake of potassium, magnesium, calcium, and fiber and risk of stroke among US men // Circulation. – 1998; 98: 1198–204. 7. Cooper W., Kuan P., Reuben S., Vanderburg M. Cardiac arrhythmias following acute myocardial infarction: Assosiation with serum potassium level and prior diuretic therapy // Eur. Heart J. – 1984; 5: 464–9. 8. D’Elia L., Barba G., Cappuccio F., Strazzullo P. Potassium intake stroke and cardiovascular disease. A meta-analisys of prospective studies // J. Am. Coll. Cardiol. – 2011; 57: 1210–19. 9. Dykcner T., Wester P. Relation between potassium, magnesiumand cardiac arrhythmias // Acta Med. Scand. Suppl. – 1981; 647: 163–9. 10. Gettes L., Surawicz B. Effects of low and high concentrations of potassium on the simultaneously recorded Purkinje and ventricular action potentials of the perfused pig moderator band // Circ. Res. – 1968; 23: 717–29. 11. Hoffman B., Suckling E. Effect of several cations on transmembrane potentials of cardiac muscle // Am. J. Physiol. – 1956; 186: 317–24. 12. Hohnloser S., Verrier R., Lown B., Reader E. Effect of hypokalemia on susceptibility to ventricular fibrillation in the normal and ishemic canine heart // Am. Heart J. – 1986; 112: 32–5. 13. Ito S., Surawicz B. Transient, «paradoxical» effects of increasing extracellular K+ -concentration on transmembrane potential in canine cardiac Purkinje fibers // Circ. Res. – 1977; 41: 799–807. 14. Keller P., Aronson R. The role of magnesium in cardiac arrhythmias // Prog. Cardiovasc. Dis. – 1990; 32: 433–48. 15. Khaw K., Barrett-Connor E. Dietary potassium and stroke-associated mortality. A 12-year prospective population study // N. Engl. J. Med. – 1987; 316: 235–40. 16. Kulick D., Hong R., Ryzen E. Electrophysiologic effects of intravenous magnesium in patients with normal conduction systems and no clinical evidence of significant cardiac disease // Am. Heart J. – 1988; 115: 367–73. 17. Larsson S., Orsini N., Wolk A. Dietary potassium intake and risk of stroke. A dose-response meta-analysis of prospective studies // Stroke. – 2011; 42 (10): 2746–50. 18. Nordrehaug J., Johanessen K., Von der Lippe G. Serum potassium concentration as a risk factor of ventricular arrhythmias early in acute myocardial infarction // Circulation. – 1985; 71: 645–49. 19. Paice B., Paterson K., Onyanga-Omara F. et al. Record linkage study of hypokaliemia in hospitalized patients // Postgrad. Med. J. – 1986; 62: 187–91. 20. Pelzer D., Trautwein W. Currents through ionic channels in multicellular cardiac tissue and single heart cells // Experentia. – 1987; 43: 1153–62. 21. Sakmann B., Trube G. Conductance properties of single inwardly rectifying potassium channels in ventricular cells from guinea pig heart // J. Physiol. – 1984; 347: 641–57. 22. Sarkkinen E., Kastarinen M., Niskanen T. et al. Feasibility and antihypertensive effect of replacing regular salt with mineral salt – rich in magnesium and potassium – in subjects with mildly elevated blood pressure // Nutr. J.– 2011; 10: 88. 23. Schulman M., Narins R. Hypokalemia and cardiovascular disease // Am. J. Cardiol. – 1990; 65: 4–9. 24. Sheu S., Korth M., Lathrop D.A. et al. Intra- and extra-cellular K+ and Na+ activities and resting membrane potential in sheep cardiac Purkinje strands // Circ. Res. – 1980; 47: 692–700. 25. Soave P.M., Conti G., Costa R., Arcangeli A. Magnesium and anaesthesia // Curr. Drug Targets. – 2009; 10 (8): 734–43. 26. Surawicz B. Relation between electrocardiogram and electrolites // Am. Heart J. – 1967; 73: 814–43. 27. Surawicz B., Lepeschkin E., Herrlich H. Low and high magnesiu concentrations at various calcium levels: Effect on the monophasic action potential, electrocardiogram and contractility of isolated rabbit hearts // Circ. Res. – 1961; 9: 811–8. 28. Takanaka C., Ogunyankin K., Sarma J., Singh B. Antiarrhythmic and arrhythmogenic actions of varying levels of extracellular magnesium: Possible cellular basis for the differences in the efficacy of magnesium and lidocaine in torsades de pointes // J. Cardiovasc. Pharmacol. Ther. – 1997; 2: 125–34. 29. Thompson R. Gobb L., Hypokalemia after resuscitation out-of-hospital ventricular fibrillation // JAMA. – 1982; 248: 2860–3. 30. Tsuji H., Venditti F., Evans J., et al. The assiciations of levels of serum potassium and magnesium with ventricular premature complexes (the Framingham Heart Study) // Am. J. Cardiol. (US). – 1994; 74: 232–5. 31. Yang T., Roden D. Extracellular potassium modulation of drug block of Ikr // Circulation. – 1996; 93: 407–11. 32. Yang C. Calcium and magnesium in drinking water and risk of death from cerebrovascular disease // Stroke. – 1998; 29: 411–4. 33. Zhu Y., Auerbach A. K+-occupancy of the n-methyl-d-aspartate receptor channel probed by Mg2+-block // J. Gen. Physiol. – 2001; 117(3): 287–98.
Что такое гиперкалиемия?
Гиперкалиемией называют состояние, при котором уровень сывороточного калия превышает 5 ммоль/л. Гиперкалиемия встречается у 1-10 % пациентов, госпитализируемых в больницы.
Гиперкалиемией называют состояние, при котором уровень сывороточного калия превышает 5 ммоль/л. Гиперкалиемия встречается у 1-10 % пациентов, госпитализируемых в больницы. Количество пациентов с гиперкалиемией увеличилось в последние годы в связи с увеличением числа пациентов, принимающих лекарства, влияющие на ренин-ангиотензин-альдостероновую систему (РААС).
Калий внутри организма человека
Калий – важнейший электролит организма человека. Он играет ключевую роль в проведении нервных импульсов и сокращении мышц. 98% калия сосредоточено во внутриклеточной жидкости, концентрация калия здесь достигает 140 ммоль/л. Вне клеток находится только 2% калия, концентрация здесь составляет 3,8-5,0 ммоль/л.
Роль калия в организме
Калий – основной внутриклеточный катион (положительно заряженный ион) в отличие от натрия – основного внеклеточного катиона.
Функционально калий и натрий связаны между собой:
- Создание мембранного потенциала, важного для мышечного сокращения (скелетных и сердечной мышцы), обеспечивается путем поддержания высокой концентрации натрия вне клетки и калия внутри клетки (натрий-калиевый насос, см.рис.1).
- Поддержание кислотно-основного равновесия, осмотического баланса, водного баланса
- Активация многих ферментов
Механизмы регуляции обмена калия
Чтобы поддерживать нормальный баланс калия (транспорт между внутри- и внеклеточной жидкостью) требуется слаженное взаимодействие всех регуляторных механизмов. Основной механизм регуляции уровня калия — выделение его почками. Этот механизм управляется гормоном надпочечников альдостероном. Наличие этого механизма гарантирует, что, несмотря на высокое содержание калия в пище (от 40 ммоль до 200 ммоль), уровень его в сыворотке крови будет поддерживаться на постоянном уровне. Нарушение регуляции уровня калия, и, как следствие, повышение его в крови, может изменять возбудимость мембран. А значит, будет нарушаться функция нервов, мышц, сердца.
Рис.1 Схема регуляции чрезмембранного транспорта калия Концентрация калия внутри клеток поддерживается путем активного транспорта калия с помощью Na-K-АТФ-азы и пассивно за счет градиента концентрации. Скорость пассивного перемещения зависит от проницаемости калиевых каналов в клеточной мембране. Инсулин и бета-2-адреномиметики через цАМФ содействуют поглощению калия клетками, стимулируя Na-K-АТФ-азы. При дефиците инсулина и действии бета-2-андреноблокаторов увеличивается выход калия из клеток, что ведет к гиперкалиемии. Ацидоз, гиперосмолярность, лизис клеток также вызывает выход калия и увеличение уровня калия в крови. На схеме: ECF=extracelluar fluid (внутриклеточная жидкость); ICF=intracellular fluid (внеклеточная жидкость) Альдостерон – минералкортикоидный гормон, синтезирующийся в коре надпочечников из холестерола. Под действием альдостерона в почках увеличивается канальциевая реабсорбция (то есть обратное всасывание из первичной мочи) ионов натрия: альдостерон стимулирует переход натрия внутрь клеток, а калия – наружу (в межклеточное пространство, то есть далее калий переходит в мочу, выделяясь из огранизма) – см.рис.2. Альдостерон также увеличивает секрецию почками ионов калия и водорода. Таким образом, в организме повышается содержание натрия и внеклеточной жидкости (в организме удерживается вода). Уровень альдостерона зависит от уровня натрия (Na+) и калия (К+). При высокой концентрации калия и низкой концентрации натрия синтез и секреция альдостерона усиливается. Наиболее важное влияние на уровень альдостерона оказывается ренин-ангиотензиновая система (см.РААС). Также на уровень альдостерона оказывают влияние и другие факторы.
Многие факторы участвуют в развитии гиперкалиемии, которая развивается в результате снижения выделения калия или увеличении выхода калия из клеток.
Гиперкалиемия может быть ложной (псевдогиперкалиемия), это надо исключать в первую очередь (за исключением тех случаев, когда требуется экстренная помощь).
Псевдогиперкалиемия
Псевдогиперкалиемией называется состояние, когда определенный в лаборатории уровень кальция не отражает уровня калия в организме. Это связано с тем, что внутриклеточный уровень калия очень высок и в определенных ситуациях он высвобождается из клеток после забора крови. В таких случаях, для подтверждения истинной гиперкалиемии следует повторить забор крови и одновременно измерить уровень калия в плазме и сыворотке. Концентрация в сыворотке выше концентрации в плазме на 0.2–0.4 ммоль/л, что связано с формированием сгустка и выходом калия из клеток в сыворотку.
Таблица 1: причины псевдогиперкалиемии
- Не вовремя выполненный анализ
- Забор крови из вены, в которую вводился калий
- Слишком сильное давление при наложении жгута или интенсивная работа кулаком для наполнения вен
- Гемолиз при протекании крови через тонкую иглу или травматическая венепункция
- Длительное хранение крови
- Высокий лейкоцитоз или тромбоцитоз (значительно повышенный уровень лейкоцитов или тромбоцитов)
- Необычные генетические нарушения (семейная гиперкалиемия)
Гиперкалиемия при повышенном поступлении калия
Чрезмерное поступление калия с пищей может способствовать гиперкалиемии, если параллельно снижается выделение калия с мочой. При нормальной функции почек весь калий должен выводиться.
Таблица 2: продукты с высоким содержанием калия
- Заменители соли
- Фиги
- Патока
- Отруби, злаки, пшеничные ростки
- Овощи (шпинат, томаты, морковь, картофель, брокколи, лимская фасоль, цветная капуста) и грибы
- Сушеные фрукты, орехи, семечки
- Фрукты (бананы, киви, апельсины, манго, дыня)
Гиперкалиемия может быть связана с гемотрансфузией — внутривенным введением клеток крови, из которых калий выходит во внеклеточное пространство, со слишком быстрым введением препаратов кальция для лечения гипокалиемии, при высоком содержании калия при парентеральном питании.
Гиперкалиемия, связанная с выходом калия из клеток
Некоторые экзогенные и эндогенные факторы могут нарушать обмен калия между межклеточной и внутриклеточной жидкостями и увеличивать концентрацию калия в сыворотке. Однако, этот механизм редко вызывает тяжелую гиперкалиемию, за исключением тех случаев, когда фактором является, например, повреждение тканей, некроз (местная гибель тканей в результате повреждения), рабдомиолиз, распад опухоли, тяжелые ожоги.
Таблица 3:причины перераспределения калия Перераспределение калия между внеклеточной и внутриклеточной жидкостями
- Некроз мышц, миолиз (рабдомиолиз – повреждение скелетных мышц), распад опухоли, тяжелые ожоги
- Дефицит инсулина (в норме этот гормон ускоряет перемещение калия в клетки)
- Метаболический ацидоз
- Гиперосмолярность (гипергликемия – повышение уровня глюкозы в крови, введение маннитола)
- Лекарства (например, сукцинилхолин (он же дитилин, листенон), бета-блокаторы, дигоксин)
- Гиперкалиемический периодический паралич (приступы развиваются чаще всего через 30-40 минут после физической нагрузки)
Снижение экскреции калия
- Повреждение почек (гломерулярная фильтрация <20 мл/мин)
- Снижение активности минералкортикоидов
- Гипоренинемическая форма гипоальдостеронизма (хронические заболевания почек, диабетическая нефропатия, НПВС)
- Недостаточность надпочечников (болезнь Аддисона, врожденный дефект ферментов)
- Блокаторы альдостерона (см.таблицу 4)
- Невосприимчивость к альдостерону (серповидно-клеточная анемия, системная красная волчанка, амилоидоз, обструктивная нефропатия)
Снижение скорости фильтрации мочи и доставки натрия к дистальному нефрону
- Гиповолемия
- Некоторые генетические нарушения, например, синдром Гордона (Gordon’s syndrome)
Гиперкалиемия, вызванная нарушением выделения калия
Основная часть калия выводится почками, поэтому поражение почек является основной причиной гиперкалиемии. На поражение почек приходится до 75% случаев этого состояния.
У пациентов с хроническими заболеваниями почек способность к выделению калия сохраняется до тех пор, пока не развивается почечная недостаточность (когда фильтрация снижается менее 15-20 мл/мл) или в тех случаях, когда пациент потребляет большое количество калия или принимает препараты, повышающие уровень калия.
Повреждение юкстагломерулярного аппарата приводит к дефициту продукции ренина (см.РААС), что вызывает гипонатриемию и гипоальдостеронизм, что также может вызывать гиперкалиемию даже в отсутствии тяжелых повреждений почек. Гипоренинемический гипоальдостеронизм также известен как 4 тип канальциевый ацидоз 4 типа, так как часто ассоциирован с легким или средней тяжести метаболическим ацидозом, с нормальным анионным промежутком (разницей между катионами и анионами; Anion gap = (Na + K) — (Cl + [HCO3-]) (единицы измерения – моль/л)). Чаще всего это состояние развивается при диабетической нефропатии.
Также гипоальдостеронизм может быть следствием первичных заболеваний надпочечников (болезнь Аддисона, врожденные нарушения синтеза стероидов, дефицит 21-гидроксилазы) или снижения минералкортикоидной активности. Последняя проблема часто связана с серповидно-клеточной анемией, системным красной волчанкой, амилоидозом, обструктивной нефропатией, использованием калийсберегающих диуретиков . В редких случаях выявляется мутация гена рецептора минералкортикоидов.
В общем, нарушение обмена минералкортикоидов не вызывает гиперкалиемию, если в дистальный нефрон попадает нормальное количество натрия. Таким образом, не всегда у пациентов с болезнью Аддисона развивается гиперкалиемия, если они имеют адекватное потребление соли. Нарушение мочевыделения или доставки натрия в дистальный нефрон играет важную роль в развитии гиперкалиемии. Эти нарушения могут быть вызванными внутренними факторами или (чаще) некоторыми лекарствами (см.таблицы 3, 4).
Лекарства, вызывающие гиперкалиемию
Лекарственные препараты могут нарушать калиевый гомеостаз по нескольким механизмам: активация трансмембранного транспорта калия, уменьшение почечной экскреции (изменение действия альдостерона, доставки натрия к дистальному нефрону, изменение функции собирательных трубочек). Риск возрастает, когда такие препараты принимают пациенты с почечной недостаточностью. Особенно подвержены развитию гиперкалиемии пожилые пациенты и пациенты с диабетом. В этих группах такие препараты надо использовать с осторожностью, начиная с малых доз и контролируя уровень калия каждый раз при изменении дозы. Не существует рекомендаций в отношении количества исследований, частота определения уровня калия зависит от уровня почечной недостаточности, наличия диабета, принимаемых лекарств, сопутствующих заболеваний.
В частности, очень осторожно надо подходить к ведению пациентов с нарушением электропроводимости сердечной мышцы, так как даже незначительное увеличение содержания калия может привести к аритмии.
Полный список лекарств – в таблице.
Лекарства, нарушающие трансмембранный транспорт калия
- Бета-блокаторы
- Дигоксин
- Гиперосмолярный растворы (маннитол, глюкоза)
- Суксаметоний (Листенон)
- Внутривенное введение положительно заряженных аминокислот
Вещества, содержащие калий
- Калиевые добавки
- Salt substitutes
- Растительные препараты (люцерна, одуванчик, хвощ, молочай, крапива)
- Красные клетки крови (при их разрушении калий высвобождается)
Лекарства, снижающие секрецию альдостерона
- Ингибиторы АПФ
- Блокаторы рецептора ангиотензина II
- НПВП (НПВС)
- Препараты гепарина
- Противогрибковые препараты (кетоконазол, флуконазол, интраконазол)
- Циклоспорины
- Програф
Лекарственные вещества, которые блокируют связывание альдостерона и минералкортикоидных рецепторов
- Спиронолактон
- Инспра (Eplerenonum)
- Дроспиренон
Препараты, ингибирующие активность калиевых каналов в эпителиальных клетках
- Калийсберегающие диуретики (амилорид, триамтерен)
- Триметоприм (противомикробный препарат)
- Пентамидин (противомикробный препарат)
Остановимся на некоторых из них:
Ингибиторы ангиотензин-превращающего фермента (Angiotensin converting enzyme (ACE) inhibitors) и блокаторы рецептора ангиотензина II (angiotensin II receptor blockers (ARBs)) активно используются для защиты почек и снижения смертности от сердечных заболеваний, особенно у диабетиков. Также они входят в стандартные схемы лечения пациентов с хроническими заболеваниями сердца.
Эти препараты предрасполагают к развитию гиперкалиемии, так как нарушают секрецию альдостерона и снижают реперфузию в почках (и уровень гломерулярной фильтрации). Оба препарата уменьшают выделение калия с мочой.
Они не вызывают гиперкалиемию у пациентов с нормальной функцией почек; степень супрессии выделения альдостерона недостаточна для значительного нарушения экскреции калия, если не было предшествующего гипоальдостеронизма (вследствие какого-то заболевания или приема иных лекарств). К несчастью, люди, принимающие эти препараты, имеют высокий риск развития гиперкалиемии. Около 10% амбулаторных пациентов гиперкалиемия развивается в течение года после начала лечения ингибиторами АФП или блокаторами рецептора ангиотензина II.
Более того, эти препараты содействуют развитию гиперкалиемии у 10-38% пациентов, доставленных в больницы. При этом риск особенно повышен, если пациент принимает высокие или дозы препаратов или в комбинации с другими препаратами, вызывающими гиперкалиемию.
Антагонисты рецепторов альдостерона (Aldosterone (mineralocorticoid) receptor antago¬nists) также часто используются при лечении пациентов congestive cardiac failure с тех пор как the Randomized Aldactone Evaluation Study показало, что добавление спиронолактона в лечение снижается количество осложнений и смертности. В этом исследовании указано, что тяжелая гиперкалиемия развилась только у 2% пациентов, когда уровень концентрации креатинина был 106 ммоль/л, а доза спиронолактона не превышала 25 мг в сутки. В противоположность этому, population based time-series analyses, демонстрируют значительное повышение госпитализации и смертности от гиперкалиемии. Это вероятно, так как в исследование включены пациенты с тяжелым нарушением функции почек, принимавшие высокие дозы спиронолактона. Эти пациенты чаще других в исследовании принимают добавки калия или другие препараты, нарушающие выделение калия. Риск возрастает при комбинации спиронолактона с ингибиторами АФП и ARBs, особенно у пожилых пациентов с нарушениями функции почек.
Нестероидные противовоспалительные препараты (НПВС, Non-steroidal anti-inflammatory drugs (NSAIDs)) ингибируют секрецию ренина (что ведет к гипоальдостеронизму и снижению экскреции калия почками) и могут нарушать функцию почек. Эти препараты могут задавать judiciously у пациентов с диабетом или почечной недостаточностью, особенно, если пациенты принимают другие препараты (ингибиторы ACE и ARBs).
Как диагностируется гиперкалиемия
Гиперкалиемия часто протекает без симптомов и обнаруживается при лабораторном исследовании. Когда симптомы есть, они не специфичны, и преимущественно связаны с нарушениями мышечных функций (парестезии, мышечная слабость, усталость) или функций сердца (palpitations).
ЭКГ: высокий «пикообразный» зубец Т, выравнивание или отсутствие зубца Р, расширение комплекса QRS, sine waves.
Тем не менее, ЭКГ не является чувствительным методом диагностики гиперкалиемии. В исследовании Acer и коллег почти у половины пациентов с уровнем калия выше 6,5 ммоль/л не было изменений на ЭКГ. Кроме того, у некоторых пациентов наблюдается постепенное изменение функции сердца, а у других наблюдается быстрый прогресс от доброкачественных изменений к смертельным желудочковым аритмиям.
Обследование пациентов с гиперкалиемией должно включать:
- Тщательный анализ истории болезни для выявления потенциальных факторов риска, таких как нарушение функции почек, диабет, надпочечниковая недостаточность, использование лекарств, которые могут вызывать гиперкалиемию.
- Лабораторные тесты должны быть направлены на подтверждение истории болезни и физикального обследования, и должны включать мочевину, креатинин, электролиты, осмолярность (острое повышение осмолярности может вызвать выход калия я из клеток), а также анализ концентрации калия в моче.
- У некоторых пациентов проводятся дополнительные специальные тесты, такие как определение фракционной экскреции натрия или транстубулярный градиент калия может быть использовано для различения почечной и непочечной причин гиперкалиемии.
Что делать с тяжелой гиперкалиемией?
Руководство по ведению гиперкалиемии базируется на мнениях экспертов, так как есть недостаток клинических исследований. Лечение должно быть направлено на восстановление электролитного обмена, профилактике серьезных осложнений и лечение основного заболевания. Рисунок В ведении легкой или средней тяжести гиперкалиемии используются петлевые диуретики для увеличения экскреции калия. Потребление калия с пищей должно быть ограничено. Дозу лекарств, увеличивающих уровень калия в крови, следует максимально снизить или отменить. Если же у пациента имеется нарушение функции почек, диуретики могут быть неэффективны. Тогда требуются другие меры, в частности, проведение диализа.
Тяжелая гиперкалиемия является угрожающим жизни состоянием, так как может вызвать серьезные нарушения работы сердца и нервно-мышечной системы, включающими остановку сердца и паралич дыхательной мускулатуры. Следовательно, требуется неотложная и агрессивная терапия. Многие авторы приводят следующие критерии тяжелой гиперкалиемии: более 6,0 ммоль/л + изменения на ЭКГ, либо более 6,5 ммоль/л независимо от наличии изменений на ЭКГ.
Если на ЭКГ есть признаки гиперкалиемии или в случае остановки сердца у пациентов, находящихся на диализе, например, терапия начинается без лабораторных данных. Другие факторы, которые требуют упреждающего лечения: быстрое нарастание уровня калия, признаки ацидоза, быстрое ухудшение функции почек.
Большинство рекомендаций и эксперты советуют при тяжелой гиперкалиемии лечение следует проводить в условиях стационара, что позволяет непрерывно проводить мониторинг сердечной деятельности, так как даже у пациентов без симптомов и изменений на ЭКГ может развиваться аритмия, угрожающая жизни.
Хотя экстренный диализ удаляет калий из организма, необходимо срочно начинать лечение основного заболевания, так как Cochrane systematic review of emergency interventions for hyperkalaemia от 2005 года рекомендует одновременно делать три вещи:
- Первым шагом является стабилизация деятельности миокарда, снижение вероятности аритмии. Внутривенный кальций используется как непосредственный антагонист калия при влиянии на мембрану, стабилизирующий сердечную проводимость. Глюконат кальция в объеме 10 мл 10% раствора вводится в течение 3-5 минут под контролем работы сердца на кардиомониторе. Инфузия кальция не оказывает влияния на уровень сывороточного калия, но оказывает влияние на работу сердца: изменения на ЭКГ видны уже через 1-3 минуты после введения кальция, эффект last for 30-60 minutes. Инфузия может быть повторена, если в течение 5-10 минут не возникает эффекта. Следует очень осторожно применять кальций у пациентов, принимающих дигоксин, так как кальций усиливает токсические эффекты дигоксина.
- Второй шаг – перевод калия из внеклеточной жидкости во внутриклеточную. Это снижает уровень сывороточного калия.Это достигается введением инсулина или бета-2-агонистов, которые стимулируют натриево-калиевый насос. Инсулин вводится внутривенно струйно с достаточным количеством глюкозы (для предотвращения гипогликемии). Эффект от введения инсулина наступает через 20 минут, достигает максимума через 30-60 минут, сохраняется до 6 часов. Из селективных бета-2-агонистов чаще всего используется сальбутамол. Сальбутамол употребляется с помощью небулайзера Эффект наступает через 20 минут, максимальное действие на 90-120 минутах. Сальбутамол может быть использован один или в комбинации с инсулином. Пациентам с ацидозом также может быть назначен бакарбонат натрия, хотя вопрос о пользе этого препарата при гиперкалиемии пока остается спорным.
- В-третьих, проводятся мероприятия по выведению калия из организма. Сильнодействующие петлевые диуретики (например, 40-80 мг фуросемида внутривенно) повышают почечную экскрецию калия путем увеличения мочеобразования и доставки натрия в дистальный нефрон. Но диуретики работают только при сохраненной функции почек, а у многих пациентов с гиперкалиемией имеются острые или хронические почечные заболевания. Катион-обменные смолы, которые удаляют калий из внеклеточной жидкости в обмен на натрий через кишечник, также используются широко, хотя их эффективность является спорной. Они действуют быстрее в виде клизмы, чем при пероральном введении. Достижение эффекта может занять 6 часов. Диализ является окончательным для лечения пациентов с тяжелой гиперкалиемией и прогрессирующими заболеваниями почек.
Длительное ведение гиперкалиемии
После экстренной помощи должны быть приняты меры, предотвращающие повторение гиперкалиемии. В первую очередь следует проанализировать принимаемые пациентом лекарства. По возможности снизить или отменить лекарства, повышающие уровень калия. Так как ингибиторы АФП и блокаторы рецептора ангиотензина II замедляют прогрессирование хронических почечных заболеваний, использование других мер для контроля за гиперкалиемией или снижение дозы препарата является более предпочтительным, чем прекращение приема этих препаратов. Разумно ограничить потребление калия до 40-60 ммоль в день. Также может быть эффективно применение диуретиков. Тиазидные диуретики могут применяться у пациентов с сохраненной функцией почек, но они обычно неэффективны, если клубочковая фильтрация менее 40 мл/мин, когда более предпочтительными являются петлевые диуретики. Флудрокортизон может быть использован у пациентов с гипоренинемическим гипоальдостеронизмом. Однако, этот препарат следует использовать с осторожностью, особенно у пациентов с диабетом 2 типа, который часто протекает с гипертонией, так как препарат приводит к задержке жидкости и повышению давления.
Советы для неспециалистов
- У пациентов без предрасположенности к гиперкалиемии повторить анализ на калий для исключения псевдогиперкалиемии.
- Не забывайте про возможные скрытые причины гиперкалиемии, в том числе, НПВС
- Ингибиторы АПФ и блокаторы рецепторов ангиотензина II должны назначаться с небольших доз, уровень калия должен контролироваться через неделю после начала лечения и после увеличения дозы
- Все пациенты с гиперкалиемией должны пройти ЭКГ (12 отведений)
- Изменения на ЭКГ и аритмия, связанные с гиперкалиемией, требуют срочной медицинской помощи.
Вопросы для настоящих и будущих исследователей
- Насколько важен вклад различных факторов риска в развитие гиперкалиемии и как оценить их?
- С увеличением использовать кардио- и ренопротекторов, способствующих удержанию калия, какой метод наиболее предпочтителен для контроля за уровнем калия?
Более глубокое понимание молекулярных механизмов, лежащих в основе поддержания уровня калия во внеклеточной жидкости, разработка новых терапевтических стратегий для лечения угрожающей жизни гиперкалиемии.
| Спиронолактон (Spironolactone) – калийсберегающий диуретик, конкурентный антагонист альдостерона по влиянию на дистальные отделы нефрона. Повышает выведение Na+, Cl- и воды и уменьшает выведение K+ и мочевины Торговые названия: Верошпирон, Спиронолактон. Противопоказания: Болезнь Аддисона, гиперкалиемия, гиперкальциемия, гипонатриемия, хроническая почечная недостаточность, анурия, печеночная недостаточность, сахарный диабет при подтвержденной или предполагаемой хронической почечной недостаточности, диабетическая нефропатия, I триместр беременности, метаболический ацидоз, нарушение менструального цикла или увеличение молочных желез, повышенная чувствительность к спиронолактону. Подробнее на сайте vidal.ru: | Экзогенный – в дословном переводе образованный вовне. В медицине употребляется относительно организма и означает, что некий фактор образован и поступает извне. Например, экзогенными факторами являются пищевые. Эндогенный – противоположный термин, означает, что некий фактор образован внутри организма. |
РААС – ренин-ангиотензин-альдостероновая система. При снижении давления в почках (кровотечение, потеря жидкости, снижение концетрации хлорида натрия) в юкстагломерулярных клетках почек вырабатывается фермент ренин. Субстрат этого фермента (вещество, на которое фермент дейсвует) – ангиотензиноген. Под действием ренина ангиотензиноген превращается в ангиотензин I. Ангиотензин II образуется из ангиотензина II под действием ангиотензинпревращающего фермента (АПФ, ACE) и оказывает следующие действия:
Наследственная предрасположенность к выраженному сосудистому спазму, в том числе, связанному с АПФ определяется с помощью блока анализов «Полиморфизм генов сосудистого тонуса». | ЭКГ – электрокардиография – исследование, основанное на регистрации электрических полей, образующихся при работе сердца, с помощью специального прибора — электрокардиографа. ЭКГ регистрируется с помощью специальных электродов, наложенных на определенные участки тела. ЭКГ является распространенным методом для оценки работы сердца. Анализ ЭКГ, азбука Анализ ЭКГ, практика: https://www.practica.ru/BK1/5.htm |
| Ацидоз (от лат. acidus — кислый) – изменение кислотно-щелчного состояния, связанное с повышением кислотности (повышение ионов водорода). Об ацидозе говорят, когда рН артериальной крови падает ниже 7,35. В противоположность алкалозу, когда рН превышает 7,45. Метаболический ацидоз связан с нарушением обмена веществ (избыточное образование кислот, недостаточное их выведение, потеря оснований) Респираторный (дыхательный) ацидоз развивается при нарушениях легочной вентиляции (дыхательная недостаточность или недостаточность кровообращения в легких). | Геодиализ (диализ) – метод внепочечного очищения крови при почечной недостаточности. Гемодиализ проводится с помощью аппарата «искусственная почка». |
| Гомеостаз – в физиологии – способность саморегулирующейся системы сохранять постоянство внутреннего состояния путем скоординированных реакций, направленных на поддержание динамического постоянства. Термин предложен американским физиологом У. Кенноном в 1929. Примеры гомеостаза – поддержание рН крови, температуры тела, давления и так далее. | Парентеральное питание (parenteral nutricion) – это введение питательных веществ (углеводы, аминокислоты, липиды, соли, витамины), внутривенно, когда прием естественный прием пищи невозможен. |
| Синдром Гордона – редкое заболевание, связанное с повышением реабсорбции хлора в дистальных отделах нефрона. Характерно наличие гиперкалиемии, метаболического ацидоза, гипоренинемия, гипоальдостеронемия, снижение чувствительности почек к минералкортикоидам. | |
| Минералкортикоиды – группа кортикостероидных гормонов коры надпочечников, влияющих на водно-солевой обмен (альдостерон, дезоксикортикостерон). | |
| Юкстагломерулярный аппарат почек (ЮГА) – совокупность клеток почечной ткани, образующих и выделяющих биологически активные вещества, в том числе, ренин. |
Теги:
гиперкалиемия, калий, электролиты
Назад в раздел