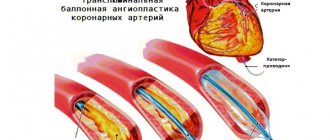
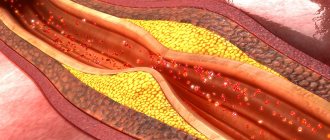
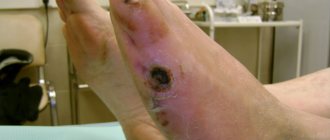
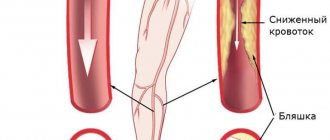
Синдром Педжета-Шреттера — тромбоз подключичной вены, распространяющийся на подключичную и подмышечную вены, а также на вены плеча, что приводит к нарушению венозного оттока в руке. Синдром также называют травматическим тромбозом или синдромом усилия. Несмотря на относительную его редкость, он стал чаще диагностироваться в последнее десятилетие. Основные жалобы это отёк тканей верхней конечности и распирающие боли.
Первый случай синдрома был описан Джеймсом Педжетом в 1875 году, а в 1894 году фон Шреттер идентифицировал сосудистую травму как потенциальную причину заболевания. Термин синдром Педжета-Шреттера впервые был использован в 1948 году.
Общие сведения о тромбозе
Тромбоз
ー процесс прижизненного свертывания крови в полости сосудов и сердца. Этот процесс опасен еще и тем, что часть тромба может оторваться и занестись током крови в другие органы. Например, при тромбозе глубоких вен нижних конечностей часто развивается тромбоэмболия легочной артерии или сосудов головного мозга.
5.3. Лечебная тактика при тромбозе глубоких вен
Консервативное лечение
Постельный режим и возвышенное положение конечности может уменьшить болевой синдром, однако строгий постельный режим существенно не влияет на частоту развития ТЭЛА, при условии что верифицированный тромбоз не является флотирующим. Более того, болевой синдром и отек уменьшаются гораздо быстрее при ранней активизации и адекватной компрессии нижних конечностей с помощью специализированного компрессионного трикотажа 2—3-го класса. Когда отек нестабилен (т. е. объем конечности имеет значительную суточную динамику), допустимо использование эластичных бинтов длинной растяжимости.
Неоспорима необходимость адекватной антикоагулянтной терапии как основы лечения больных с ТГВ (в том числе бессимптомного). Антикоагулянтная терапия НФГ или НМГ при обоснованном подозрении на ТГВ может быть начата до инструментальной верификации диагноза.
Лечение начинают с парентерального введения лечебных доз антикоагулянтов.
Схема лечения нефракционированным гепарином
1. Внутривенно болюсом 80 МЕ/кг (или 5000 МЕ) и инфу зия с начальной скоростью 18 МЕ/кг в 1 ч (или 1250— 1300 МЕ/ч), затем подбор дозы МЕ по значениям АЧТВ. Цель — поддержка АЧТВ в 1,5—2,5 раза выше верхней границы нормы для конкретной лаборатории.
2. Внутривенно болюсом 5000 и затем подкожно 450 МЕ/кг в сутки каждые 8 ч с подбором дозы для поддержания значений АЧТВ, через 4 ч после инъекции в 1,5—2,5 раза выше верхней границы нормы для конкретной лаборато рии
Известно, что частота ретромбоза при АЧТВ, находящемся в пределах 1,5—2 от нормы, составляет 4—6%, тогда как при АЧТВ, составляющем менее 1,5 от нормы, частота развития ретромбоза возрастает до 23%.
Необходимо помнить, что применение гепарина может индуцировать тромбоцитопению, поэтому при лечении гепарином обязательно контролировать уровень тромбоцитов периферической крови на 1, 3, 5, 7 и 10-е сутки. Также необходимо следить за гематокритом, уровнем гемоглобина и клиренсом креатинина.
Лучшей биодоступностью и более прогнозируемой фармакокинетикой и фармакодинамикой обладают НМГ при подкожном введении. Благодаря этим свойствам НМГ не требуют постоянного лабораторного контроля, кроме определения количества тромбоцитов. Исключение составляют пациенты с выраженным дефицитом или избытком массы тела, а также больные с почечной недостаточностью. В этих случаях рекомендовано определение анти-Xа-активности. Кроме того, фармакодинамика НМГ позволяет использовать их один или два раза в день.
Схема лечения низкомолекулярными гепаринами:
Клексан (Эноксапарин)
1. Подкожно 100 анти-Ха МЕ (1 мг)/кг 2 раза в сутки
2. Подкожно 150 анти-Ха МЕ (1,5 мг)/кг 1 раз в сутки
Фрагмин (Далтепарин) 1. Подкожно 100 анти-Ха МЕ/кг 2 раза в сутки
2. Подкожно 200 анти-Ха МЕ/кг (максимально 18 000 МЕ) 1 раз в сутки
Фраксипарин (Надропарин)
1. Подкожно 86 анти-Ха МЕ/кг 2 раза в сутки
2. Подкожно 172 анти-Ха МЕ/кг (максимально 17 100 МЕ) 1 раз в сутки
Фондапаринукс
Подкожно 5 мг 1 раз в сутки при массе тела 50 кг; 7,5 мг 1 раз в сутки при массе тела 50—100 кг; 10 мг 1 раз в сутки при массе тела более 100 кг
Первичная антикоагулянтная терапия НМГ и НФГ, как правило, требует перехода на оральные антикоагулянты для поддержания антикоагулянтного эффекта в течение длительного времени. В настоящее время для этой цели применяют антагонисты витамина К (Варфарин). Учитывая отсроченный фармакологический эффект АВК, необходимо начинать прием варфарина параллельно с парентеральным введением лечебных доз антикоагулянтов в течение не менее 5 дней. Парентеральное введение антикоагулянтов может быть прекращено при достижении терапевтических значений МНО (2,0— 3,0) дважды, с интервалом в 1 сут.
В соответствии с современными отечественными и зарубежными рекомендациями продолжительность проведения антикоагулянтной терапии для пациентов с первичным ТГВ после хирургического вмешательства или длительной иммобилизации должна составлять 3 мес. Для пациентов с идиопатическим ТГВ — 6—12 мес. Среди онкологических пациентов предпочтительнее использование НМГ вместо АВК в течение 3—6 мес. У пациентов с первичным ТГВ и выявленными антифосфолипидными антителами, тромбофилией рекомендовано продолжать терапию АВК не менее 12 мес. В дальнейшем вопрос решается индивидуально. При рецидивирующем ТГВ рекомендован пожизненный прием АВК.
Хирургическое лечение
Острый флеботромбоз в системе глубоких вен нижних конечностей — системное заболевание, не только негативно отражающееся на системе венозного и лимфатического возврата, но и ухудшающее функцию сердечно-сосудистой системы в целом. Если не предпринимать активных действий по лечению данной патологии, дальнейшее течение патологического процесса принимает стойкий, склонный к прогрессированию необратимый характер. Необходимость удаления тромба (хирургическое вмешательство или тромболитическая терапия) является частью стратегии, направленной на снижение риска развития посттромботического синдрома, особенно при распространенных тромбозах.
Малоинвазивные методы
На сегодняшний день это самая распространенная в клиническом применении группа методов, призванная решать перечисленные выше задачи в лечении больных с глубокими флеботромбозами. Здесь необходимо выделить три подгруппы методов: 1. Установка кава-фильтров или парциальная кава-пликация. 2. Регионарный и системный тромболизис. 3. Катетерная тромбэкстракция и реолитическая тромбэктомия.
Установка кава-фильтров и парциальная кава-пликация
В начале становления флебологии как отдельной хирургической специальности одним из главных вопросов, требующих незамедлительного решения, был вопрос профилактики ТЭЛА при флеботромбозах. После разработки в 1959 г. метода внешней пликации полой вены матрацными швами и внешней пликации клеммами удалось определить дальнейшее направление решения проблемы острых глубоких флеботромбозов и их осложнения — ТЭЛА. До 1967 г. метод, в сочетании с консервативной терапией, оставался единственным клиническим подходом в данной проблеме. Несмотря на то что выполнение технологии внешнего парциального клипирования клеммами сопряжено с необходимостью травматичного хирургического доступа и практически невыполнимо у тяжелобольных пациентов, данный подход в ограниченных ситуациях применяется и совершенствуется до настоящего времени (например, с использованием эндовидеоскопической техники). Созданный и примененный клинически в 1967 г. внутрипросветный зонтичный кава-фильтр Моббина—Аддина явился первым опытом подобного эндоваскулярного вмешательства. Дальнейшее развитие данного направления велось преимущественно по пути совершенствования конструкции кавафильтров и изучения их влияния на гемодинамику и клиническое течение основного процесса. Показаниями к имплантации кава-фильтра являются невозможность проведения и неэффективность адекватной антикоагулянтной терапии, флотирующий тромб с узким основанием, невозможность его удаления оперативно, рецидивирующая ТЭЛА у больных с высокой легочной гипертензией.
У молодых пациентов при устранимых факторах риска и причинах ТГВ необходимо имплантировать съемные модели, которые удаляют в срок до 30 сут после установки при устранении угрозы ТЭЛА.
Уже неоднократно отмечено, что в результате установки кава-фильтров в ближайшем периоде с частотой 1,5—8% могут возникать ТЭЛА, а в сроки до 3 лет с частотой 12—25% возникает тромбоз нижней полой вены.
Несомненным можно считать тот факт, что установка кава-фильтра — манипуляция, сама по себе представляющая угрозу для жизни пациента, значительно влияющая на качество жизни.
Обоснованность удаления тромба
В основе посттромботической болезни лежит затруднение венозного оттока, которое приводит к патофизиологическим изменениям, характерным для хронической венозной недостаточности: отеку, гиперпигментации и липодерматосклерозу. Именно нарушение венозного оттока, вызванное обструкцией, приводит к наиболее тяжелым формам посттромботической болезни. Таким образом, лечебная тактика, направленная на удаление тромба, является патофизиологически обоснованной и в значительной степени снижает риск тяжелой посттромботической болезни.
Показано, что у пациентов, которым выполняли тромбэктомию из глубоких вен, чаще сохраняется функция венозных клапанов бедренно-подколенного сегмента, чем у больных, которым проводилась только терапия антикоагулянтами. Накапливается также положительный опыт, показывающий высокую эффективность селективной тромболитической терапии, особенно при илеофеморальном флеботромбозе.
Тромболитическая терапия
Первые попытки системной тромболитической терапии с использованием активаторов плазминогена для лечения венозных тромбозов сопровождались высокой частотой геморрагических осложнений и неудовлетворительным тромболитическим эффектом. По данным крупных рандомизированных исследований, менее чем у половины больных, пролеченных с помощью системного тромболизиса, отмечается положительный эффект. Еще менее утешительными являются результаты лечения с применением только антикоагулянтов: только у 4% отмечается полная реканализация, у 14% — частичная. У оставшихся 82% больных либо объективных признаков улучшения не наступает вовсе, либо отмечается ухудшение.
Регионарный катетерный тромболизис
Основным механизмом тромболизиса является активация фибрин-связанного плазминогена и перевод его в активную форму — плазмин. Местное воздействие активатора плазминогена на тромб более эффективно и потенциально безопаснее, чем его системное использование. При местном введении тромболитического препарата в тромботические массы его общая доза и длительность введения уменьшаются, что уменьшает риск развития геморрагических осложнений.
Многочисленные исследования показывают обнадеживающие результаты лечения острых тромбозов глубоких вен при помощи регионарного катетерного тромболизиса. В качестве тромболитических преператов чаще использовали урокиназу и рекомбинантный тканевый активатор плазминогена (RT-PA). Удовлетворительные результаты лечения отмечаются в 75— 90% наблюдений. Частота геморрагических осложнений составляет от 5 до 11%. При этом внутричерепные кровоизлияния встречаются редко. Большинство геморрагических осложнений развивается в месте венозного доступа. Также редко развиваются клинически значимая ТЭЛА и ТЭЛА с летальным исходом. Исследование качества жизни показывает, что после проведения регионарного катетерного тромболизиса качество жизни больных выше, чем в группе пациентов, получавших только антикоагулянтную терапию.
Фармакомеханический тромболизис
Несмотря на хорошие результаты, достигаемые при использовании регионарного катетерного тромболизиса, лечение зачастую становится длительным, что, в свою очередь, увеличивает риск кровотечения. Время выполнения катетерного тромболизиса в среднем составляет 71 ч. Кроме того, при его выполнении необходимо наблюдение за больным в отделении интенсивной терапии. Эти недостатки привели к развитию сочетанной методики механического воздействия на тромб с фармакотерапией с целью быстрого восстановления венозного кровотока. К методам механического воздействия на тромб относятся эндоваскулярная механическая тромбэктомия с помощью катетера (AngioJet, Amplatz и др.), тромболизис, усиленный ультразвуком, изолированный сегментарный фармакомеханический тромболизис (ISPMT). Одним из важных условий выполнения фармакомеханического тромболизиса является срок от момента появления первых симптомов не более 7—14 сут. По данным литературы, фармакомеханический тромболизис показывает хорошие результаты при меньшей длительности пребывания пациента в палате интенсивной терапии и сопоставимом числе геморрагических осложнений.
Следует отметить, что российские эксперты не рекомендуют широкое использование регионарной тромболитической терапии. Исключением является проведение тромболитической терапии при первичном тромбозе подключичной вены (болезнь Педжета—Шреттера).
Открытая тромбэктомия при илеокавальном флеботромбозе
Выполнение своевременной открытой тромбэктомии при илеокавальном флеботромбозе позволяет добиться хороших непосредственных и отдаленных результатов при относительно небольшом количестве осложнений. Оперативному лечению подлежат все эмболоопасные тромбозы. Эмболоопасным (эмбологенным) считается флотирующий тромб длиной более 4 см с узким основанием. Выбор метода оперативного лечения определяется уровнем тромбоза, распространенностью, наличием сопутствующей патологии пациента, а также техническими возможностями стационара.
При обтурирующем флеботромбозе радикальная тромбэктомия выполняется в случаях сегментарного поражения, с небольшой (до 5 сут) давностью заболевания.
Положительные отдаленные результаты тромбэктомии обусловлены восстановлением проходимости проксимального сегмента вены и сохранением функции клапанного аппарата дистальнее тромбированного участка. Благоприятный исход операции зависит от правильного технического выполнения операции и отсутствия рецидива тромбоза. Следовательно, особое внимание необходимо уделять деталям оперативной техники, максимально полному удалению тромботических масс, а также проведению адекватной антикоагулянтной терапии в послеоперационном периоде.
В ряде клинических исследований показано, что раннее выполнение тромбэктомии при илеокавальном тромбозе позволяет достигнуть хороших отдаленных результатов с восстановлением проходимости венозного сегмента в 75—80% наблюдений. У большинства больных отмечается снижение частоты отеков и других симптомов посттромботической болезни в отдаленном периоде.
Техника выполнения венозной тромбэктомии
Продольным разрезом в паховой области выполняют доступ к общей бедренной вене, поверхностной бедренной вене, сафенофеморальному соустью и глубокой бедренной вене. Выполняется венотомия общей бедренной вены для обеспечения доступа к устью подкожной и глубокой бедренной вен.
При наличии тромботических масс ниже паховой связки нижняя конечность приподнимается и производится ее тугое эластичное бинтование. Стопа сгибается в тыльном направлении. Как только все тромботические массы ниже паховой связки удалены, выполняется тромбэктомия баллонным катетерным способом в илеофеморальном сегменте. Тромбэктомия из илеофеморального сегмента выполняется баллонным катетером № 8 или 10. При этом до проведения катетера в нижнюю полую вену необходимо частями удалить максимально возможное количество тромботических масс. «Проксимальную» тромбэктомию целесообразно выполнять под рентгенологическим контролем с введением контраста в баллон, особенно в тех случаях, когда установлен кава-фильтр, есть окклюзия нижней полой вены или трудности при проведении баллонного катетера. Во время выполнения данного этапа операции следует создать положительное давление в конце выдоха для снижения риска развития эмболии легочных артерий. Если тромб локализуется в нижней полой вене, тромбэктомию можно выполнить с дополнительным созданием баллонной окклюзии нижней полой вены проксимальнее границы тромботических масс, что является альтернативой установки кава-фильтра (рис. 5.7).
Рис. 5.7.
Создание баллонной окклюзии нижней полой вены проксимальнее верхней границы тромбоза для предотвращения развития легочной эмболии может быть альтернативой имплантации кава-фильтра
После завершения тромбэктомии из илеофеморального сегмента интраоперационно следует выполнить флебографию/ -скопию для оценки проходимости подвздошных вен. В качестве дополнительного высокоинформативного метода интраоперационного контроля можно использовать внутрисосудистое УЗИ.
Выполнение венозной тромбэктомии рекомендуют проводить в условиях общей анестезии. Безусловно, подобное хирургическое вмешательство может быть выполнено опытным, хорошо подготовленным персоналом.
Хирургические вмешательства при илеофеморальных и бедренно подколенных флеботромбозах
Уровень тромбоза ниже общей подвздошной вены позволяет проводить вмешательство без введения в просвет вены катетеров и других травмирующих инструментов.
Принципиально решение проблемы хирургической тромбэктомии из бедренно-подколенного сегмента сегодня рассматривается в двух направлениях: решение вопроса методом переключения флебогемодинамики на глубокую бедренную вену и путем восстановления естественного потока с возможным сохранением клапанного аппарата собственно бедренной и/или подколенной вен. Если наличие эмбологенного тромба в сегменте можно считать абсолютным показанием к активной тактике, то при обтурирующих тромбах вопрос решается с учетом давности процесса. Известно, что эффективная тромбэктомия возможна только при тромбах давностью не более 3—7 сут [Савельев В. С., 2001]. Существует расхожее мнение о том, что следует придерживается осторожной тактики при хирургическом удалении тромбомасс из бедренно-подколенного сегмента, завершая операцию перевязкой или резекцией приустьевого сегмента собственно бедренной вены, оценивая ближайшие результаты как хорошие по отсутствию симптомов хронической венозной недостаточности. Расчет при таком подходе ведется на переключение основного венозного потока на глубокую вену бедра, которая и должна обеспечить устойчивый отток. Однако известно, что последняя только в 38% случаев имеет прямую связь с подколенной веной .
Именно поэтому предложен способ тромбэктомии при лечении эмбологенного флеботромбоза, направленный не только на удаление тромба, но и на сохранение бедренной вены как полноценного органа, включая систему клапанов.
Показано [Кайдорин А. Г., Цыплящук А. В., 2008], что циркулярное выделение вены приводит к выраженному нарушению интрамурального кровообращения и, как следствие, рубцовым изменениям в стенке, клапанной деформации.
Поэтому в ходе доступа из перивенозных тканей выделяется только передневнутренняя стенка вены на протяжении 1— 2 см, по возможности повреждая адвентицию только по линии разреза и не более чем на 1/2 окружности.
На 1—1,5 см выше проекции основания флотирующей части тромба и обязательно выше проксимального клапана бедренной вены в поперечном направлении накладываются П-образные швы-держалки монофиламентной нитью 6/0, между которыми поперечно производится вскрытие просвета вены.
Флотирующая часть тромба при повышении внутрибрюшного давления (натуживании пациента) самопроизвольно вывихивается в рану под давлением обратного тока крови. После получения ретроградного кровотока свободную вену выше места инцизии прижимают мягким тупфером или пальцем.
При адекватном размере флеботомического отверстия, в ряде случаев, выведенный тромб может служить временным тампоном, препятствующим истечению крови в рану.
Затем при помощи интенсивной поступательной компрессии мягких тканей голени и бедра удаляют тромбы из дистальных глубоких вен нижней конечности.
При невозможности полного удаления тромбомасс на всем протяжении вены в обязательном порядке необходимо убедиться и оценить качество антеградного потока через ПКБВ. Последнее необходимо для оценки перспективы сохранения функции клапана. Если добиться антеградного кровотока не удается, а стенка бедренной вены в зоне операции подвержена воспалительным или рубцово-склеротическим изменениям, следует выполнить ее перевязку ниже впадения глубокой бедренной вены, так как высока вероятность ретромбоза.
При адекватном антеградном кровотоке, убедившись в отсутствии подвижных частей тромба, П-образные швы подтягивают, при этом образуется клапаноподобная дубликатура, обеспечивающая временный гемостаз. Также временный гемостаз легко осуществляется пальцевым прижатием выше и ниже флеботомического дефекта (через массу перивазальных тканей.
Вышеуказанная методика тромбэктомии не требует циркулярного выделения вен и артерий, а потому проста технически и занимает меньше времени.
Послеоперационный период
В послеоперационном периоде продолжается парентеральное введение антикоагулянтов. Параллельно подбирают дозу оральных антикоагулянтов до достижения целевого значения МНО (2,0—3,0)
В последующем целесообразно проведение переменной пневмокомпрессии на обеих нижних конечностях. В обязательном порядке назначают ношение компрессионного трикотажа с давлением 30—40 мм рт. ст. на уровне лодыжек. Ношение компрессионного трикотажа позволяет избежать развития тяжелой посттромботической болезни.
Выбор тактики (оценка факторов риска, отбор пациентов)
Одним из значимых факторов, ограничивающих энтузиазм хирургов по отношению к тромбэктомии, является угроза интраоперационной ТЭЛА. Особенно высок этот риск у больных с неокклюзивным характером тромба в подвздошной и нижней полой вене. В связи с этим принципиально важным является знание проксимальной распространенности тромба, что позволит выбрать адекватный метод профилактики ТЭЛА (имплантация кава-фильтра, баллонная окклюзия). Недостатки и противопоказания тромболитической терапии могут быть значительно сокращены при использовании регионарного тромболизиса и уменьшения дозы тромболитика.
Тщательная оценка и анализ факторов риска и сопутствующей патологии позволяет выявить существенную группу больных с илеофеморальным флеботромбозом, которым показана активная хирургическая тактика. Прежде всего в свете стратегии по удалению тромба следует рассматривать пациентов с окклюзивным характером тромба в илеофеморальном сегменте, так как именно у этих больных часто развивается тяжелая инвалидизирующая посттромботическая болезнь.
В Пироговском центре при отсутствии противопоказаний приоритетной является активная хирургическая тактика по отношению к больным с илеофеморальным флеботромбозом. За последние 5 лет было пролечено более 1000 пациентов с тромбозом глубоких вен. На основании этого опыта разработан алгоритм ведения таких пациентов, представленный на рис. 5.8.
Рис. 5.8.
Алгоритм тактики лечения пациентов с илеофеморальным флеботромбозом
Классификация тромбозов
В зависимости от локализации патологического процесса:
Артериальный:
- артерий головного мозга;
- сердца;
- кишечника (мезентериальный тромбоз);
- печени;
- бедренной артерии и других.
Венозный (флеботромбоз):
- вен нижней конечности;
- геморроидального сплетения;
- бедренной и подвздошной вен;
- кавернозного синуса (внутричерепного коллектора венозной крови);
- вен сетчатки глаза.
По тяжести течения заболевания выделяют острый
ー резкая блокада тока крови, и
хронический
ー тромб растет постепенно, ткани успевают приспособиться к этому и компенсировать патологические изменения.
Причины тромбоза в системе верхней полой вены
– в основном те же, что и других венозных тромбозов. Может, также, развиться как осложнение катетеризации вен (кубитальный, подключичный катетер), иногда возникает как следствие длительного сдавления или неудобного положения верхней конечности (например, во сне).
Наиболее часто встречается тромбоз подмышечной или подключичной вены (синдром Педжета-Шреттера). В течение суток возникает отек всей верхней конечности с подушкообразным отеком кисти. Могут быть небольшие распирающие боли. Цвет конечности не изменен, либо слегка цианотичный.
Механизм развития и причины тромбоза
В процессе образования внутрисосудистого тромба есть три патологических звена:
- Нарушение целостности сосудистой стенки. При повреждении внутренней выстилки сосудов активируются ферментные системы, которые запускают процесс свертывания крови.
- Замедление тока крови. Это происходит при нарушении оттока (сдавливании вен, варикозном расширении), длительном отсутствии движения конечностей, сердечной недостаточности.
- Сгущение крови. Обусловлено обезвоживанием, аутоиммунными заболеваниями, химиотерапией, приемом оральных контрацептивов.
Тромб часто образуется на фоне таких болезней:
- атеросклероз;
- сердечная недостаточность;
- аневризмы сосудов и сердца;
- сахарный диабет;
- ожирение;
- переломы костей;
- гормональные нарушения;
- онкологические заболевания.
Эмболия.
Эмболия чаще других ведет к острой окклюзии артерий. Под эмболией понимают попадание в артериальное русло постороннего тела, приводящего к его закупорке. Чаще всего эмболами служат кусочки организованного тромба, скопления жира или газа, другие инородные тела (пластмассовые трубки, металические предметы, пули). Эмболия периферических артерий встречается в 2 раза чаще у женщин, чем у мужчин, что объясняется большей подверженностью женщин ревматизму и большей продолжительностью жизни. Эмболии могут наблюдаться в любом возрасте, но чаще от 40 до 80 лет. Основными источниками эмболии периферических артерий в настоящее время принято считать заболевания сердца (95% всех случаев). При этом более половины из них приходится на атеросклеротические кардиопатии: мерцательная аритмия, инфаркт миокарда, постинфарктный кардиосклероз, аневризмы сердца. Приобретенный порок сердца составляет 40-43% и врожденные пороки 1-2%. При атеросклеротических кардиопатиях тромб обычно локализуется в левом желудочке, а при пороках сердца в левом предсердии или его ушке. Вслед за эмболией артерий развивается острая ишемия конечности или органа, кровоснабжаемых этим сосудистым бассейном. Ее тяжесть будет зависеть от ряда факторов: 1. выраженности окольного кровообращения, 2. продолженного тромбоза, 3. артериального спазма, 4. состояния центральной гемодинамики. Падение внурисосудистого давления до стагнационного уровня приводит к агрегации тромбоцитов и образованию тромбов в системе микроциркуляции. Наступают, как следствие, необратимые изменения в тканях. Позже развивается тромбоз и в более крупных артериях. Разные ткани различаются по толерантности к ишемии. Так в тканях конечностей необратимые изменения при полной ишемии наступают через 6-8 часов, в кишечнике через 2 часа, почках 40-50 минут, в головном мозге через несколько минут.
Клиническое течение и симптоматика эмболии периферических артерий.
Основным симптомом артериальной эмболии является боль в пораженной конечности. Она возникает внезапно и носит сильнейший характер. Иногда больные падают, не выдерживая этой сильной боли. Наряду с болью, больные часто отмечают чувство онемения конечности. При осмотре бросается в глаза изменение цвета кожных покровов конечности: от выраженной бледности до «мраморной» окраски. В поздней стадии ишемии, когда происходит тромбоз венозного русла, окраска кожи становится цианотичной. При сравнительной пальпации заметна разница в кожной температуре, особенно в дистальных отделах конечности. Имеется также расстройство всех видов чувствительности (болевой, тактильной, глубокой). Граница расстройства чувстви-тельности не совпадает с уровнем окклюзии артерии, а находится ниже, что не должно вводить диагноста в заблуждение. Не менее характерным симптомом является нарушение активных движений в суставах конечности, которые различаются по степени от ограничения до полной плегии. В поздней стадии тяжелой ишемии могут отсутсвовать и пассивные движения, обусловленные ригидностью мышц и суставов. Контрактура суставов является неблагоприятным признаком, указывающим на нежизнеспособность конечности. Отсутствие пульса на артериях, расположенных дистальнее от уровня закупорки также один из важных симптомов эмболии. При выраженном отеке конечности иногда возникают затруднения в определении пульса. Замедленное заполнение подкожных вен или симптом «канавки», также указывают на нарушение кровообращения. Иногда отмечается усиленная пульсация на артериях расположенных проксимальнее от окклюзии, определяемая при сравнительной пальпации. В запущенных случаях наблюдается резкая болезненность мышц при пальпации, ригидность и субфасциальный отек. Для оценки тяжести ишемии конечности были предложены различные классификации. Наиболее полно отвечает практическим целям классификация, предложенная В.С.Савельевым с соавторами в 1978 году. Диагноз эмболии магистральных артерий обычно ставится на основании данных физикальных методов. Из дополнительных методов исследования можно указать на ультразвуковые, радиоизотопную и рентгенконтрастную ангиографию. При этом основная цель их применения состоит в том, чтобы установить проходимость артерий, расположенных дистальнее окклюзии. Следует отметить, что из-за спазма как магистральных, так и коллатеральных сосудов, информативность этих методов резко снижается.
Лечение на догоспитальном этапе.
Снятие болей достигается введением наркотиков или анальгетиков. Важным моментом является введение антикоагулянтов (10 тыс. ед. гепарина) для предотвращения продолженного тромбоза. При необходимости назначаются кардиотонические средства. Основным методом лечения эмболии аорты и периферических артерий должен быть хирургический, направленный на восстановление кровотока у всех больных, у которых нет абсолютных противопоказаний к операции.
Хирургическое лечение.
Операцией выбора является эмболэктомия. Наилучшие результаты получаются в ранние сроки (6-8 часов) после развития эмболии. При более поздних сроках возможно развитие необратимых тканевых изменений. Однако сами по себе сроки не определяют показания к операции. Эмболэктомия может быть успешно выполнена даже через несколько несколько суток, если конечность остается еще жизнеспособной.
Тромбозы у детей
Возможные причины образования тромба у детей:
- тромбофилия ー врожденный дефицит антикоагулянтных факторов крови;
- лейкозы, другие онкологические заболевания;
- кожная фульминантная пурпура, синдром диссеминированного внутрисосудистого свертывания (развивается при тяжелых интоксикациях, воспалительных заболеваниях: панкреатит, перитонит и др.);
- наличие антифосфолипидных антител, волчаночного антикоагулянта, других аутоантител (антител к собственным клеткам).
Эпизоды появления тромбов у ребенка должны стать поводом к серьезному обследованию для определения причины.
Факторы риска развития тромбоза
Вероятность развития заболевания повышают такие факторы:
- возраст старше 50 лет;
- ожирение;
- курение, алкоголизм, наркомания;
- неправильное питание;
- малоподвижный образ жизни;
- травмы;
- потребность в частых внутривенных инъекциях и процедурах, связанных с нарушением целостности сосудов (забор крови, гемодиализ, установка венозного катетера) ー повышают риск развития флебита, воспаления венозной стенки.
Меры профилактики
В основе профилактики тромбоэмболии лежит своевременное выявление и лечения заболеваний сердца и сосудов, поэтому мы рекомендуем проходить комплексное обследование не реже одного раза в год.
Также необходимо вести здоровый и активный образ жизни, умеренно занимаясь спортом и придерживаясь принципов здорового питания. В рационе должна преобладать пища растительного происхождения, а вот продукты, содержащие холестерин, желательно исключить.
В летнее время года следует избегать обезвоживания, соблюдая питьевой режим. Вредные привычки, такие как курение, способствуют повышению риска формирования тромбов – откажитесь от них.
Симптомы тромбоза
Клинические проявления этой патологии разнятся в зависимости от локализации.
Симптомы венозных тромбозов
Когда перекрывается вена, затрудняется отток крови, поэтому ткани дальше места закупорки отекают, синеют. Скапливаются продукты жизнедеятельности клеток, потому развивается интоксикация тканей, это сопровождается болью, нарушением чувствительности (ощущение “ползания мурашек”). Если вовремя не вмешаться ткани начинают отмирать.
Симптомы тромбоза вен нижних конечностей:
- отечность ноги, резкое увеличение в размерах, синюшность;
- судороги икроножных мышц;
- постоянная боль в ноге, которая усиливается при ходьбе;
- усиление венозного рисунка на бедре.
Тромбоз кавернозного синуса:
В твердой мозговой оболочке есть каналы, в которые стекается венозная кровь от головного мозга. Закупорка одного из этих синусов ー кавернозного несет опасность, поскольку через него проходит несколько черепно-мозговых нервов и внутренняя сонная артерия. Наиболее частые причины образования тромба кавернозного синуса ー воспалительные заболевания носа, приносовых пазух, кожи лица и головы. Признаки:
- головная боль;
- снижение остроты зрения, двоение в глазах;
- спутанность сознания;
- жар, лихорадка;
- отек век и окологлазной области;
- боль в шее при поворотах и наклонах головы;
- нарушение чувствительности кожи лица.
Среди последствия такого тромбоза: инсульт, потеря зрения, кома.
Геморроидальный тромбоз
Развивается на фоне геморроя. Ему способствуют хронические запоры, физическое перенапряжение, беременность и роды, злоупотребление алкоголем. Признаки:
- боль, жжение и зуд в области анального сфинктера;
- выделение крови с калом и независимо от акта дефекации;
- выпадение геморроидальных узлов.
Тромбоз сосудов сетчатки глаза
Патология является типичным осложнением сахарного диабета и гипертонической болезни, но может развиваться и по другим причинам. Симптомы:
- ухудшение зрения, вплоть до полной потери (чаще одностороннее);
- появление пятен, сетки, пелены перед глазами.
Симптомы артериальных тромбозов
Закупорка артерии приводит к кислородному и энергетическому голоданию тканей, что быстро приводит к их отмиранию. Артериальные формы заболевания чаще бывают острыми.
Тромбоз артерий головного мозга
Этот процесс ведет к некрозу участка мозга, который кровоснабжает пораженная артерия ー ишемическому инсульту. Признаки:
- гемипарез ー отсутствие движений в правой или левой половине тела (противоположной зоне поражения);
- асимметрия улыбки ー один угол рта опущен, не принимает участие в разговоре и улыбке;
- неясность речи;
- когда больной высовывает язык, он отклоняется в сторону.
Тромбоз коронарных артерий сердца
Частичная закупорка этих сосудов приводит к приступам стенокардических болей, полная ー к инфаркту миокарда. Симптомы:
- давящая, жгучая боль за грудиной, отдает в левую лопатку, руку, плечо, половину лица и шеи;
- одышка;
- при стенокардии помогает покой и нитроглицерин, при инфаркте улучшения не наступает, необходима срочная медицинская помощь.
Тромбоз легочной артерии
Является осложнением тромбоза вен нижних конечностей, эндокардита, инфаркта миокарда. Развивается стремительно, имеет высокую летальность. Признаки:
- острая колющая боль в груди;
- набухание вен шеи;
- одышка, ощущение нехватки воздуха;
- кровохарканье;
- учащение сердечных сокращений.
Тромбоз печеночной артерии
Отмирание (инфаркт) тканей печени является осложнением эндокардита, инфаркта миокарда или пересадки печени, проявляется так:
- сильная боль под правым ребром;
- тошнота, рвота, горечь во рту;
- желтушность кожных покровов и белков глаз.
Тромбоз бедренной артерии
Эта форма патологии проявляется болью при ходьбе, похолоданием, побледнением конечности. Пульс в подколенной ямке и на стопе прощупывается слабо или не определяется вовсе.
Терапевтическая тактика
При обнаружении поражений брахиоцефальных сосудов, специалисты традиционно избирают консервативную тактику лечения. Она предполагает прием определенных медикаментозных препаратов (антикоагулянтов или антиагрегантов), витаминотерапию, диетотерапию. Пациенту даются подробные рекомендации относительно коррекции образа жизни и питания. Он обязан контролировать уровень холестерина в крови, а также следить за состоянием и стабильностью артериального давления.
Хирургическое вмешательство как лечебная тактика избирается в условиях прямой угрозы инсульта. При отсутствии насущного риска, больного ставят на учет и наблюдают.
Оперативное вмешательство бывает:
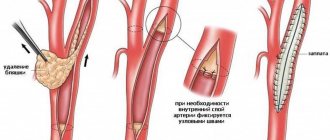
- Открытым (резекция пораженного артериального участка с его немедленным протезированием или сшиванием);
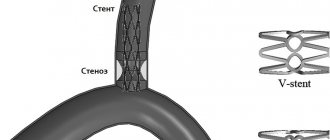
- Эндоваскулярным (внедрение в сосуд стента).
В категорию открытых вмешательств включают эндартерэктомию (эверсионную каротидную).
Стентирование является более современным, атравматичным и эффективным методом, однако он приемлем и показан не в каждом случае. Чем позднее вы обратитесь за профессиональной медицинской помощью, тем меньше ваши шансы излечиться подобными способами.
Заболевания брахиоцефальных артерий – это серьезное нарушение, ведущее к непредсказуемым последствиям. Призываем вас своевременно обращаться к сосудистым хирургам с тревожными симптомами, чтобы избежать необходимости агрессивного лечения и сохранить свою жизнь.
Диагностика и лечение тромбозов в Медицинском
Специалисты медицинского центра “Парацельс” помогут в диагностике и устранении этой патологии, обеспечат поддержку в реабилитационном периоде, дадут рекомендации по дальнейшей профилактике.
В нашем центре для диагностики и лечения применяется оборудование экспертного класса ведущих мировых производителей. Приём ведут практикующие хирурги-флебологи.
На базе «Операционной №1» проводятся флебологические операции при заболевании вен. Ключевое преимущество сети Медицинских центров “Парацельс”— это высококвалифицированные профессионалы-хирурги с огромным практическим опытом.
Медикаментозное лечение
Основу лекарственной терапии составляют антикоагулянты (разжижают кровь, препятствуют увеличению тромба), фибринолитики и тромболитики (растворяют уже имеющиеся сгустки), антиатеросклеротические препараты (снижают уровень холестерина). При необходимости как симптоматическая терапия могут понадобиться анальгетики, противовоспалительные, кардиотонические средства, витамины, минералы и прочее.
Хирургическое лечение
Существуют такие способы оперативного лечения заболевания:
- тромбэктомия ー удаление тромба;
- стентирование (расширение при помощи каркаса) и шунтирование (создание обходного пути кровотока) при атеросклеротическом поражении артерий;
- артериовенозное шунтирование.
Если тромб удалить не удается, можно установить кава-фильтр ー приспособление помещается в вену выше уровня закупорки, чтобы не дать ему сместиться и закрыть просвет сосудов жизненно важных органов.
Типичные признаки и симптомы
Симптоматика заболеваний брахиоцефальных артерий специфична. Если вы чувствуете тревожные симптомы, но ваш врач, выслушав жалобы, ограничился беспредметными диагнозами (СХУ, ВСД и др.), непременно настаивайте на расширенной диагностике.
К симптомам заболеваний брахиоцефальных артерий относят:
- Общую усталость, слабость, снижение работоспособности и концентрации внимания;
- Резкие головные боли, возникающие при движениях головой;
- Головокружения и синкопе (кратковременные потери сознания);
- Обморочные состояния при снижении артериального давления;
- Шум или звон в ушах;
- Преходящие парезы головы и конечностей;
- Зрительные нарушения (появление пятен и мушек в поле зрения, снижение его остроты с внезапным восстановлением);
- Стенокардию;
- Ишемию (иногда бессимптомную);
- Зуд, онемение, покалывание в левых конечностях;
- Покачивание при ходьбе;
- Тошноту;
- Редкие или частые расстройства двигательных или речевых функций (оцепенение, неспособность внятно вести диалог).
Коварство атеросклероза брахиоцефальных артерий заключается в его «размытом» раннем течении. Перечисленные признаки порой вовсе не дают о себе знать, либо выражены настолько слабо, что больной не придает им должного значения. Игнорирование диагностики и лечения приводит к летальному исходу или вегетативному состоянию.