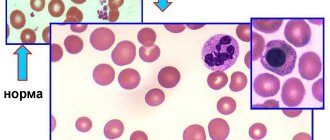
Апластическая анемия – серьёзное нарушение формирования, развития и созревания клеток крови. Оно характеризуется угнетением кроветворной функции костного мозга, что проявляется дефицитом образования белых и красных кровяных клеток, а также тромбоцитов. Иногда наблюдается недостаток формирования только эритроцитов. Заболевание считается одним из самых тяжёлых расстройств гемопоэза и при отсутствии адекватного лечения может стать причиной летального исхода в течение нескольких месяцев. Оно в одинаковой степени поражает пациентов мужского и женского пола в возрасте от десяти до двадцати пяти лет или старше пятидесяти. Согласно медицинской статистике каждый год диагностируют два случая патологии на один миллион человек.
Пройти диагностику и лечение апластической анемии в Москве предлагает отделение гематологии ЦЭЛТ. Наша многопрофильная клиника одна из первых в РФ начала деятельность на рынке платных медицинских услуг и успешно продолжает её уже третье десятилетие. В отделении гематологии ведут приём ведущие отечественные специалисты, в арсенале которых имеется современная лечебно-диагностическая база, позволяющая точно ставить диагноз и проводить лечение в соответствии с международными стандартами. Стоимость услуг доступна в нашем прайс-листе, который мы регулярно обновляем. Во избежание недоразумений просим Вас уточнять цифры у операторов нашей информационной линии.
Апластичная анемия: этиология
Согласно происхождению, выделяют врождённую и приобретённую анемию. Первая развивается вследствие хромосомных мутаций, вторая – под воздействием химических веществ, излучения, инфекций. Специалисты считают, что угнетение кроветворения костного мозга может быть инициировано появлением в нём и в крови цитотоксических Т-лимфоцитов. Они производят ФНО (внеклеточный белок) и интерферон “y”, которые подавляюще воздействуют на ростки кроветворения. Причина запуска механизма может крыться в:
- Воздействии ионизирующего излучения или химических веществ в виде ароматических соединений, мышьяка, пестицидов;
- Попадании в организм инфекционных агентов (возбудители гепатитов “D”, “B”, цитомегаловируса, ДНК-содержащего вируса Эпштейна-Барр);
- Приёме миелотоксических препаратов при прохождении курса лечения транквилизаторами, противосудорожными, антитиреоидными и антиопухолевыми средствами;
- Развитии ряда аутоиммунных процессов (красная системная волчанка, поражение соединительной ткани – синдром Шегрена).
В 50% случаев причину развития патологии установить не удаётся. Такая форма апластической анемии называется идиопатической.
Общая характеристика недуга
Гипопластические анемии характеризуются дисфункцией костного мозга, в результате чего нарушаются процессы его самовосстановления, что приводит к повреждению ростков кроветворения. Сниженное содержание тромбоцитов, лейкоцитов, эритроцитов сопровождается нарушением их созревания на различных этапах формирования.
Заболеванию подвержены лица молодого возраста, преимущественно женщины и подростки
Характерным признаком патологии является полное истощение костного мозга на последних стадиях, а также выраженное нарушение его функций.
Симптоматика проявляется выраженной анемией, тромбоцитопенией, лейкопенией. При отсутствии лечения патология быстро прогрессирует, что может привести к летальному исходу.
Классификация апластической анемии
| Форма патологии | Чем отличается? |
| По продолжительности течения | |
| Острая | Не более одного месяца |
| Подострая | От одного месяца до полугода |
| Хроническая | Более полугода |
| По степени тяжести при избирательной аплазии | |
| Умеренная | Гранулоцитов менее 0,0х109/л, тромбоцитов менее 20,0х109/л. |
| Тяжёлая | Гранулоцитов менее 0,5х109/л, тромбоцитов менее 20,0х109/л. согласно результатам диагностики клеточность костного мозга составляет менее трети от нормы. |
| Очень тяжёлая | Гранулоцитов более 0,5х109/л, тромбоцитов более 20,0х109/л. |
Диагностические показатели
Для подтверждения диагноза «гипопластической анемии» пациенту необходимо пройти множество исследований, которые смогут подтвердить наличие нарушения процесса кроветворения. Отличительной чертой данного вида анемии является то, что селезенка и лимфатические узлы не увеличиваются.
Выраженный геморрагический синдром сопровождается развитием гипохромной анемии
Лабораторная и инструментальная диагностика определяют следующие изменения:
- Клинический анализ крови (сниженный уровень красных тел, гемоглобина, лейкоцитопения).
- Биохимия крови (повышенная концентрация сывороточного железа, повышение насыщаемости железа трансферином).
- Миелограмма (уменьшение клеточных элементов эритроцитов, гранулоцитов, дисплазия ростков гомепоэза).
Апластическая анемия: симптомы
Заболевание начинается остро, оно сопровождается ощущением сильной слабости и быстрой утомляемостью. Кожные покровы больного и видимые слизистые оболочки выглядят бледными, а сам он страдает от следующих клинических проявлений:
- шум в ушах;
- появление одышки даже при несущественных усилиях;
- неприятное покалывание в области грудной клетки.
При снижении количества тромбоцитов в единице объёма крови проявляется геморрагический синдром:
- даже после незначительной компрессии или ударах кожного покрова на нём появляются синяки и кровоизлияния;
- на теле, руках и ногах можно увидеть сыпь в виде мелких точек;
- наблюдается кровоточивость дёсен;
- спонтанные кровотечения из носа;
- обильные менструации (у женщин).
Снижение количества лейкоцитов в единице объёма крови характеризуется регулярным частым развитием инфекционных заболеваний кожи и структур мочевыводящей системы, воспалительными процессами слизистой оболочки рта, воспалениями лёгких.
Врождённая форма анемии развивается у детей до десяти лет и сопровождается целым рядом других нарушений:
- недоразвитие черепа и головного мозга;
- снижение размеров и массы почек (гипоплазия);
- интенсивная окраска отдельных участков кожи – гиперпигментация;
- сильное снижение слуха и нарушения речевой функции из-за него.
Механизм развития
Механизм развития гипопластической анемии связан с действием провоцирующих факторов на систему кроветворения. Патологические изменения приводят к замедлению процесса размножения форменных элементов до их полного исчезновения.
Прогрессирование патологического процесса приводит к замещению тканей костного мозга жировыми клетками
При данном типе анемии наблюдается нарушение обмена железа в результате усиленного разрушения эритроцитов и изменения порфиринового обмена. Далее происходит снижение утилизации железа и его отложение в тканях и органах, что приводит к возникновению вторичного гемохроматоза.
В формировании недуга выделяют несколько механизмов:
- поражение стволовых клеток костного мозга;
- нарушение клеточного и гуморального механизма;
- дисфункция элементов стромы костного мозга;
- недостаток факторов, стимулирующих процесс кроветворения.
Кроме этого, механизм возникновения патологии может быть связан с образованием антител, действующих на выработку форменных элементов крови в костном мозге.
Апластическая анемия: диагностика
Перед тем, как приступить к лечению заболевания, гематологи ЦЭЛТ проводят комплексную диагностику, направленную на точную постановку диагноза и выявление этиологического фактора. Она включает в себя:
- осмотр у гематолога;
- общий и биохимический анализы крови;
- забор образца костного мозга и его исследование – стернальная пункция.
При наличии заболевания у пациента выявляют серьёзное снижение гемоглобина, вплоть до критического уровня – 20-30 г/л, наблюдается агранулоцитоз – снижение зернистых лейкоцитов и моноцитов. Количество лимфоцитов может быть в норме или сниженным, тромбоцитов – всегда снижено, иногда их не обнаруживают вовсе. Скорость оседания эритроцитов – повышается до 4-60 мм/ч. Исследование образца костного мозга выявляет повышенное содержание жировой ткани – 90%, включающее в себя элементы стромы и лимфы, а вот гематогенные клетки имеются в очень малом количестве.
Причины развития
Гипопластическая анемия может быть обусловлена негативным действием различных факторов, их совокупность способствует не только развитию болезни, но и приводит к усугублению течения патологического процесса.
Очень часто данный вид анемии возникает вследствие токсического действия некоторых медикаментов, способных спровоцировать нарушения в костном мозге с дальнейшей дисфункцией ростков кроветворения. Ее формирование не зависит от дозировки медикаментов и от длительности терапевтического курса.
К препаратам, способным вызвать нарушения в системе кроветворения, относят:
- сульфаниламиды,
- антибиотики,
- антигистаминные,
- тетрациклины.
Очень часто недуг определяют у лиц, длительно принимающих Левомицетин
Нарушение гемопоэза наблюдается после курса химиотерапии, так как токсическое действие препаратов разрушает не только патологические образования, но и здоровые клетки и ткани.
Причинами расстройства кроветворной функции также являются аутоиммунные болезни, при которых иммунный механизм направлен на угнетение не только патогенных микроорганизмов, но и на собственное повреждение элементов костного мозга.
Таким образом, различают три группы основных причин, вызывающих нарушение кроветворной функции костного мозга:
- Наследственная. Передача генетически модифицированных генов, проявляющаяся хромосомными аномалиями.
- Основная. Токсическое воздействие химиопрепаратов, радиационное излучение, отравление мышьяком и бензолом.
- Редкая. Формируется на фоне приема некоторых медикаментов, при инфицировании грибком.
Факторы, провоцирующие развитие заболевания:
- гепатит вирусного происхождения;
- вирус герпеса;
- цитомегаловирусная инфекция;
- ВИЧ-инфекция.
Ионизирующее излучение, применяющееся в ходе рентгенологического исследования, играет важную роль в механизме формирования анемии. Чаще всего данная патология встречается у работников рентгенологических кабинетов, а также у пациентов, прошедших курс радиоволновой терапии.
Лечение апластической анемии
Лечение идиопатической и других видов апластической анемии – очень сложная задача, требующая комплексного индивидуального подхода. При разработке тактики специалисты ЦЭЛТ учитывают результаты диагностики и показания пациента. Больного помещают в изолятор с асептическими условиями, что позволяет исключить риск развития инфекций и их осложнений. Медикаментозная терапия заключается в приёме:
- Глюкокортикоидов – при выявлении аутоиммунных механизмов и формировании антител против собственных кровяных клеток;
- Цитостатиков – при отсутствии эффекта от лечения глюкокортикоидами при аутоиммунной анемиии;
- Циклоспорина «А» – для подавления производства ФНО и интерферона “y”;
- Анаболиков – для стимулирования функции кроветворения;
- Андрогенов – для стимулирования образования красных кровяных клеток.
Всем больным апластической анемией проводят переливание эритроцитарной и/или тромбоцитарной массы, в объёмах, определяемых исходя из клинической картины и показателей периферической крови. Кроме того, пациенту могут назначить спленэктомию – хирургическое вмешательство, направленное на удаление селезёнки. Самые благоприятные прогнозы может обеспечить трансплантация костного мозга. Она заключается в пересадке донорских или собственных стволовых кроветворных клеток, предварительно изъятых из подвздошных костей путём пункции. К сожалению, процедура недоступна для широкого применения из-за сложности подбора совместимого донора. В том случае, если это невозможно, пациенту назначают паллиативную терапию с применение циклоспорина А.
В отделении гематологии нашей клиники ведут приём кандидаты, доктора и профессоры медицинских наук с опытом практической и научной работы от двадцати пяти лет. Вы можете записаться к ним на приём онлайн или обратившись к нашим операторам. Специалисты высокой квалификации работают и в отделении урологии. К ним можно записаться на цистоскопию мочевого пузыря.
В ЦЭЛТ вы можете получить консультацию гематолога.
- Первичная консультация — 3 500
- Повторная консультация — 2 300
Записаться на прием
Записавшись на прием гематолога, вы сможете получить всестороннюю консультацию. В компетенции врача находится лечение различных заболеваний крови, большинство из которых можно выявить на ранних стадиях и назначить своевременное лечение, позволяющее справиться с болезнью быстро и легко.
Особенности течения патологии при беременности
Сочетание беременности с гипоапластической анемией встречается довольно редко. В случае возникновения патологии прогноз для беременной неблагоприятный, поскольку в большинстве случаев он заканчивается летальным исходом.
Особенно неблагоприятное течение имеет анемия, сформировавшаяся в период вынашивания ребенка. Как правило, она выявляется во втором триместре, сопровождаясь стремительным ухудшением гематологических показателей и присоединением инфекционных заболеваний. Прерывание течения беременности не останавливает развитие патологических процессов в организме. Лечебные мероприятия не приносят результатов.
При наличии адаптационных механизмов в организме женщины к нарушению гомепоэза возможно сохранение беременности
Беременность, которая образовалась на фоне гипопластической анемии, вызывает ее обострение. В данном случае необходимо срочное диагностирование нарушенного кроветворения с дальнейшим прерыванием беременности на раннем сроке и удалением селезенки.
Выявление анемии на позднем сроке беременности требует индивидуального подхода в вопросах родоразрешения. Оно может быть произведено как путем кесарева сечения, так и с сохранением беременности до начала самопроизвольного выкидыша.
Описаны случаи благоприятного исхода родоразрешения, однако у ребенка диагностировалась железодефицитная анемия на протяжении нескольких месяцев.