Гипертрофия миокарда левого желудочка (ГЛЖ), как элемент его структурной перестройки, считается признаком морфологического отклонения от нормы, ярким предиктором неблагоприятного прогноза вызвавшего его заболевания, а так же критерием, определяющим выбор активной тактики лечения [28]. За последние двадцать лет были проведены клинические исследования, доказавшие независимый вклад медикаментозного уменьшения массы миокарда ЛЖ (ММЛЖ) у больных артериальной гипертонией (АГ), что делает необходимым определение и контролирование ММЛЖ [18 ]. На основе этих представлений рекомендации последних лет по диагностике и лечению АГ включают в алгоритм антигипертензивной тактики ведения пациентов измерение ММЛЖ с целью определения наличия ГЛЖ [4, 35].
Но все же однозначное представление о патогенности ГЛЖ отсутствует, что связано с взаимосвязанными проблемами как методического, так и методологического порядка: Первые касаются достоверности методик определения ММЛЖ, вторые — оценки полученных результатов с точки зрения наличия или отсутствия ГЛЖ. Кроме того, существует многочисленность и инструментальных подходов к определению ММЛЖ.
При измерении ММЛЖ исследователи сталкиваются с многофакторностью, оказывающей не неё влияние. Это — и зависимость ММЛЖ от размеров тела, и возможность лишь адаптивного увеличения ММЛЖ, например, при физической активности. Имеет место и разная чувствительность инструментальных методов определения ММЛЖ: некоторые авторы склоняются к большей чувствительности МРТ измерения [1, 3].
Все Эхо-кг вычисления ММЛЖ, основанные на определении разницы объемов ЛЖ по эпикарду и эндокарду, умноженной на плотность миокарда, сталкиваются с проблемами определения границ раздела тканей и оценки формы левого желудочка. При этом многие методы основаны на линейных измерениях в М-режиме под контролем В-режима, либо непосредственно в двухмерном изображении [24]. Существовавшая ранее проблема идентификации границ раздела тканей, таких как «перикард-эпикард» и «кровь-эндокард», в последние годы, в общем, разрешена, но требует критического отношения к исследованиям прошлых лет и не освобождает исследователей от необходимости использования всех технических возможностей УЗ-сканеров.
Индивидуальные же различия геометрии ЛЖ препятствует созданию универсальной его математической модели даже в отсутствии локальных нарушений структуры ЛЖ и приближением его формы к эллипсу, что породило большое количество формул, а, следовательно, критериев определения ГЛЖ, следствием чего являются разные выводы о наличии гипертрофии у одного и того же пациента.
Кроме того, в настоящее время пользуются несколькими расчетными формулами определения ММЛЖ. Чаще применяются формулы рекомендованные American Society of Echocardiography (ASE) и Penn Сonvention (PC), использующие три измеренных параметра: толщину миокарда межжелудочковой перегородки (МЖП), задней стенки ЛЖ (ЗСЛЖ) в конце диастолы и его конечно-диастолический размер (КДР) с включением (формула ASE) или не включением толщины эндокарда (формула PC) в диаметр левого желудочка в зависимости от используемой формулы. Но результаты, полученные при применении этих формул не всегда сопоставимы, поэтому для интерпретации получаемых данных необходимо уточнение используемого метода расчёта параметров левого желудочка, которое на практике не всегда доступно или которым пренебрегают. Причина расхождения кроется в следующем. Кубическая формула, изначально рекомендуемая ASE, была предложена B.L. Troy и соавторами в 1972 г. (ММЛЖ, гр = [(КДР+МЖП+ЗСЛЖ) 3 -КДР 3 ]×1,05) [37], а затем модифицирована с использованием уравнения регрессии R.B. Devereux и Reichek в 1977 г. (формула Penn Сonvention) путем анализа взаимоотношений между эхокардиографической ММЛЖ и посмертной анатомической массой ЛЖ у 34 взрослых лиц (r=0,96, р 3 -КДР 3 ]-13,6) [16].
Расхождения значений рассчитанной ММЛЖ, полученные при использовании этих двух формул (кубической, предложенной B.L. Troy, и формулой PC) были в пределах 20% и в 1986 г. R.B. Devereux, D.R. Alonso at.all. на основе аутопсии 52 пациентов предложили скорректированное уравнение (ММЛЖ, гр = 0,8×<1,04×[(КДР+МЖП+ЗСЛЖ) 3 -КДР 3 ]>+0,6 — формула ASE). ММЛЖ, определенная по формуле PC тесно коррелировала с ММЛЖ при аутопсии (r=0,92; p 215 гр.) составила 100% при специфичности 86% (у 29 из 34 больных). Кубическая формула аналогично коррелировала с ММЛЖ при аутопсии (r=0,90; p 3 )/2,4+КДР+ТЗСЛЖ+ТМЖП)-((7×КДР 3 )/(2,4+КДР))) [36]. Согласно L. Teiсholz, нормой является ММЛЖ 200 гр — выраженной ГЛЖ. Однако, данные параметры могут быть ориентирами лишь при использовании формулы Teiсholz и, кроме того, они не учитывают соотношение ММЛЖ с размерами тела.
Виртуальный расчет ММЛЖ по трем вышеназванным формулам при стабильном значении одного из параметров (либо суммы толщины МЖП и ЗСЛЖ, либо КДР) и увеличении другого (либо КДР, либо суммы толщины МЖП и ЗСЛЖ соответственно) на стабильную произвольную величину, показали разную чувствительность формул к изменяющемуся линейному показателю [23]. Оказалось, что формула ASE более чувствительна к увеличению толщин стенок миокарда, формула Teiсholz — к увеличению полости ЛЖ, а формула PC — паритетно учитывает изменения линейных размеров и толщины миокарда и полости. Таким образом, оценивать ММЛЖ за счёт изменения толщины миокарда лучше используя более чувствительные в этом отношении формулы — ASE и PC.
Второй проблемой, кроме определения ММЛЖ, является отсутствие унифицированных критериев её индексации, а, следовательно, и формирования критериев ГЛЖ. Определение размеров органов через аллометрические зависимости их от массы тела, принятые в сравнительной морфологии, неприемлемо в человеческой популяции по причине вариабельности массы тела индивидуума, зависящей от многих факторов, в частности от конституциональных особенностей, физического развития, а также возможного изменения размеров органа в результате заболевания [5].
Наличие же прямой зависимости ММЛЖ от размеров тела требует её индексации. В этой связи чаще рассчитывают индекс массы миокарда левого желудочка (ИММЛЖ) при стандартизации к площади поверхности тела (ППТ). Есть еще несколько способов расчета индекса массы миокарда: по росту, росту 2,0 , росту 2,13 , росту 2,7 , росту 3,0 ; коррекции с помощью регрессионной модели ММЛЖ в зависимости от возраста, индекса массы тела и ППТ [7].
Исследования прошлых лет доказывают влияние различных факторов на массу миокарда в разных возрастных группах. Так, в раннем детском возрасте вес миокарда ЛЖ в основном определяется количеством кардиомиоцитов (КМЦ), которые достигают максимального числа в течении первого года жизни [31], в дальнейшем рост ЛЖ зависит уже от увеличения размеров КМЦ (физиологическая гипертрофия) и на этот физиологический процесс оказывают влияние многие факторы — размер тела, АД, объем крови, генетические факторы, потребление соли, вязкость крови [8, 10, 33, 38], которые и определяют фенотипический рост массы ЛЖ. После же полового созревания уже другие факторы определяют степень физиологической гипертрофии, при этом у взрослых прослеживается связь ММЛЖ с возрастом [12]. Влияние роста на изменчивость ММЛЖ было изучено de G. Simone с соав. и в 1995 г. на 611 нормотензивных лицах с нормальной массой тела в возрасте от 4 месяцев до 70 лет (из них, детей 383 и 228 взрослых пациента). ММЛЖ нормировали к массе тела, росту, ППТ. Индексированная к росту 2,7 ММЛЖ увеличивалась с увеличением роста и возраста у детей, но не у взрослых, что свидетельствовало о влиянии других переменных на массу ЛЖ во взрослом состоянии [11].
Причины отклонения массы и индекса массы сердца от нормальных цифр
Масса миокарда увеличена при патологических процессах, приводящих к его перегрузке:
Возрастание массы мышечной ткани происходит и в норме — при усиленных физических тренировках, когда интенсивные занятия спортом вызывают наращивание не только скелетной мускулатуры, но и миокарда, обеспечивающего органы и ткани тренирующегося богатой кислородом кровью.
Спортсмены, однако, рискуют со временем перейти в разряд людей с гипертрофией миокарда, которая при определенных условиях может стать патологической. Когда толщина сердечной мышцы станет больше, чем коронарные артерии способны обеспечить кровью, есть риск появления сердечной недостаточности. Именно с этим явлением наиболее часто связывают внезапную смерть у хорошо тренированных и внешне вполне здоровых людей.
Таким образом, увеличение массы миокарда, как правило, говорит о высокой нагрузке на сердце, будь то при спортивных тренировках или патологических состояниях, но независимо от причины гипертрофия сердечной мышцы заслуживает пристального внимания.
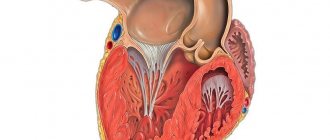
Характеристики миокарда и методы их расчета
Миокард представляет собой мышечный слой сердца, который состоит из одноядерных клеток, имеющих особое поперечное расположение. Благодаря этому обеспечивается чрезвычайная прочность мышцы и способность к равномерному распределению работы по всему сердцу. Взаиморасположение клеток по типу вставочных дисков определяет необыкновенные свойства миокарда. К ним относятся возбудимость, сократимость, проводимость, расслабление и автоматизм.
Оценить, здорово ли сердце, возможно с помощью дополнительных инструментальных обследований. Нормальные показатели по результатам эхокардиографии миокарда желудочков (один из ключевых методов диагностики патологии выброса крови) выглядят следующим образом:
- левый желудочек (ЛЖ): масса миокарда — 135—182 г, 95—141 г; индекс массы (ИММЛЖ) — 71—94 г/м 2 , 71—84 г/м 2 у мужчин и женщин соответственно;
- правый желудочек (ПЖ): толщина стенки — 3 мм; размерный индекс — 0,75—1,25 см/м 2 ; величина диастолы в покое — 0,8—2,0 см.
Левый желудочек берет на себя большую функциональную нагрузку, чем какие-либо другие части сердца, соответственно, чаще подвержен патологическим изменениям. Поэтому его параметры рассмотрим более подробно.
Расчет массы миокарда левого желудочка получают, производя различные вычисления. Калькулятор обрабатывает цифры при помощи специальных формул. На современном этапе наиболее чувствительными признаны 2 формы расчёта, которые рекомендованы American Society of Echocardiography (ASE) и Penn Сonvention (PC). Отличие между ними состоит лишь во включении толщины внутреннего слоя сердца при использовании первой формулы.
Во Фремингемском исследовании впервые было показано, что гипертрофия левого желудочка (ГЛЖ), независимо от уровня АД, является фактором риска внезапной смерти, застойной сердечной недостаточности, желудочковых аритмий, ИБС, инфаркта миокарда, а также смертности от сердечно-сосудистых заболеваний. С помощью эхокардиографии установлено, что повышение массы миокарда на 50 г/м 2 увеличивает относительный риск сердечно-сосудистых заболеваний в 1,73 раза у мужчин и в 2,12 раза у женщин [9]. Относительный риск смерти при увеличении массы миокарда на 100 г возрастает в 2,1 раза. Смертность от сердечно-сосудистых заболеваний у больных с АГ при наличии ГЛЖ в 25 раз выше (15%), чем при ее отсутствии (0,6%) [8].
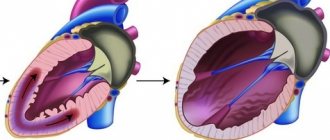
Считается, что ГЛЖ является адаптационным ответом на повышенную гемодинамическую нагрузку или следствием генетического дефекта. Однако, в последнее время стало очевидным, что анатомические изменения ЛЖ не всегда сопровождаются нарастанием массы миокарда. Происходит изменение архитектоники интерстиция миокарда, которое приводит к фиброзу и специфическим морфологическим изменениям или ремоделированию миокарда [2,4,5 ].
По эхоКГ у больных в ответ на увеличение нагрузки на сердце определяются различные изменения формы ЛЖ. За основу классификации принимается определение индекса массы миокарда ЛЖ (ММЛЖ) и относительная толщина стенок ЛЖ (ОТС) [ 3,6 ]. При «чистой» форме перегрузки сердца давлением ГЛЖ чаще имеет концентрический вариант ремоделирования — увеличение ММЛЖ и ОТС >0,45 (КГЛЖ). При перегрузке объемом, как это наблюдается при ожирении, она приобретает эксцентрическую форму — увеличение ММЛЖ и ОТС < 0,45 (ЭГЛЖ). Худший прогноз (смертность 21%, частота других сердечно-сосудистых осложнений — 31%) наблюдался у лиц с концентрической ГЛЖ [ 9 ]. В отсутствие ГЛЖ, но при ОТС ³ 0,45, определяется концентрическое ремоделирование (КР).
В настоящее время патогенетические аспекты развития ГЛЖ при метаболическом синдроме окончательно не установлены. Считается, что в ее возникновении имеют значение несколько факторов. Основное значение имеют систолическое напряжение стенок ЛЖ, увеличение объема циркулирующей крови и ее вязкости, общее периферическое сопротивление. К повышению систолического напряжения стенок ЛЖ, обуславливающего увеличение количества саркомеров в миокарде, приводит в первую очередь перегрузка давлением, характерная для АГ [ 2 ]. Кроме того, при АГ выявлено увеличение толщины интимы периферических артерий, что повышает общее периферическое сопротивление сосудов, постнагрузку на сердце. При ожирении увеличенный ударный объем приводит к повышению сердечного выброса и развивается эксцентрическая ГЛЖ [ 1,7 ]. В случае сочетания АГ и ожирения происходит взаимное усугубление гемодинамических процессов, создается смешанная нагрузка на сердце — увеличивается пред- и постнагрузка. Однако при обеих нозологиях, наблюдается выраженная нейрогуморальная активация симпатической и ренин — ангиотензиновой систем, с выработкой гипертрофических стимулов. Влияние гиперинсулинемии / инсулинрезистентности на ГЛЖ может реализоваться как через прямые гипертрофические эффекты инсулина на мышечную ткань, так и опосредованно [3,7,10].
Выявление ГЛЖ имеет важное клиническое значение, поскольку ее наличие оказывает существенное влияние на характер течения и прогноз заболевания. Очевидно, что ММЛЖ в значительной степени зависит от массы тела, пола, возраста. Поэтому принято индексировать ММЛЖ к площади тела или росту. В последние годы наметилась тенденция к использованию более низких значений ММЛЖ в качестве критерия его гипертрофии [ 6 ].
Воздействие на промежуточные точки в лечении артериальной гипертензии, в частности на ГЛЖ, в последние десятилетия стало одним из ведущих направлений в кардиологии. Имеющиеся данные свидетельствуют о том, что регресс ГЛЖ приводит к двукратному снижению риска смерти [ 5,8 ].
Цель нашей работы: изучить особенности ремоделирования миокарда у больных с метаболическим синдромом и оценить влияние многофакторной терапии на регресс
Материалы и методы
Обследовано 84 человек в возрасте 43-61 год. У всех пациентов имелось абдоминальный тип ожирения- ИМТ > 26 кг/м2, и отношение окружности талии к окружности бедер (ОТ/ОБ) у женщин > 0.85, у мужчин > 0.9. Сахарный диабет (СД) 2 типа имели 59 больных, средняя продолжительность заболевания 6,4±2,2 года. У больных измерялось каузальное давление и проводилось суточное мониторирование (СМАД) с помощью портативных приборов АВРМ-04 (, Венгрия). Деление больных на 5 групп происходило по результатам СМАД. В группы 1 и 4 артериальной гипертензии вошли пациенты с высоким «офисным» АД, которая подтверждалась данными СМАД. Группа 2, обозначенная нами как группа нестабильной артериальной гипертензии, сформирована из больных, указывающих на эпизоды повышенного АД с «офисным» АД более 140/90 мм рт, но по результатам СМАД имеющим среднее суточное САД < 140 мм рт. ст. и среднее ДАД < 90 мм рт. ст. В группы 3 и 5 с нормальным АД вошли больные с АД менее 130/ 85 мм рт.ст. по данным СМАД. Группы 1,2,3 были сформированы из больных сахарным диабетом.
В пробе плазмы крови, взятой натощак, определяли мочевую кислоту, глюкозу, креатинин, липиды плазмы. Содержание инсулина (ИРИ), С-пептида, кортизола определяли методом радиоиммунологического анализа с использованием стандартных тест наборов. «Immunotech» (Чехия). Инсулинрезистентность оценивали с помощью индексов: индекс инсулинрезистентности НОМА (НОМА IR) (тощаковый инсулин Х тощаковая глюкоза / 22.5), индекс функции в-клетки (НОМА b-c) (20 Х тощаковый инсулин / тощаковая глюкоза — 3.5).
Эхокардиографическое исследование проводили на аппарате HP SONOS 4500 в М- модальном и двухмерном режиме в стандартных эхокардиографических позициях. Изучались общепринятые показатели по методике Teicholz. Масса миокарда левого желудочка (ММЛЖ) определялась по Devereux R. и Reicheck N. (1977): ММЛЖ = 1,04 *[( МЖП+ЗСЛЖ+КДР)3 — КДР3 ] — 13,6. Индекс массы миокарда рассчитывался по отношению ММ к площади поверхности тела, к росту и к росту в степени 2.7. Нами взято несколько индексов для определения ГЛЖ. Индексация по площади тела (ИМ/ПТ) у лиц с избыточной массой тела сопровождается недостаточным выявлением случаев ГЛЖ, индекс ИМ /Р (рост) недооценивает частоту встречаемости ГЛЖ у высоких пациентов, в то время как индексация по Р2,7 уменьшает несоответствие между ростом и мало зависит от веса. ГЛЖ фиксировали по известным параметрам и сочетание более 2- х критериев принимали за ГЛЖ..
1. ММЛЖ более 200 грамм;
2.1. ИМ /Р у мужчин.> 163 г/м, у женщин > 121 г/м;
2.2. ИМ /ПТ у мужчин > 134 г/ м 2, у женщин > 110 г/ м 2 ;
2.3. ИМ / РОСТ 2.7 у мужчин > 53 г/м 2.7, у женщин > 47 г/м 2.7
3. толщина МЖП и/или ЗСЛЖ ³ 1,1см.
Статистическая обработка проводилась при помощи статистического пакета Statistica 5.0. Рассчитывались средние значения показателей и стандартное отклонение (M±SD). При сравнении выборок использовали непараметрические критерии U тест Манна -Уитни, ранговый тест Вальд -Вольфовича, тест Колмогорова -Смирнова. Для установления взаимосвязи признаков применяли многофакторный корреляционный анализ с использованием критериев Пирсона и Спирмена. Различия значений и корреляционные связи считали достоверными при р < 0,05. [4]
Результаты
Данные о морфометрических показателях сердца и его сократительной способности представлены в таблице 1.
Таблица 1.
Показатели эхоКГ исследования сердца по группам
| Показатель | 1 группа (n=26) | 2 группа (n=19) | 3 группа (n= 14) | 4 группа (n=15) | 5 группа (n=10) | Р |
| ЛП мл | 3,7± 0,59 | 3,54±0,54 | 3,44± 0,57 | 3,47± 0,64 | 3,43± 0,43 | нз |
| СР мл | 3,23±0,57 | 3,36±0,39 | 3,21±0,48 | 3,2±0,42 | 3,0±0,44 | нз |
| КДР мл | 5,08± 0,44 | 4,96±0,47 | 4,89± 0,35 | 4,84± 0,44 | 4,97± 0,37 | 2-4<0,05 |
| КСО мл | 42,31±13,5 | 45,16±12,2 | 41,75±14,0 | 43,93±13,1 | 35,17±23,2 | 1-3< 0,05 |
| КДО мл | 130,2± 32,8 | 123,0±25,6 | 112,2± 23,4 | 114,31±28,4 | 120,2±23,2 | 1-3< 0,05 |
| УО мл | 81,77± 16,0 | 115,26±16,4 | 71,2± 11,6 | 73,8± 18,1 | 85,3± 13,7 | нз |
| ФВ% | 66,69± 10,3 | 65,95± 9,3 | 61,3± 6,0 | 63,2± 4,4 | 71,5± 5,3 | 1-3<0,005 4-5<0,01 |
| ФУ | 37,66± 8,6 | 48,44± 12,0 | 54,5± 16,5 | 52,15± 10,5 | 67,6± 11,2 | 1-2<0,01 1-3< 0,01 1-4<0,01 4-6< 0,05 |
| МЖП мм | 1,23± 0,13 | 1,31± 0,12 | 0,98± 0,15 | 1,15± 0,17 | 1,07± 0,09 | 1-2< 0,05 1-3< 0,0005 2-3< 0,01 |
| ЗСЛЖ мм | 1,2± 0,14 | 1,11±0,09 | 1,02±0,13 | 1,08±0,17 | 1,03±0,09 | 1-2< 0,05 1-3< 0,001 1-4< 0,05 2-3<0,05 |
| ММЛЖ г | 292,47 ±60,67 | 250,64 ±52,86 | 206,9 ±44,15 | 240,49 ±69,85 | 201,5 ±9,45 | кроме 4-5 |
| ИМ/Р г/м | 179,41 ±39,0 | 150,8 ±30,4 | 130,4 ±25,0 | 148,9 ±44,7 | 118,4 ±3,4 | |
| ИМ/ПТ г/ м 2 | 153,54±37,4 | 128,56±26,5 | 115,96±20,4 | 127,19±37,5 | 95,1 ±4,8 | |
| ИМ/Р2.7 г/м 2.7 | 78,7 ±20,56 | 63,9 ±13,76 | 59,7 ±10,22 | 66,26±21,82 | 48,12 ±3,4 | кроме 1-4 |
Эхокардиографические параметры систолической функции миокарда левого желудочка УО, ФВ, ФУ были не ниже, чем у здоровых, а в группах в основном зависели от степени увеличения АД. При отсутствии различий по величине ударного объема (УО), определялись разнонаправленные значения индексов сократимости. Так, среди больных с нормальным АД, фракция выброса (ФВ) и степень укорочения передне — заднего размера ЛЖ (ФУ) были выше чем у больных АГ. Среди групп СД 2 показатель сократимости — ФУ был ниже в группе АГ, при более высоких значениях ФВ и КДО по сравнению с группой нормального АД. У больных этой группы высокая фракция выброса поддерживалась за счет увеличения объема ЛЖ, но снижение ФУ могло быть свидетельством латентной декомпенсации.
Объемные параметры ЭХО-КГ по группам также зависели от наличия АГ и СД 2. Отсутствовали различия у больных СД 2 и ожирением без АГ (3 и 5 группы) и у больных 2 и 3 групп: СД 2 с нестабильной АГ и с нормальным АД. Особый интерес представляет сравнение 3 и 4 групп, из которого следует, что больные с СД 2 и нестабильной АГ имели такие же параметры внутрисердечной гемодинамики, как и больные АГ и ожирением и, более того, они их превосходили по величине КДР.
Анализ средних величин толщины стенок ЛЖ показал, что в группах 1, 2 и 4, средние показатели толщины ЗСЛЖ и МЖП превышали 1,1 см, что свидетельствовало об их гипертрофии. Показатели структурной характеристики миокарда, толщина стенок ЛЖ были наибольшими у лиц с СД 2 и АГ, даже при сравнении с АГ и ожирением.
Анализ индексов массы миокарда, показал, что индексация по росту 2,7 выявляет больший процент ГЛЖ в группах с ожирением, чем другие. Индекс ММЛЖ к площади тела приводил к занижению количества больных с ГЛЖ примерно на 14%, особенно это проявлялось у больных с ИМТ более 30 кг/м 2.
Обращают внимание показатели 2 и 3 групп. Больные с СД 2 и нестабильной АГ (которые имели нормальные среднесуточные показатели АД) почти в 90% случаев имели ГЛЖ. Более того, частота ГЛЖ в группе больных СД 2 и нормальным АД (где 70% лиц имели оптимальное АД) была такой же, как и у лиц с АГ без СД.
Ремоделирование ЛЖ в целом выявлено у большинства больных (табл.2). Среди больных, страдающих АГ, преобладали больные с концентрической ГЛЖ. У больных СД 2 без АГ процент больных с КГЛЖ и ЭГЛЖ был примерно одинаковым. Стоит отметить, что среди больных СД 2 и нормальным АД количество с ГЛЖ было таким же, как при АГ без СД 2. Следовательно, больные СД 2 в рамках метаболического синдрома имеют высокую распространенность ГЛЖ, вне зависимости от уровня АГ.
Таблица 2.
Характер ремоделирования миокарда в группах
| 1 группа (n=26) | 2 группа (n=19) | 3 группа (n=14) | 4 группа (n=15) | 5 группа (n=10) | |
| ГЛЖ % | 100 | 89,5 | 50 | 46,6 | 10 |
| КГЛЖ % | 65,4 | 52,9 | 42,8 | 85,7 | 100 |
| ЭГЛЖ % | 34,6 | 47,1 | 57,2 | 14,3 | 0 |
| КР % | 0 | 10,5 | 0 | 13 | 37,5 |
| Норма % | 0 | 10,5 | 50 | 40 | 50 |
При сравнении общеклинических характеристик у больных с КГЛЖ по сравнению с ЭГЛЖ отмечалась достоверно выраженная микроальбуминурия (135,8 ± 40,8 мг/с и 29,52 ± 15,7мг/с — р<0,05 соответственно). Группы больных не различались по длительности АГ (6,39±3,9 г и 5,39 ± 5,1 г, соответственно).
При анализе параметров периферической гемодинамики в группах с разным видом ремоделирования миокарда были выявлены более высокие показатели нагрузки давлением у больных с КГЛЖ. Выявлялась высокой степени корреляции между уровнем кортизола и ММЛЖ (r= 0,61; р< 0,05) у больных СД и АГ. Увеличение инсулинрезистентности НОМА IR в группах СД сопровождалось увеличением КДР (r= 0,74; р< 0,05), КДО (r= 0,63; р< 0,05) и ЛП (r= 0,67; р< 0,05). Повышение ИРИ сопровождалось увеличением ММЛЖ как в группах СД, так и без него (от r= 0,31 до r= 0,52 соответственно; р< 0,05).
Корреляционные взаимоотношения между ММЛЖ, ИРИ и показателями СМАД и метаболическими параметрами оказались зависимыми от варианта ремоделирования ГЛЖ. При концентрической ГЛЖ увеличение уровней инсулина и кортизола сопровождалось ростом ММЛЖ (r= 0,38 и 0,44; р< 0,05). Увеличение времени нагрузки давлением (САД, ИВ САД, ИВ ДАД), также способствовало развитию КГЛЖ.
У больных с эксцентрической ГЛЖ масса миокарда зависела от индекса абдоминального ожирения (r= 0,48; р< 0,05). У этих пациентов мы выявили значимую связь уровней ИРИ и мочевой кислоты, холестерина, триглицеридов (r= 0,64; r= 0,66; r= 0,51; р< 0,05).
Анализ полученных данных позволяет сделать вывод, что инсулинрезистентность оказывает влияние на структурно-функциональные параметры сердца, как у больных СД 2, так и при абдоминальном ожирении. Так, выявилась положительная связь уровня ИРИ с ММЛЖ / ИМ как у больных с СД 2, так и без СД. Очевидно также, что инсулинрезистентность оказывала значительное влияние на развитие ГЛЖ, т.е. чем выше инсулинрезистентность, тем больше величина ММЛЖ. Тем не менее, можно определить следующие особенности: у больных СД 2 влияние гиперинсулинемии и инсулинрезистентности определялось в увеличении структурных параметры миокарда — толщину ЗСЛЖ и ММЛЖ, т.е. проявлялся гиперпластический эффект инсулина на орган — мишень. У больных без АГ и СД действие инсулина и ИР проявлялось увеличением объемных показателей полостей миокарда.
Е.Н. Смирнова
Пермская государственная медицинская академия
Литература:
1. Аметов А.С., Демидова Т.Ю., Целиковская А.Л. Ожирение и сердечно-сосудистые заболевания // Тер.архив. — 2001. — №8. — С 66- 69.
2. Мартынов А.И., Остроумова О.Д., Мамаев В.И. и др. Гипертрофия миокарда левого желудочка при артериальной гипертензии: клиническое значение, диагностика, влияние антигипертензивных препаратов // Клиническая медицина. — 2000. — №10. — С. 10-17.
3. Конради А.О., Жукова А.В., Винник Т.А. и др. Структурно — функциональные параметры миокарда у больных гипертонической болезнью в зависимости от массы тела, типа ожирения и состояния углеводного обмена // Артериальная гипертензия. — 2002. — Т.8. — №1. — С.12-15.
4. Шляхто Е.В., Моисеева О.М. Клеточные аспекты ремоделирования сосудов при артериальной гипертензии // Артериальная гипертензия.- 2002.- №2. — С.45- 49.
5. de Simone G.,Palmieri V., Koren M.J. et al. Prognostic implications of the compensatory nature of left ventricular mass in arterial hypertension // J. Hуpertens. — 2001. — V.19. — P.119-126.
6. Gosse P., Jullien P, Jarnier P. et al. Echocardiografic definition of left ventricular hypertrophy in the hypertensive: with method of indexation of left ventricular mass? // J.Hum.Hypertens. — 1999. — V.13. — P.505-509.
7. Iacobellis G., Ribaudo M.C. Correlation between insulin resistance and left ventricular mass in uncomplicated obesity // Diabetologia. — 2001. -V.44. — A.701.
8. Kannel W.B. Left ventricular hypertrophy and regression. London, 1992.
9. Koren M., Devereux R.B., Casale P.N., Savage D.D. et al. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension // Ann. Intern. Med. — 2001. — V.114. — P.345-352.
10. Moller D.E., Flier J. Insulin resistance — mechanisms, syndromes, and implications // N. Engl. J. Med. — 2001. — V.26. — P.938-948.