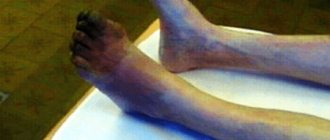
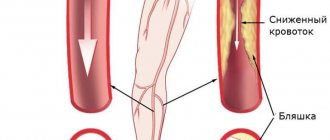
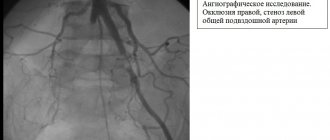
Окклюзия бедренной артерии – это нарушение ее проходимости (закупорка).
В результате окклюзии артериальная, обогащенная кислородом кровь перестаёт поступать в нижнюю часть ноги. Развивается ишемия (местное малокровие).
Окклюзия бедренной артерии наблюдается в основном у мужчин. На лица старше 50 лет приходится до 75% случаев заболевания.
Окклюзия бедренной артерии может быть:
- сегментарной, затрагивающей лишь ограниченный по протяженности участок артерии;
- полной, когда поражается вся артерия;
- сочетающейся с окклюзиями других артерий нижних конечностей.
Причины окклюзии бедренной артерии
Причиной окклюзии бедренной артерии в большинстве (75-80%) случаев является облитерирующий атеросклероз. Атеросклероз – это заболевание, при котором на стенках артерии отлагаются холестериновые бляшки, которые со временем перекрывают просвет сосуда. Также окклюзия бедренной артерии может быть вызвана травмой, тромбом и некоторыми другими причинами.
Факторами, способствующими развитию окклюзии
, являются:
- курение;
- высокое артериальное давление;
- наследственная предрасположенность;
- неправильная диета (жирная пища);
- сахарный диабет.
Диагностика острой окклюзии сосудов конечностей
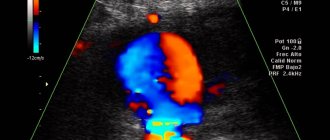
Диагностический алгоритм при подозрении на острую окклюзию сосудов конечностей предусматривает проведение комплекса физикальных, лабораторных, инструментальных исследований. Пальпация пульса в типичных точках (на тыльной артерии стопы, в подколенной ямке, на заднебольшеберцовой и бедренной артерии и др.) выявляет отсутствие пульсации артерии ниже окклюзии и ее сохранение выше участка поражения. Важную информацию при первичном обследовании дают функциональные пробы: маршевая (проба Дельбе-Пертеса), коленный феномен (проба Панченко), определение зоны реактивной гиперемии (проба Мошковича).
Лабораторные исследования крови (коагулограмма) при острой окклюзии сосудов конечностей обнаруживают повышение ПТИ, уменьшение времени кровотечения, увеличение фибриногена. Окончательная диагностика острой окклюзии сосудов конечностей и выбор лечебной тактики определяются данными УЗДГ (дуплексного сканирования) артерий верхних или нижних конечностей, периферической артериографии, КТ-артериографии, МР-ангиографии.
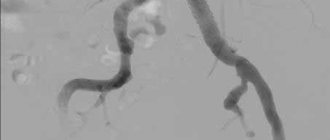
КТ-ангиография брюшной аорты и ее ветвей. Полная окклюзия просвета левой внутренней подвздошной артерии
Дифференциальная диагностика проводится с расслаивающейся аневризмой брюшной аорты и острым тромбофлебитом глубоких вен.
Методы лечения окклюзии бедренной артерии
При ограниченной окклюзии организм может компенсировать кровообращение конечности с помощью кровотока по боковым ветвям артериальной системы (коллатерального кровообращения). В этом случае возможно консервативное лечение.
При нарастании тяжести ишемических симптомов, перемежающейся хромоте возникающей менее через 100 метров ходьбы, болей в состоянии покоя необходимо прибегнуть к хирургическому лечению. Подобные симптомы означают, что компенсация кровообращения недостаточна, а это грозит развитием язвенно-некротических изменений, гангреной и потерей конечности.
Хирургическое лечение
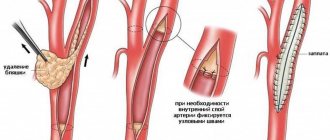
При хирургическом лечении окклюзии в зависимости от области поражения артерии используются:
- эндартерэктомия (удаление атеросклеротических отложений из просвета артерии);
- бедренно-подколенное шунтирование;
- бедренно-берцовое шунтирование (если есть сопутствующая окклюзия подколенной артерии).
Записаться на прием Не занимайтесь самолечением. Обратитесь к нашим специалистам, которые правильно поставят диагноз и назначат лечение.
Оцените, насколько был полезен материал
Спасибо за оценку
Симптомы окклюзии сосудов
Острая окклюзия сосудов конечностей проявляется симптомокомплексом, обозначаемым в англоязычной литературе как «комплекс пяти P» (рain – боль, рulselessness — отсутствие пульса, рallor – бледность, рaresthesia – парестезии, рaralysis – паралич). Наличие хотя бы одного из этих признаков заставляет думать о возможной острой окклюзии сосудов конечностей.
Внезапная боль дистальнее места окклюзии возникает в 75-80% случаев и обычно служит первым признаком острой окклюзии сосудов конечностей. При сохранности коллатерального кровообращения боль может быть минимальной или отсутствовать. Чаще боль носит разлитой характер с тенденцией к усилению, не стихает при изменении положения конечности; в редких случаях спонтанного разрешения окклюзии боль самостоятельно исчезает.
Важным диагностическим признаком острой окклюзии сосудов конечностей является отсутствие пульсации артерий дистальнее места окклюзии. При этом конечность вначале бледнеет, затем приобретает цианотический оттенок с мраморным рисунком. Кожная температура резко снижена – конечность холодная на ощупь. Иногда при осмотре выявляются признаки хронической ишемии – морщинистость и сухость кожи, отсутствие волос, ломкость ногтей.
Расстройства чувствительности и двигательной сферы при острой окклюзии сосудов конечностей проявляются онемением, ощущением покалывания и ползания «мурашек», снижением тактильной чувствительности (парестезиями), снижением мышечной силы (парезом) или отсутствием активных движений (параличом) сначала в дистальных, а затем в проксимальных суставах. В дальнейшем может наступить полная обездвиженность пораженной конечности, что указывает на глубокую ишемию и является грозным прогностическим признаком. Конечным результатом острой окклюзии сосудов может стать гангрена конечности.
Облитерирующие заболевания аорты и артерий нижних конечностей
Х
ронические облитерирующие заболевания аорты и артерий нижних конечностей (обусловленные в большинстве случаев атеросклерозом) составляют более 20% от всех видов сердечно-сосудистой патологии, что соответствует 2–3% от общей численности населения [1]. Так, в эдинбургском исследовании (1990) [2] пациенты с перемежающейся хромотой составили 4,5% в возрастной группе от 55 до 74 лет, а асимптомные поражения отмечены в 8% случаев. Показательно, что лечащие врачи только 30–50% пациентов знали о наличии у последних перемежающейся хромоты [3].
Главной особенностью данной патологии является неуклонно прогрессирующее течение
, характеризующееся нарастанием выраженности перемежающейся хромоты и переходом ее в постоянный болевой синдром или гангрену, которая возникает у 15–20% больных [4]. Периоперационная летальность при ампутациях ниже колена составляет 5–10%, выше колена – 15–20%. Летальность в течение первых двух лет после ампутации колеблется в пределах 25–30%, а через 5 лет – 50–75%. При этом после ампутации голени на протезе через 2 года ходят лишь 69,4% больных, а бедра – всего 30,3%.
Летальность после реконструктивных операций, ранее составлявшая 2–13% [5], в настоящее время в ведущих клиниках России не превышает 1,2% [6]. Оценивая необходимое количество операций больным с облитерирующими заболеваниями аорты и артерий нижних конечностей, можно как пример привести США, где в 1995 г. выполнено 400 000 госпитализаций по поводу заболеваний периферических артерий. Было выполнено 50 000 баллонных ангиопластик, 110 000 шунтирований, 69000 ампутаций. При этом расходы при первичной ампутации в развитых странах, таких как Великобритания, превышали вдвое расходы при успешной реваскуляризации [7].
По данным Л.А. Бокерия и соавт. [8], на 1998 г. потребность в реконструктивных операциях на артериальной системе в России составляет 930 на 1 млн населения, ежегодно выполняется не более 22% от необходимого количества.
Патоморфология и патогенез
Термин “атеросклероз” происходит от греческих слов “athtre” – пшеничная кашица и “sclerosis” – твердый. Несмотря на то что патоморфология атеросклероза изучается более 140 лет, начиная с первых работ Р. Вирхова (1856), характер и особенности процессов, происходящих в стенке сосудов при этом заболевании, остаются до конца не ясными. Даже наблюдаемые при микроскопическом исследовании клеточные и внеклеточные изменения в стенке сосуда в области формирования атеросклеротической бляшки трактуются по-разному. При формировании атеросклероза основные изменения происходят в эндотелии и гладких мышечных клетках субэндотелиального слоя интимы.
Различают 4 вида атеросклеротических изменений сосудов:
1. Жировые пятна или полоски, представляющие собой участки бледно-желтого цвета, содержащие липиды, не возвышающиеся над поверхностью интимы. Это наиболее ранние проявления атеросклероза.
2. Фиброзные бляшки
– овальные или округлые образования, содержащие липиды, возвышающиеся над поверхностью интимы, нередко сливающиеся в сплошные бугристые поля.
3. Фиброзные бляшки с различного рода осложнениями:
изъязвлением, кровоизлиянием, наложением тромботических масс.
4. Кальциноз
– отложение в фиброзных бляшках солей кальция.
Наиболее значительные атеросклеротические изменения чаще всего локализуются в местах наибольшего гемодинамического или механического воздействия на стенку сосуда: зонах бифуркации, местах отхождения магистральных артерий от аорты и в извитых участках артерии.
По данным J.S.A. Fuchs [9], к ведущим факторам риска развития атеросклероза относятся артериальная гипертензия, гиперхолестеринемия и курение. В меньшей степени влияют ожирение, сахарный диабет, гипертриглицеридемия, сидячий образ жизни, стресс и наследственность.
Современные методы диагностики
Современные методы диагностики расстройств периферического артериального кровообращения отличаются широтой диапазона – одни используются для уточнения клинического диагноза, характера и степени поражения сосудов, другие – для оценки эффективности проводимого лечения либо динамического наблюдения за больным. С целью изучения гемодинамики в нижних конечностях и топической диагностики поражений артериального русла используют следующие инструментальные методы исследования:
ультразвуковая допплер-сфигмоманометрия, тредмил-тест, ультразвуковое ангиосканирование, в том числе дуплексное, и рентгеноконтрастная аортоартериография. Кроме этого, необходимо определять показатели липидного обмена, свертывающей системы и реологических свойств крови.
Как первый этап, всем пациентам с подозрением на окклюзионно-стенотическое поражение аорты или артерий нижних конечностей выполняется ультразвуковая допплерография с измерением лодыжечно-плечевого индекса
.
Этот индекс составляет отношение максимального давления на одной из берцовых артерий к давлению на плечевой артерии. Снижение этого показателя менее 0,9 требует более пристального внимания к пациенту. В этой связи одним из наиболее перспективных в настоящее время представляется комбинированное использование ультразвуковой допплерометрии и стандартного тредмил-теста
[10]. К неинвазивным методам исследования также относится
ультразвуковое ангиосканирование
, благодаря которому можно с большой долей достоверности определить степень стенотического поражения. В последнее время
дуплексное ультразвуковое ангиосканирование
в алгоритме диагностической программы занимает одно из ведущих мест вследствие неинвазивности и безопасности, а также высокой чувствительности и специфичности. По данным дуплексного сканирования определяется не только структура атеросклеротической бляшки, но и оценивается гемодинамическая степень стеноза, что имеет принципиальное значение.
Рентгеноконтрастное ангиографическое исследование
в настоящее время остается основным методом диагностики облитерирующих заболеваний сосудистого русла. С помощью этого метода возможно точно определить локализацию, протяженность, степень и характер стеноза, множественность окклюзионных поражений магистральных артерий нижних конечностей, оценить состояние коллатерального русла, прогнозировать характер и объем реконструктивной операции, а также осуществлять контроль за эффективностью лечения и хирургического вмешательства. В арсенале ангиологов и сосудистых хирургов имеются также такие методы диагностики, как лазерная допплер-флоуметрия, транскутанное мониторирование О2, фотоплетизмография, радиоизотопное исследование, компьютерная томография и ядерно-магнитный резонанс.
Терминология и клиническая классификация
В клинической практике для обозначения заболеваний брюшной аорты, приводящих к ее сужению или окклюзии, часто употребляют термин “синдром Лериша”
, который обобщает картину поражения бифуркации брюшной аорты и подвздошных артерий.
Основными особенностями клинического течения этого поражения являются высокая перемежающаяся хромота (боль в конечности при ходьбе), двустороннее отсутствие пульса на артериях и импотенция.
Примерно у 30% пациентов с хронической артериальной недостаточностью нижних конечностей атеросклеротический окклюзирующий процесс локализуется в брюшном отделе аорты, у 70% больных – в артериях бедренно-подколенного сегмента.
Тактические вопросы в выборе того или иного метода лечения при атеросклеротическом поражении аорты и артерий конечности основываются на выраженности хронического ишемического синдрома, который классифицируется по 4 стадиям заболевания. Преобладающей системой оценки являются классификация R. Fontaine и А.В. Покровского.
При 1-й стадии заболевания
боль в нижних конечностях появляется только при большой физической нагрузке, она не связана с проходимой пациентом дистанцией.
Для 2-й стадии
характерно появление лимитирующей боли при ходьбе (лимитирующая перемежающаяся хромота). С тактических позиций эту стадию подразделяют на 2А (проходимая дистанция без боли более 200 м) и 2Б (появление болей при ходьбе на расстояние менее 200 м).
Боль в конечности в состоянии покоя характеризует 3-ю стадию
, появление язвенно-некротических изменений –
4-ю стадию заболевания.
Хирургическая тактика и определение степени операционного риска
Принципиальной общепризнанной позицией в выборе метода лечения в соответствии с данной классификацией считается необходимость восстановления магистрального кровотока с применением реконструктивных операций, начиная со стадии 2Б.
При решении вопроса об оперативном лечении необходимо учитывать мультифокальный характер атеросклеротического поражения и наличие сопутствующей патологии, отягощающей состояние больных. По нашим данным, около 70% пациентов страдают ишемической болезнью сердца, у каждого 4-го выявляют постинфарктный кардиосклероз и хроническую недостаточность мозгового кровообращения, у половины больных имеется гипертоническая болезнь в сочетании с хроническими заболеваниями легких. У 35% — заболевания желудочно-кишечного тракта и у каждого 7-го — сахарный диабет.
Исходя из всего вышеизложенного, лечение больных атеросклерозом должно быть комплексным
, направленным как на восстановление кровообращения в аорте и магистральных артериях конечности, так и на коррекцию сопутствующей патологии. Основная цель – восстановление крообращения – должна достигаться с минимальной травмой для больного.
Принципы консервативного лечения
Одним из главных направлений консервативного лечения является улучшение реологических свойств крови.
И это не случайно, так как у больных имеются выраженные отклонения реологических характеристик: повышение уровня фибриногена в плазме, увеличение времени агрегации тромбоцитов, вязкости крови и плазмы, уменьшение фибринолитической активности крови и изменение показателей тромбоэластограммы в сторону гиперкоагуляции.
Среди лекарственных средств, используемых для консервативной терапии, выделяется несколько групп.
1. Спазмолитики:
периферические миолитики (папаверин, дротаверин, бенциклан), препараты блокирующие a-адренорецепторы или преганглионарную передачу импульса (кофеин, празозин), центральные холиномиолитики (толперизон, баклофен), вещества с разносторонним действием (абана).
2. Дезагреганты:
пентоксифиллин, ацетилсалициловая кислота, ксантинола никотинат, тиклопидин, реополиглюкин.
3. Антиатеросклеротические средства:
препараты, блокирующие всасывание холестерина из кишечника (холестирамин), тормозящие биосинтез и перенос холестерина и триглицеридов (производные фиброевой кислоты – клофибрат, ципрофибрат) и статины (ловастатин, симвастатин), другие средства (никотиновая кислота).
4. Препараты метаболического действия:
солкосерил, актовегин и др.
5. Ангиопротекторы:
пирикарбат и др.
Особо хочется подчеркнуть, что важное место в общем арсенале лечебных мероприятий у больных с облитерирующими заболеваниями аорты и артерий нижних конечностей занимает дозированная ходьба
– терренкур, которая способствует развитию коллатерального кровообращения.
Сугубо консервативное лечение показано больным с хронической артериальной недостаточностью 1-й стадии и 2А, у пациентов со стадией 2Б и критической ишемией с развитием язвенно-некротических поражений встает вопрос о необходимости восстановления магистрального кровообращения. Благодаря возможностям современных технологий в последние годы появилось много работ по применению баллонной ангиопластики
у пациентов с различной локализацией окклюзионно-стенотических поражений артерий таза и нижних конечностей.
Однако не во всех случаях удается применить баллонную пластику вследствие окклюзии аорты или распространенных окклюзий артерий. Попытки реканализации в этих случаях опасны развитием тромбоза магистральных артерий (нередко с тромбозом периферического русла), что неминуемо ведет к ампутации конечности в 60% случаев, а нередко и к летальным исходам.
Виды реконструктивных хирургических вмешательств
При высокой окклюзии аорты, двустороннем поражении артерий конечностей в зависимости от тяжести состояния больного выполняют операции от аортобедренного бифуркационного или линейного шунтирования до подмышечно- или подключично-бедренного бифуркационного шунтирования. Если критическая ишемия имеется только с одной стороны, то при поражении подвздошной и бедренной артерии на контралатеральной конечности выполняется одностороннее перекрестное подвздошно-бедренное, подмышечно- или подключично-бедренное шунтирование
.
На современном этапе реконструктивные операции занимают ведущее место в лечении этих больных. Количество таких операций постоянно увеличивается, значительно расширяется их объем, что дает возможность сохранить конечность даже при тяжелых формах хронической артериальной недостаточности. Для рассасывания келлоидных рубцов, возникающих после операции, эффективен препарат Контрактубекс
, обладающий фибринолитическим, антитромботическим и кератолитическим действием.
Между тем выполнение полноценной реконструкции нередко вступает в противоречие с возможностями больного перенести оперативное вмешательство. Операции в этих случаях должны быть минимальными по травматичности и продолжительности, так как у подавляющего большинства этого контингента больных имеются тяжелые сопутствующие заболевания, резко ограничивающие функциональные резервные возможности организма [11]. Использование метода комбинированных операций
, включающих баллонную ангиопластику в сочетании с открытой операцией под перидуральным или местным обезболиванием, позволяет значительно сократить объем вмешательства и отказаться от сложной хирургической реконструкции на нескольких сегментах.
Клинический случай
Больной З., 68 лет, поступил с жалобами
на ноющие боли в правой голени и стопе в покое, перемежающуюся хромоту через 30 м.
Ультразвуковая допплерография:
значительное снижение магистрального кровотока по правой общей бедренной артерии, коллатеральный кровоток на подколенных и тибиальных артериях.
Лодыжечно-плечевой индекс
слева 0,59, справа 0,35.
Аортоартериография:
критический стеноз общей подвздошной артерии (ОПА) справа; стеноз глубокой бедренной артерии (ГБА) справа; окклюзия обеих поверхностных бедренных артерий (ПБА), сегментарная окклюзия правой подколенной артерии на протяжении 5 см (рис. 1).
Рис. 1. Ангиограммы больного З.: а — стеноз ОПА справа; б — стеноз ГБА справа, окклюзия обеих ПБА; в — после баллонной ангиопластики (отсутствие зоны стеноза правой ОПА).
Атеросклеротическое поражение артерий (история болезни).
Сопутствующие заболевания: ишемическая болезнь сердца, атеросклеротический кардиосклероз, стенокардия напряжения, хронический бронхит, пневмосклероз, эмфизема легких.
ишемическая болезнь сердца, атеросклеротический кардиосклероз, стенокардия напряжения, хронический бронхит, пневмосклероз, эмфизема легких.
Первым этапом выполнена баллонная ангиопластика ОПА справа, вторым – под перидуральной анестезией – боковая пластика ГБА справа (рис. 2).
Рис. 2. Схема этапов оперативного лечения больного З.: а — до операции; б — баллонная ангиопластика правой ОПА; в — состояние после пластики ГБА и баллонной ангиопластики ОПА справа.
В результате
отмечена положительная динамика: лодыжечно-плечевой индекс справа увеличился до 0,71 (исходно 0,35). В удовлетворительном состоянии больной выписан на амбулаторное лечение.
Список литературы Вы можете найти на сайте https://www.rmj.ru
Литература:
1. Покровский А.В., Кошкин В.М., Кириченко А.А. и др. Вазапростан (простагландин Е1) в лечении тяжелых стадий артериальной недостаточности нижних конечностей. Пособие для врачей. М., 1999; 16.
2. Fowkes F.G., Housley E., Cawood E.H. et al. Edinburgh artery study: prevalence оf asymptomatic and symptomatic peripheral arterial disease in the general population. Int J Epidimiol 1991; 20: 384–92.
3. Бураковский А.И., Бокерия Л.А. Сердечно-сосудистая хирургия. М., 1989; 750.
4. Dormandy J., Mahir M., Ascady G. et al. Fate of the patient with chronic leg ischaemia. J. Cardiovasc Surg 1989; 30: 50–7.
5. Stoffers HEJH. Kaiser V. and Knottnerus J.A. Prevalence in the general practice. In: Fowkes FGR, ed. Epidemiology of peripheral vascular disease. London: Springer Verlag. 1992; 109–13.
6. Спиридонов А.А., Фитилева Е.Б., Аракелян В.С. Пути снижения летальности при хирургическом лечении хронической ишемии нижних конечностей. Ж. Анналы хирургии. 1996; 1: 62–6.
7. Биэд Дж.Д. Ампутация или реконструкция при критической ишемии. Ж. Ангитология и сосудистая хирургия 1998; 1 (4): 72–82.
8. Бокерия Л.А., Гудкова Р.Г. Хирургия сердца и сосудов в Российской федерации. М., 1998; 43.
9. Fuchs JSA. Atherogenesis and the medical management of Atherosclerosis. In: Rutherford RB, ed. Vascular surgery. Philadelphia: W.B. Saunders Company. 1996; 1: 222–35.
10. Затевахин И.И., Цициашвили М.Ш., Юдин Р.Ю. Тредмил в диагностике и лечении хронической артериальной недостаточности. М., 1999; 87.
11. Siskin G., Darling R.C. III, Stainken B. et al. Combined use of Iliac artery angioplasty and infrainguinal revascularization for treatment of multilevel atherosclerotic disease. Annals of Vascular Surgery. St. Louis. 1999; 13 (1): 45.
Прогноз и профилактика
Важнейшим прогностическим критерием при острой окклюзии сосудов конечностей является фактор времени. Ранняя операция и интенсивная терапия позволяют восстановить кровоток в 90% случаев. При поздно начатом лечении или его отсутствии наступает инвалидизация вследствие утраты конечности или летальный исход. При развитии реперфузионного синдрома гибель может наступить от сепсиса, почечной недостаточности, полиорганной недостаточности.
Профилактика острой окклюзии сосудов конечностей заключается в своевременном устранении потенциальных источников тромбоэмболии, профилактическом приеме антиагрегантов.
Анестезия при стентировании
Большинство эндоваскулярных процедур ангиопластики и стентирование сосудов нижних конечностей могут быть выполнены с умеренной внутривенной седацией и местной анестезией в месте прокола для доступа. Обязательно проводится мониторинг артериального давления, электрокардиограммы и уровня насыщения крови кислородом (пульсоксиметрия). На случай непредвиденных осложнений в операционной имеется дыхательный аппарат и дефибриллятор. Если операция проводится по поводу критической ишемии, то для комфортного положения пациента проводится эпидуральная анестезия (введение через катетер в область позвоночника анестезирующего препарата).
Наблюдение после ангиопластики и стентирования
В нашей клинике принята схема ведения пациента после операции для исключения осложнений ангиопластики и стентирования периферических артерий нижних конечностей:
- Для лучшего результата показана двойная дезагрегантная терапия, включающая приём плавикса и аспирина. Медикаментозная профилактика играет важную роль в отдалённых результатах вмешательства и продолжительности жизни пациентов.
- Первый осмотр проводится в первые 2 недели послеоперационного периода с обязательным УЗИ периферических сосудов.
- Следующие осмотры проводятся через несколько месяцев.
- Через год после хирургического лечения обязательно делают МСКТ ангиографию ног.
Баллонная ангиопластика и стентирование артерий нижних конечностей является эффективным методом восстановления кровотока при большинстве окклюзионных поражений кроме подколенной артерии. По своим непосредственным результатам этот метод не уступает открытым операциям шунтирования, если проводится по строгим показаниям. Преимуществом эндоваскулярной хирургии является малая травматичность, отсутствие боли, возможность повторных вмешательств, а также меньший риск для жизни.
По мере совершенствования инструментария для ангиопластики и стентирования малоинвазивные вмешательства занимают всё большее место в ведении пациентов с критической ишемией и гангреной.
Эндоваскулярные технологии в Инновационном сосудистом центре
Основной миссией нашей клиники является лечение критической ишемии и гангрены конечностей. Мы стремимся к использованию новейших подходов для решения этой задачи. С 2011 года в практику наших сосудистых хирургов внедрены методы эндоваскулярной хирургии при критической ишемии. Отмечая преимущества эндоваскулярного подхода, мы с каждым годом расширяем возможности нашей клиники в применении данных методов.
Роль малоинвазивных технологий растёт — сейчас более 50% с критической ишемией и гангреной оперируется эндоваскулярно, а ещё более, чем у 40% применяется гибридный подход. Это шунтирование с ангиопластикой и стентированием артерий нижних конечностей. Инновационный сосудистый центр — это клиника, где делают более 500 операций ангиопластики и стентирования артерий нижних конечностей в год.
Возможности эндоваскулярной хирургии развиваются синхронно с созданием инновационных инструментов для лечения, поэтому в нашей практике операции через прокол всё больше вытесняют открытые вмешательства.
Подготовка к стентированию
Перед выполнением операции стентирования пациент должен быть соответствующим образом обследован на предмет сосудистых поражений, рисков осложнений. Должен быть выполнен комплекс лабораторных обследований перед операцией и коагулограмма. Учитывая нагрузку пациента антитромботическими препаратами, необходимо исключить возможные источники кровотечения (язву желудка, кровоточащий геморрой).
Накануне вмешательства вводится лёгкий седативный препарат, позволяющий пациенту хорошо поспать и не нервничать. Перед операцией пациенту выбривается место предполагаемого доступа. В предоперационной сестра установит мочевой катетер и внутривенную иглу для инфузий. В операционной на плечо накладывается манжета для измерения давления и датчики для непрерывного снятия ЭКГ фиксируются на груди.
Виды ангиопластики
- Субинтимальная баллонная ангиопластика сосудов — проводник проводится под изменённой внутренней стенкой (интимой) сосуда и дальше выходит в свободный просвет.
- Интралюминарная ангиопластика — разновидность вмешательства, когда проводник проходит по естественному просвету артерии, проскальзывая через суженные и закупоренные участки.
- При лазерной ангиопластике — атеросклеротическая бляшка выжигается специальным лазерным катетером.
Баллонная ангиопластика артерий нижних конечностей без стентирования рекомендуется для лечения поражений голени. Обязательно надо стентировать подвздошные артерии, так как частота повторных сужений (рестенозов) без стента очень высока.
После проведения ангиопластики и стентирования обязательно проводится контрольная ангиография для оценки результата.
Лечение острой окклюзии сосудов конечностей
При подозрении на острую окклюзию сосудов конечностей пациент нуждается в неотложной госпитализации и консультации сосудистого хирурга. При ишемии напряжения и ишемии IА степени проводится интенсивная консервативная терапия, включающая введение тромболитиков (гепарин внутривенно), фибринолитических средств (фибринолизина, стрептокиназы, стрептодеказы, тканевого активатора плазминогена), антиагрегантов, спазмолитиков. Показаны физиотерапевтические процедуры (диадинамотерапия, магнитотерапия, баротерапия) и экстракорпоральная гемокоррекция (плазмаферез).
При отсутствии положительной динамики в течение 24 ч от момента возникновения острой окклюзии сосудов конечностей необходимо выполнение органосохраняющей хирургической операции — тромбэмболэктомии из периферической артерии с помощью баллонного катетера Фогарти или эндартерэктомии.
При ишемии IБ–IIБ степеней необходимо экстренное вмешательство, направленное на восстановление кровотока: эмбол- или тромбэктомия, обходное шунтирование. Протезирование сегмента периферической артерии проводится при непротяженных острых окклюзиях сосудов конечностей.
Ишемия IIIА–IIIБ степеней является показанием к экстренной тромб- или эмболэктомии, обходному шунтированию, которые обязательно дополняются фасциотомией. Восстановление кровообращения при ограниченных контрактурах позволяет выполнить отсроченную некрэктомию или последующую ампутацию на более низком уровне.
При ишемияи IIIВ степени операции на сосудах противопоказаны, поскольку восстановление кровотока может привести к развитию постишемического синдрома (аналогичному травматической токсемии при синдроме длительного раздавливания) и гибели больного. На данной стадии выполняется ампутация пораженной конечности. В послеоперационном периоде продолжается антикоагулянтная терапия для предупреждения ретромбоза и повторной эмболии.