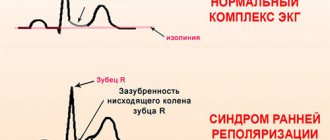
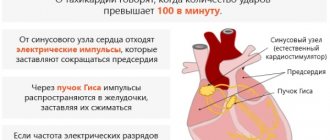
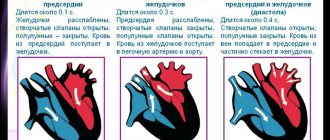
Потенциал действия (ПД) — это кратковременные амплитудные изменения мембранного потенциала покоя (МПС), возникающие при возбуждении живой клетки. По сути это электрический разряд — быстрая кратковременное изменение потенциала на небольшом участке мембраны возбудимой клетки (нейрона или мышечного волокна), в результате которого внешняя поверхность этого участка становится отрицательно заряженной по отношению к соседним участкам мембраны, тогда как его внутренняя поверхность становится положительно заряженной по отношению к соседним участкам мембраны. Потенциал действия является физической основой нервного или мышечного импульса, который играет сигнальную (регуляторную) роль.
Общая характеристика
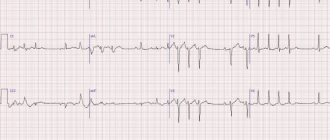
Потенциалы действия могут отличаться по своим параметрам в зависимости от типа клетки и даже на разных участках мембраны одной и той же клетки. Наиболее характерный пример различий: потенциал действия сердечной мышцы и потенциал действия большинства нейронов. Все же, в основе любого потенциала действия лежат следующие явления:
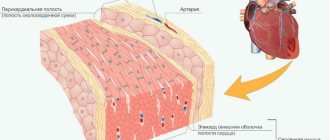
- «Мембрана живой клетки поляризована» — ее внутренняя поверхность заряжена отрицательно по отношению к наружной благодаря тому, что в растворе у ее внешней поверхности находится большее количество положительно заряженных частиц (катионов), а у внутренней поверхности — большее количество отрицательно заряженных частиц (анионов).
- «Мембрана имеет избирательную проницаемость ‘- ее проницаемость для различных частиц (атомов или молекул) зависит от их размеров, электрического заряда и химических свойств.
- «Мембрана возбудимой клетки способна быстро менять свою проницаемость ‘для определенного вида катионов, вызывая переход положительного заряда с внешней стороны на внутреннюю
Первые два свойства характерны для всех живых клеток. Третья же является особенностью клеток возбудимых тканей и причиной, по которой их мембраны способны генерировать и проводить потенциалы действия.
Основной математической моделью, описывающей генерацию и передачу потенциала действия, является модель Ходжкина-Хаксли.
Фаза реполяризации потенциала действия обусловлена диффузией ионов
Здравствуйте читатели моего проекта »Биология для студентов»! Подготовка к экзаменам, зачетам и госэкзаменам, а также рефераты и презентации занимают много времени, если готовится по учебникам. Есть три способа подготовки к экзамену: по учебнику, по лекциям и поиск в интернете. Готовиться по учебнику очень долго.
Что касается лекций, не у всех есть хорошие лекции, так как не все преподаватели их нормально читают, и кроме того не все успевают их записывать. И остается третий вариант искать ответы на вопросы в интернете. Не для кого не секрет, что в настоящее время большинство студентов предпочитают именно этот вариант.
За пять лет учебы на факультете биотехнологии и биологии подготовка к сессии у меня занимала много времени. В Рунете не так много биологических сайтов. Конспекты по экономике, истории, социологии, политологии, математике найти очень просто. А ответы на вопросы по ботанике, зоологии, генетики, биофизике, биохимии гораздо сложнее.
Наверное, потому что биология не самая распространенная специальность. К тому же биологические предметы не являются общеобразовательными в отличие, например, от экономики и истории, которые изучаются практически на любых специальностях. В Рунете я не нашел ни одного сайта на которым был бы представлен необходимый контент для подготовки к экзаменам, зачетам и госэкзаменам по биологическим дисциплинам. И я решил создать его.
Также я хотел бы вас попросить рассказать об этом сайте своим однокурсникам, друзьям и знакомым, которые являются студентами биологических специальностей. Это поможет развитию данного проекта.
Фазы
Можно четко выделить пять фаз развития ПД:
Нарастание (деполяризация)
Возникновение потенциала действия (ПД) связано с увеличением проницаемости мембраны для ионов натрия (в 20 раз по сравнению с проницаемостью для К +, и в 500 раз по сравнению с исходной проницаемостью Na +) и последующим усилением диффузии этих ионов по концентрационном градиенту внутрь клетки, приводит к изменению (уменьшение) мембранного потенциала. Уменьшение мембранного потенциала приводит к увеличению проницаемости мембраны для натрия путем открытия потенциал-зависимых натриевых каналов, а увеличение проницаемости сопровождается усилением диффузии натрия в цитоплазму, что вызывает еще более значительную деполяризацию мембраны. Благодаря наличию положительной обратной связи деполяризация мембраны при возбуждении происходит с ускорением и поток ионов натрия в клетку все время растет. Интенсивность же потока ионов калия, направленного из клетки наружу, в первые моменты возбуждения остается в начале. Усиленный поток положительно заряженных ионов натрия внутрь клетки вызывает сначала исчезновение избыточного отрицательного заряда на внутренней поверхности мембраны, а затем приводит к перезарядки мембраны. Поступления ионов натрия происходит до тех пор, пока внутренняя поверхность мембраны не приобретет положительный заряд, достаточный для уравновешивания градиента концентрации натрия и прекращение его дальнейшего перехода внутрь клетки. Натриевый возникновения ПД подтверждают опыты с изменением внешней и внутренней концентрации этого иона. Было показано, что десятикратном изменении концентрации ионов натрия во внешнем или внутреннем среде клетки, соответствует изменение ПД на 58 мВ. При полном удалении ионов натрия из окружающей клетку жидкости ПД ни возникал. Таким образом, установлено, что ПД возникает в результате избыточной, по сравнению с покоем, диффузии ионов натрия из окружающей жидкости внутрь клетки. Период, в течение которого проницаемость мембраны для ионов натрия при открытии натриевых каналов растет, является небольшим (0,5-1 мс) вслед за этим наблюдается повышение проницаемости мембраны для ионов калия благодаря открытию потенциал-зависимых калиевых каналов, и, следовательно, усиление диффузии этих ионов из клетки наружу.
Принцип «все или ничего» Согласно закону «все-или-ничего» мембрана клетки возбудимой ткани или не отвечает стимул совсем, или отвечает с максимально возможной для нее на данный момент силой. Действие раздражителя обычно приводит к локальной деполяризации мембраны. Это вызывает открытие натриевых каналов, которые чувствительны к изменениям потенциала, а через это — увеличивает натриевую проводимость, что приводит к еще большей деполяризации. Существование такой обратной связи обеспечивает регенеративную (возобновляемую) деполяризацию клеточной мембраны. Величина потенциала действия зависит от силы раздражителя, а сам он возникает только в том случае, когда деполяризация превышает некоторый определенный для каждой клетки предельный уровень. Это явление получило название «все или ничего». Однако, если деполяризация составляет 50-75% от предельной величины, то в клетке может возникнуть локальный ответ, амплитуда которой значительно ниже амплитуду потенциала действия. Отсутствие потенциала действия при пидграничному уровне деполяризации объясняется тем, что при этом недостаточно увеличивается натриевая проницаемость, чтобы вызвать регенеративную деполяризацию. Уровень деполяризации, который возникает при этом, не вызывает открытие новых натриевых каналов, поэтому натриевая проводимость быстро уменьшается, и в клетке снова устанавливается потенциал покоя.
Овершут
Деполяризация мембраны приводит к реверсии мембранного потенциала (МП становится положительным). В фазу овершута Na + -ток начинает стремительно снижаться, что связано с инактивацией потенциал-зависимых Na + -каналов (время открытого состояния — судьбы миллисекунды) и исчезновением электрохимического градиента Na +.
Рефрактерность Одним из последствий исчезновения градиента Na + является рефрактерность мембраны — временная неспособность отвечать на раздражитель. Если раздражитель возникает сразу после прохождения потенциала действия, то возбудимость не возникнет ни при силе раздражителя на уровне порога, ни при значительно более сильное раздражителю. Такое положение полной невозбудимости называется абсолютным рефрактерным периодом. За ним следует относительный рефрактерный период, когда надпороговый раздражитель может вызвать потенциал действия со значительно меньшей амплитудой чем в норме. Потенциал действия привычной амплитуды при действии порогового раздражителя можно вызвать только после нескольких миллисекунд после предварительного потенциала действия. Абсолютный рефрактерный период ограничивает максимальную частоту генерации потенциалов действия.
Реполяризация
Увеличение ионного потока калия, направленного из клетки наружу, приводит к уменьшению мембранного потенциала, в свою очередь обусловливает уменьшение проницаемости мембраны для ионов натрия, что, как указывалось, является функцией мембранного потенциала. Таким образом, второй этап характеризуется тем, что поток ионов калия из клетки наружу растет, а встречный поток ионов натрия уменьшается. Такая реполяризация мембраны продолжается, пока не произойдет восстановление потенциала покоя — реполяризация мембраны. После этого проницаемость для ионов калия также падает до исходной величины. Внешняя поверхность мембраны за счет положительно заряженных ионов калия, вышедших в среду, вновь приобретает положительный потенциала относительно внутреннего.
Следовая деполяризация и гиперполяризация
В конечной фазе происходит замедление восстановления мембранного потенциала покоя, и при этом регистрируются следовые реакции в виде следовой деполяризации и гиперполяризации, обусловлены медленным восстановлением исходной проницаемости для ионов К +.
ПОЛЯРИЗАЦИЯ И ДЕПОЛЯРИЗАЦИЯ
В тех случаях, когда имеет место разделение зарядов и положительные заряды расположены в одном месте, а отрицательные в другом, физики говорят о поляризации заряда. Физики употребляют термин по аналогии с разноименными магнитными силами, которые скапливаются на противоположных концах, или полюсах (название дано потому, что свободно двигающаяся намагниченная полоска указывает своими концами в стороны географических полюсов) полосового магнита. В обсуждаемом случае мы имеем концентрацию положительных зарядов на одной стороне мембраны и концентрацию отрицательных зарядов на другой стороне мембраны, то есть мы можем говорить о поляризованной мембране.
Однако в любом случае, когда имеет место разделение зарядов, немедленно возникает и электрический потенциал. Потенциал является мерой силы, которая стремится сблизить разделенные заряды и ликвидировать поляризацию. Электрический потенциал поэтому называют также электродвижущей силой, которая сокращенно обозначается ЭДС.
Электрический потенциал называется потенциалом именно потому, что он в действительности не приводит в движение заряды, так как существует противодействующая сила, удерживающая противоположные электрические заряды от сближения. Эта сила будет существовать до тех пор, пока расходуется энергия па ее поддержание (что и происходит в клетках). Таким образом, сила, стремящаяся сблизить заряды, обладает лишь возможностью, или потенцией, сделать это, и такое сближение происходит только в том случае, когда энергия, затрачиваемая на разделение зарядов, ослабевает. Электрический потенциал измеряют в единицах, названных вольтами, в честь Вольта, человека, создавшего первую в мире электрическую батарею.
Физики сумели измерить электрический потенциал, существующий между двумя сторонами клеточной мембраны. Он оказался равным 0,07 вольт. Можно сказать также, что этот потенциал равен 70 милливольтам, так как милливольт равен одной тысячной вольта. Конечно, это очень маленький потенциал по сравнению со 120 вольтами (120 000 милливольт) напряжения в сети переменного тока или по сравнению с тысячами вольт напряжения в линиях электропередачи. Но это все же удивительный потенциал, учитывая материалы, которые имеет в своем распоряжении клетка для построения электрических систем.
Любая причина, прерывающая деятельность натриевого насоса, приведет к резкому выравниванию концентраций ионов натрия и калия по обе стороны мембраны. Это, в свою очередь, автоматически приведет к выравниванию зарядов. Таким образом, мембрана станет деполяризованной. Конечно, это происходит при повреждении или гибели клетки. Но существуют, правда, три вида стимулов, которые могут вызвать деполяризацию, не причиняя клетке никакого вреда (если, конечно, эти стимулы не слишком сильны). К таким лам относятся механические, химические и электрические.
Давление — это пример механического стимула. Давление на участок мембраны приводит к а расширению и (по пока не попятным причинам) вызовет в этом месте деполяризацию. Высокая температура приводит к расширению мембраны, холод сокращает ее, и эти механические изменения тоже вызывают деполяризацию.
К такому же результату приводит воздействие на мембрану некоторых химических соединений и воздействие на нее слабых электрических токов. (В последнем случае причина деполяризации представляется наиболее очевидной. В конце концов, почему электрический феномен поляризации нельзя изменить с помощью приложенного извне электрического потенциала?)
Произошедшая в одном месте мембраны деполяризация служит стимулом для распространения деполяризации по мембране. Ион натрия, хлынувший в клетку в месте, где произошла деполяризация прекратилось действие натриевого насоса, вытесняет наружу ион калия. Ионы натрия меньше размерами и более подвижны, чем ионы калия. Поэтому в клетку входит больше ионов натрия, чем выходит из нее ионов калия. В результате кривая деполяризации пересекает нулевую отметку и поднимается выше. Клетка снова оказывается поляризованной, но с обратным знаком. На какой-то момент клеш приобретает внутренний положительный заряд, благодаря присутствию в ней избытка ионов натрия. На внешней стороне мембраны появляется маленький отрицательный заряд.
Противоположно направленная поляризация может служить электрическим стимулом, который парализует работу натриевого насоса в участках, примыкающих к месту первоначального стимула. Эти примыкающие участки поляризуются, потом происходит поляризация с обратным знаком и возникает деполяризация в более отдаленных участках. Таким образом, волна деполяризации прокатывается по всей мембране. В начальном участке поляризация с обратным знаком не может продолжаться долго. Ионы калия продолжают выходить из клетки, постепенно их поток уравнивается с потоком входящих ионов натрия. Положительный заряд внутри клетки исчезает. Это исчезновение обратного потенциала в какой-то степени реактивирует натриевый насос в этом месте мембраны. Ионы натрия начинают выходить из клетки, и в нее начинают проникать ионы калия. Данный участок мембраны вступает в фазу реполяризации. Так как эти события происходят во всех участках деполяризации мембраны, то вслед за волной деполяризации по мембране прокатывается волна реполяризации.
Между моментами деполяризации и полной ре-поляризации мембраны не отвечают на обычные стимулы. Этот период времени называется рефракторным периодом. Он длится очень короткое время малую долю секунды. Волна деполяризации, прошедшая через определенный участок мембраны, делает этот участок невосприимчивым к возбуждению. Предыдущий стимул становится в каком-то смысле единичным и изолированным. Как именно мельчайшие изменения зарядов, участвующие в деполяризации, реализуют такой ответ, неизвестно, но факт остается фактом — ответ мембраны на стимул изолирован и единичен. Если мышцу стимулировать в одном месте небольшим электрическим разрядом, то мышца сократится. Но сократится не только тот участок, к которому было приложено электрическое раздражение; сократится все мышечное волокно. Волна деполяризации проходит по мышечному волокну со скоростью от 0,5 до 3 метров в секунду, в зависимости от длины волокна, и этой скорости достаточно, чтобы создалось впечатление, что мышца сокращается, как одно целое.
Этот феномен поляризации-деполяризации-реполяризации присущ всем клеткам, но в некоторых он выражен больше. В процессе эволюции появились клетки, которые извлекли выгоды из этого явления. Эта специализация может пойти в двух направлениях. Во-первых, и это происходит весьма редко, могут развиться органы, которые способны создавать высокие электрические потенциалы. При стимуляции деполяризация реализуется не мышечным сокращением или другим физиологическим ответом, а возникновением электрического тока. Это не пустая трата энергии. Если стимул -это нападение врага, то электрический разряд может ранить или убить его.
Существует семь видов рыб (некоторые из них костистые, некоторые относятся к отряду хрящевых, являясь родственниками акул), специализированных именно в этом направлении. Самый живописный представитель — это рыба, которую в народе называют «электрическим угрем», а в науке весьма символическим именем — Electrophorus electricus.
Электрический угорь — обитатель пресных вод, и встречается в северной части Южной Америки — в Ориноко, Амазонке и ее притоках. Строго говоря, эта рыба не родственница угрям, ее назвали так за длинный хвост, который составляет четыре пятых тела этого животного, длина которого составляет от 6 до 9 футов. Все обычные органы этой рыбы умещаются в передней части туловища длиной около 15 — 16 дюймов.
Более половины длинного хвоста занято последовательностью блоков модифицированных мышц, которые образуют «электрический орган». Каждая из этих мышц производит потенциал, который не превышает потенциал обычной мышцы. Но тысячи и тысячи элементов этой «батареи» соединены таким образом, что их потенциалы складываются. Отдохнувший электрический угорь способен накопить потенциал порядка 600 — 700 вольт и разряжать его со скоростью 300 раз в секунду. При утомлении этот показатель снижается до 50 раз в секунду, но такой темп угорь может выдержать в течение длительного времени. Электрический удар достаточно силен для того, чтобы убить мелкое животное, которыми питается эта рыба, или чтобы нанести чувствительное поражение животному более крупному, которое по ошибке вдруг решит съесть электрического угря.
Электрический орган — это великолепное оружие. Возможно, к такому электрошоку с удовольствием прибегли бы и другие животные, но эта батарея занимает слишком много места. Представьте себе, как мало животных имели бы крепкие клыки и когти, если бы они занимали половину массы их тела.
Второй тип специализации, предусматривающий использование электрических явлений, протекающих па клеточной мембране, заключается не в усилении потенциала, а в увеличении скорости распространения волны деполяризации. Возникают клетки с удлиненными отростками, которые представляют собой почти исключительно мембранные образования. Главная функция этих клеток — очень быстрая передача стимула от одной части тела к другой. Именно из таких клеток состоят нервы — те самые нервы, с рассмотрения которых началась эта глава.
НЕЙРОН
Нерпы, которые мы можем наблюдать невооруженным глазом, конечно же не являются отдельными клетками. Это пучки нервных волокон, иногда в этих пучках содержится очень много волокон, каждое из которых представляет собой часть нервной клетки. Все волокна пучка идут в одном направлении и, ради удобства и экономии места, связаны между собой, хотя отдельные волокна могут выполнять совершенно разные функции. Точно так же отдельные изолированные электрические провода, выполняющие совершенно разные задачи, для удобства объединяют в один электрический кабель. Само нервное волокно является частью нервной клетки, которую также называют нейроном. Это греческое производное латинского слова «нерв». Греки эпохи Гиппократа приложили это слово к нервам в истинном смысле и к сухожилиям. Теперь этот термин обозначает исключительно индивидуальную нервную клетку. Основная часть нейрона — тело практически мало чем отличается от всех остальных клеток организма. Тело содержит ядро и цитоплазму. Самым большим отличием нервной клетки от прочих клеток является наличие длинных выростов из тела клетки. От большей части поверхности тела нервной клетки отходят выросты, которые ветвятся на протяжении. Эти ветвящиеся выросты напоминают крону дерева и называются дендритами (от греческого слова «дерево»).
На поверхности тела клетки есть одно место, из которого выходит один, особенно длинный, отросток, который не ветвится на всем своем (иногда огромном) протяжении. Этот отросток называется аксоном. Почему он так называется, я объясню позже. Именно аксонами представлены типичные нервные волокна нервного пучка. И хотя аксон микроскопически тонок, его длина может составить несколько футов, что представляется необычным, если учесть, что аксон — это всего лишь часть единственной нервной клетки.
Возникшая в какой-либо части нервной клетки деполяризация с большой скоростью распространяется по волокну. Волна деполяризации, распространяющаяся по отросткам нервной клетки, называется нервным импульсом. Импульс может распространяться по волокну в любом направлении; так, если нанести стимул на середину волокна, то импульс будет распространяться в обе стороны. Однако в живых системах практически всегда получается так, что импульсы распространяются по дендритам только в одну сторону — к телу клетки. По аксону же импульс всегда распространяется от тела клетки.
Скорость распространения импульса по нервному волокну была впервые измерена в 1852 году немецким ученым Германом Гельмгольцем. Для этого он наносил стимулы на нервное волокно па разных расстояниях от мышцы и регистрировал время, через которое мышца сокращалась. Если расстояние увеличивалось, то удлинялась и задержка, после которой наступало сокращение. Задержка соответствовала времени, которое требовалось импульсу, чтобы пройти дополнительное расстояние.
Довольно интересен тот факт, что за шесть лет до опыта Гельмгольца знаменитый немецкий физиолог Иоганнес Мюллер в припадке консерватизма, столь характерного для ученых на склоне их карьеры, категорически заявлял, что никто и никогда не сможет измерить скорость проведения импульса по нерву.
В разных волокнах скорость проведения импульса не одинакова. Во-первых, скорость, с которой импульс движется по аксону, грубо зависит от его толщины.
Чем толще аксон, тем больше скорость распространения импульса. В очень тонких волокнах импульс движется по ним довольно медленно, со скоростью двух метров в секунду и даже меньше. Не быстрее, чем, скажем, распространяется волна деполяризации по мышечным волокнам. Очевидно, чем быстрее должен реагировать организм на тот или иной стимул, тем желательнее высокая скорость проведения импульсов. Один из способов достижения такого состояния — это увеличение толщины нервных волокон. В теле человека самые тонкие волокна имеют диаметр 0,5 микрона (микрон — это одна тысячная часть миллиметра), а самые толстые — 20 микрон, то есть в 40 раз больше. Площадь поперечного сечения толстых волокон в 1600 раз больше площади поперечного сечения тонких волокон.
Можно подумать, что поскольку млекопитающие обладают лучше развитой нервной системой, чем другие группы животных, то нервные импульсы распространяются у них с наибольшей скоростью, а нервные волокна толще, чем у всех остальных биологических видов. Но в действительности это не так. У низших животных, тараканов, нервные волокна толще, чем у людей.
Самыми толстыми нервными волокнами обладают самые развитые из моллюсков — кальмары. Крупные кальмары вообще, вероятно, являются самыми развитыми и высокоорганизованными животными из всех беспозвоночных. Учитывая их физические размеры, мы не удивляемся тому, что им требуется высокая скорость проведения импульсов и очень толстые аксоны. Нервные волокна, идущие к мышцам кальмара, называются гигантскими аксонами и достигают в диаметре 1 миллиметра. Это в 50 раз больше диаметра самого толстого аксона млекопитающих, а по площади поперечного сечения аксоны кальмара превосходят аксоны млекопитающих в 2500 раз. Гигантские аксоны кальмара — это дар божий для нейрофизиологов, которые могут легко ставить на них опыты (например, измерять потенциалы на мембранах аксонов), что очень трудно делать на чрезвычайно тонких аксонах позвоночных.
Тем не менее, почему все-таки беспозвоночные превзошли позвоночных толщиной нервных волокон, хотя позвоночные обладают более развитой нервной системой?
Ответ заключается в том, что скорость проведения импульсов по нервам у позвоночных зависит не только от толщины аксонов. Позвоночные животные получили в свое распоряжение более изощренный способ повышения скорости проведения импульсов по аксонам.
У позвоночных нервные волокна на ранних стадиях развития организма попадают в окружение так называемых сателлитных клеток. Некоторые из этих клеток называются шванновскими (по имени немецкого зоолога Теодора Шваина, одного из основоположников клеточной теории жизни). Шванновские клетки обертываются вокруг аксона, образуя все более и более плотную спираль, одевая волокно жироподобной оболочкой, которая называется миелиновой оболочкой. В конечном счете шванковские клетки образуют вокруг аксона тонкую оболочку, называемую неврилеммой, которая, тем не менее, содержит ядра исходных шванновских клеток. (Кстати, сам Шванн и описал эти неврилеммы, которые иногда в его честь называют шванновской оболочкой. Мне кажется, что очень немузыкально и оскорбительно для памяти великого зоолога звучит термин, которым обозначают опухоль, исходящую из неврилеммы. Ее называют шванномой.)
Одна отдельная шванновская клетка окутывает только ограниченный участок аксона. В результате шванновские оболочки охватывают аксон отдельными секциями, между которыми расположены узкие участки, в которых миелиновая оболочка отсутствует. В результате под микроскопом аксон выглядит как связка сосисок. Участки, не покрытые миелином, сужения этой связки, называются перехватами Ранвье, в честь французского гистолога Луи Антуана Ранвье, который описал их в 1878 году. Таким образом, аксон похож на тонкий стержень, продетый сквозь последовательность цилиндров вдоль их осей. Axis
на латинском языке означает «ось», отсюда происходит и название этого отростка нервной клетки. Суффикс
-он
присоединен, видимо, по аналогии со словом «нейрон».
Функция миелиновой оболочки не вполне ясна. Самое простое предположение относительно ее функции состоит в том, что она служит своеобразным изолятором нервного волокна, уменьшая утечку тока в окружающую среду. Такие утечки возрастают по мере того, как волокно становится тоньше, и присутствие изолятора позволяет волокну оставаться тонким без увеличения потери потенциала. Доказательства в пользу такого факта основаны на том, что миелин преимущественно состоит из липидных (жироподобных) материалов, которые действительно являются превосходными электрическими изоляторами. (Именно этот материал придает нерву белый цвет. Те; о нервной клетки окрашено в серый цвет.)
Однако если бы миелин выполнял только функции электрического изолятора, то с этой работой могли бы справиться и более простые жировые молекулы. Но как выяснилось, химический состав миелина очень сложен. Из каждых пяти молекул миелина две — молекулы холестерола, еще две — молекулы фосфолипидов (жировые молекулы, содержащие фосфор), а пятая молекула — цереброзид (сложная жироподобная молекула, содержащая сахар). Присутствуют в миелине и другие необычные вещества. Представляется весьма вероятным, что миелин выполняет в нервной системе отнюдь не только функции электрического изолятора.
Высказывалось предположение, что клетки миелиновой оболочки поддерживают целостность аксона, поскольку он вытянут на такое большое расстояние от тела нервной клетки, что, вполне вероятно, может утратить нормальную связь с ядром своей нервной клетки. Известно, что ядро жизненно необходимо для поддержания нормальной жизнедеятельности любой клетки и всех ее частей. Возможно, ядра шванновских клеток берут на себя функцию нянек, которые питают аксон на тех участках, которые они окутывают. Ведь аксоны нервов, даже лишенных миелина, покрыты топким слоем шванновских клеток, в которых, естественно, есть ядра.
Наконец, миелиновая оболочка каким-то образом ускоряет проведение импульса по нервному волокну. Волокно, покрытое миелиновой оболочкой, проводит импульс намного быстрее, чем волокно такого же диаметра, но лишенное миелиновой оболочки. Вот почему позвоночные выиграли эволюционную схватку с беспозвоночными. Они сохранили тонкие нервные волокна, но значительно увеличили скорость проведения импульсов по ним.
Миелинизированные нервные волокна млекопитающих проводят нервный импульс со скоростью около 100 м/с, или, если угодно, 225 миль в час. Это довольно приличная скорость. Самое большое расстрояние, которое приходится преодолевать импульсам в нервах млекопитающих, — это 25 метров, которые отделяют голову синего кита от его хвоста. Нервный импульс проходит этот неблизкий путь за 0,3 с. Расстояние от головы до большого пальца ноги у человека импульс по миелинизированному волокну проходит за одну пятидесятую долю секунды. В том, что касается скоростей передачи информации в нервной и эндокринной системах, видна огромная и вполне очевидная разница.
При рождении ребенка процесс мнелинизации нервов в его организме еще не завершен, и различные функции не развиваются должным образом до тех пор, пока нужные нервы не будут миелинизированы. Так, ребенок сначала ничего не видит. Функция зрения устанавливается только после миелинизации зрительного нерва, которая, к счастью, не заставлет себя ждать. Точно так же нервы, идущие к мышцам рук и ног, остаются не миелинизированными в течение первого года жизни, поэтому координация движений, необходимая для самостоятельного передвижения, устанавливается только к этому времени.
Иногда взрослые люди страдают так называемой «демилиенизирующей болезнью», при которой происходит дегенерация участков миелина с последующей утратой функции соответствующего нервного волокна. Лучше всего изучено одно из таких заболевании, известное как рассеянный склероз. Такое название дано этой болезни потому, что при ней в различных участках нервной системы появляются очаги дегенерации миелина с замещением его более плотной рубцовой тканью. Такая демиелинизация может развиться в результате действия на миелин какого-то белка, присутствующего в крови больного. Представляется, что этот белок является антителом, представителем класса веществ, которые в норме обычно взаимодействуют только с чужеродными белками, но часто становятся причиной симптомов состояния, которое мы знаем как аллергию. По сути дела, у больного рассеянным склерозом развивается аллергия к самому себе, и эта болезнь, быть может, является примером аутоаллергического заболевания. Поскольку чаще всего поражаются чувствительные нервы, то самыми распространенными симптомами рассеянного склероза являются двоение в глазах, утрата тактильной чувствительности и другие расстройства чувствительности. Рассеянный склероз чаще всего поражает людей в возрасте от 20 до 40 лет. Болезнь может прогрессировать, то есть могут поражаться все новые и новые нервные волокна, и в конце концов наступает смерть. Однако прогрессирование заболевания может быть медленным, и многие больные живут больше десяти лет с момента установления диагноза.
Распространение
Распространение в немиелинизированные волокне
В немиелинизированные (без`мякотному) нервном волокне ПД распространяется от точки к точке, поскольку возбуждение можно зарегистрировать как такое, что постепенно «бежит» по всему волокну от места своего возникновения. Ионы натрия, входящих внутрь возбуждении участка, служат источником электрического тока для возникновения ПД в прилегающих участках. В этом случае импульс возникает между деполяризована участком мембраны и ее невозбужденном участком. Разность потенциалов здесь во много раз выше, чем необходимо для того, чтобы деполяризация мембраны достигла предельного уровня. Скорость распространения импульса в таких волокнах 0,5-2 м / с
Распространение в миелинизированные волокне
Нервные отростки большинства соматических нервов миелинизированные. Только очень незначительные их участки, так называемые перехвата узла (перехват Ранвье), покрытые обычной клеточной мембраной. Такие нервные волокна характеризуются тем, что на мембране только в перехватах размещении потенциал-зависимые ионные каналы. Кроме того, эта оболочка повышает электрическое сопротивление мембраны. Поэтому при сдвиге мембранного потенциала ток проходит через мембрану перехватывающих участка, то есть прыжками (сальтаторно) от одного перехвата к другому, что позволяет увеличить скорость проведения нервного импульса, которая составляет от 5 до 120 м / с. Причем потенциал действия, который возник в одном из перехватов Ранвье, вызывает потенциалы действия в соседних перехвата за счет возникновения электрического поля, которое вызывает начальную деполяризацию в этих перехватов. Параметры ЭДС поля и дистанция его эффективного действия зависят от кабельных свойств аксона.
Типы нервных волокон, скорость проведения импульса, в зависимости от миелинизации
| Тип | Диаметр (мкм) | Миелинизация | Скорость проведения (м / с) | Функциональное назначение |
| А alpha | 12-20 | сильная | 70-120 | Подвижные волокна соматической НС; чувствительные волокна проприорецепторов |
| А beta | 5-12 | сильная | 30-70 | Чувствительные волокна рецепторов кожи |
| А gamma | 3-16 | сильная | 15-30 | Чувствительные волокна проприорецепторов |
| А delta | 2-5 | сильная | 12-30 | Чувствительные волокна терморецепторов, ноцицепторов |
| В | 1-3 | слабая | 3-15 | Преганглионарные волокна симпатической НС |
| С | 0,3-1,3 | отсутствует | 0,5-2,3 | Постганглионарные волокна симпатической НС; чувствительные волокна терморецепторов, ноцицепторов некоторых механорецепторов |
Задержанная постдеполяризация и триггерная поддерживающаяся ритмическая активность
частоты приводит к снижению амплитуды. Кроме того, если преждевременный потенциал действия при стимуляции возникает с постоянной частотой, то следующая за ним постдеполяризация имеет большую амплитуду, чем та, которая отмечается после регулярного потенциала действия. Более того, чем раньше во время основного цикла возникает преждевременный потенциал действия, тем больше амплитуда преждевременной постдеполяризации.
При достаточно высокой частоте постоянной стимуляции или после достаточно раннего преждевременного стимула постдеполяризация может достигнуть порога и вызвать нестимулированные потенциалы действия. Первый спонтанный импульс отмечается после более короткого интервала по сравнению с длительностью основного цикла, так как постдеполяризация, вследствие которой он возник, начинается вскоре после реполяризации предшествующего потенциала действия.
Следовательно, спонтанный импульс вызывает еще одну постдеполяризацию, которая также достигает порогового уровня, обусловливая появление второго спонтанного импульса (см. рис. 3.8). Этот последний импульс вызывает следующую постдеполяризацию, которая инициирует третий спонтанный импульс, и так на протяжении всего времени триггерной активности.
Триггерная активность может спонтанно прекратиться, и, если это происходит, за последним нестимулированным импульсом обычно следует одна или несколько подпороговых постдеполяризаций.Рис. 3.8. Индукция триггерной активности в предсердном волокне митрального клапана у обезьяны.На каждом фрагменте показаны лишь нижняя часть потенциалов действия.
Горизонтальные линии на фрагментах I и II проведены на уровне—30 мВ, а на фрагменте III — на уровне — 20 мВ. фрагмент IA и 1Б: триггерная активность, возникшая в результате сокращения длительности основного стимуляционного цикла. IA: продолжительность цикла стимуляции составляет 3400 мс; и за каждым потенциалом действия следует подпороговая задержанная постдеполяризация.
в озникновение триггерной активности вследствие преждевременной стимуляции. IIIA: преждевременный импульс (стрелка) вызывается во время фазы реполяризации постдеполяризации, и амплитуда последующей постдеполяризации возрастает. IIIБ: за преждевременным импульсом (большая стрелка) следует постдеполяризация, которая достигает порога (маленькая стрелка) и приводит к появлению ряда триггерных импульсов [40].
Распространение потенциала действия между клетками
В химическом синапсе после того, как волна потенциала действия доходит нервного окончания, она вызывает высвобождение нейротрансмиттеров из пресинаптических пузырьков в синаптическую щель. Молекулы медиатора, высвобождаемых с пресинапса, связываются с рецепторами на постсинаптической мембране, в результате чего в рецепторных макромолекулах открываются ионные каналы. Ионы, начинают поступать внутрь постсинаптической клетки через открытые каналы, изменяют заряд ее мембраны, что приводит к частичной деполяризации мембраны и, как следствие, провоцирование генерации постсинаптической клетки потенциала действия.
В электрическом синапсе отсутствует «посредник» передачи в виде нейромедиатора. Зато клетки соединены между собой с помощью специфических протеиновых тоннелей — конексонив, поэтому ионные токи, с пресинаптической клетки могут стимулировать постсинаптическую клетку, вызывая зарождения в ней потенциала действия. Благодаря такому строению, потенциал действия может распространяться в обе стороны и значительно быстрее, чем через химический синапс.
- Схема процесса передачи нервного сигнала в химическом синапсе
- Схема строения электрического синапса
Потенциал действия в различных типах клеток
Потенциал действия в мышечных тканях
Потенциал действия в скелетных мышечных клетках аналогичный потенциала действия в нейронах. Потенциал покоя в них как правило -90мВ, что меньше, чем потенциал покоя типовых нейронов. Потенциал действия мышечных клеток длится примерно 2-4 мс, абсолютный рефрактерный период составляет примерно 1-3 мс, а скорость проводимости вдоль мышц примерно 5 м / с.
Потенциал действия в сердечных тканях
Потенциал действия клеток рабочего миокарда состоит из фазы быстрого деполяризации, начальной быстрой реполяризации, которая переходит в фазу медленной реполяризации (фаза плато), и фазы быстрой конечной реполяризации. Фаза быстрой деполяризации обусловлена резким повышением проницаемости мембраны для ионов натрия, вызывает быстрый входящий натриевый ток, при достижении мембранного потенциала 30-40 мВ инактивируется и в дальнейшем главную роль играют кальциевый ионный ток. Деполяризация мембраны вызывает активацию кальциевых каналов, в результате чего возникает дополнительный Деполяризующий входящий кальциевый ток.
Потенциал действия в сердечной ткани играет важную роль в координации сокращений сердца.
В) фаза следовой реполяризации (потенциал)
Изменение проницаемости мембраны для Na продолжается недолго. Она начинает повышаться для K и снижается для Na . Это соответствует фазе реполяризации. Нисходящая часть кривой соответствует следовому потенциалу и отражает восстановительные процессы наступающие после раздражения.На кривой потенциала действия выделяют следующие фазы:1.
Локальный ответ (местная деполяризация), предшествующий развитию ПД.2.Фаза деполяризации. Во время этой фазы МП быстро уменьшается и достигает нулевого уровня. Уровень деполяризации растет выше 0. Поэтому мембрана приобретает противоположный заряд – внутри она становится положительной, а снаружи отрицательной.
Явление смены заряда мембраны называется реверсией мембранного потенциала. Продолжительность этой фазы у нервных и мышечных клеток 1-2 мсек.3.Фаза реполяризации. Она начинается при достижении определенного уровня МП (примерно 20 мВ). Мембранный потенциал начинает быстро возвращаться к потенциалу покоя. Длительность фазы 3-5 мсек.4.
Фаза следовой деполяризации или следового отрицательного потенциала. Период, когда возвращение МП к потенциалу покоя временно задерживается. Он длится 15-30 мсек.5.Фаза следовой гиперполяризации или следового положительного потенциала. В эту фазу, МП на некоторое время становится выше исходного уровня ПП. Ее длительность 250-300 мсек.
Амплитуда потенциала действия скелетных мышц в среднем 120-130 мВ, нейронов 80-90 мВ, гладкомышечных клеток 40-50 мВ. При возбуждении нейронов ПД возникает в начальном сегменте аксона – аксонном холмике.Возникновение ПДобусловлено изменением ионной проницаемости мембраны при возбуждении. В период локального ответа открываются медленные натриевые каналы, а быстрые остаются закрытыми, возникает временная самопроизвольная деполяризация.
чем она выше, тем ниже КУД и наоборот.Когда величина деполяризация приближается к равновесному потенциалу для ионов натрия ( 20 мВ), сила концентрационного градиента натрия значительно уменьшается. Одновременно начинается процесс инактивации быстрых натриевых каналов и снижения натриевой проводимости мембраны.
Деполяризация прекращается. Резко усиливается выход ионов калия, т.е. калиевый выходящий ток. В некоторых клетках это происходит из-за активации специальных каналов калиевого выходящего тока. Этот ток, направленный из клетки, служит для быстрого смещения МП к уровню потенциала покоя. Т.е. начинается фаза реполяризации.
Возрастание МП приводит к закрыванию и активационных ворот натриевых каналов, что еще больше снижает натриевую проницаемость мембраны и ускоряет реполяризацию.Возникновение фазы следовой деполяризации объясняется тем, что небольшая часть медленных натриевых каналов остается открытой.Следовая гиперполяризация связана с повышенной, после ПД, калиевой проводимостью мембраны и тем, что более активно работает натрий-калиевый насос, выносящий вошедшие в клетку во время ПД ионы натрия.
Изменяя проводимость быстрых натриевых и калиевых каналов можно влиять на генерацию ПД, а следовательно на возбуждение клеток. При полной блокаде натриевых каналов, например ядом рыбы тетродонта – тетродотоксином, клетка становится невозбудимой. Это используется в клинике. Такие местные анестетики, как новокаин, дикаин, лидокаин тормозят переход натриевых каналов нервных волокон в открытое состояние.
Поэтому проведение нервных импульсов по чувствительным нервам прекращается, наступает обезболивание (анестезия) органа. При блокаде калиевых каналов затрудняется выход ионов калия из цитоплазмы на наружную поверхность мембраны, т.е. восстановление МП. Поэтому удлиняется фаза реполяризации. Этот эффект блокаторов калиевых каналов также используется в клинической практике.
Молекулярные механизмы возникновения потенциала действия
Активные свойства мембраны, обеспечивающие возникновение потенциала действия, основанные главным образом на поведении потенциал-зависимых натриевых (Na +) и калиевых (K +) каналов. Начальная фаза ПД формируется входным натриевым током, позже открываются калиевые каналы и выходной K + -ток возвращает потенциал мембраны к исходному уровню. Начальное концентрацию ионов затем восстанавливает натрий-калиевый насос.
По ходу ПД каналы переходят из состояния в состояние: в Na + -каналов основных состояния трех — закрытый, открытый и инактивированный (в реальности все сложнее, но этих трех состояний достаточно для описания), в K + каналов два — закрытый и открытый.
Поведение каналов, участвующих в формировании ПД, описывается через проводимость и рассчитывается через коэффициенты переноса (трансфера).
Коэффициенты переноса были выведены Алан Ллойд Ходжкин и Эндрю Хаксли.
Проводимость для калия G K на единицу площади
| , |
| где: |
| an — Коэффициент трансфера из закрытого в открытое состояние для K + каналов [1 / s]; |
| bn — Коэффициент трансфера из открытого в закрытое состояние для K + каналов [1 / s]; |
| n — Фракция К + каналов в открытом состоянии; |
| (1 — n) — Фракция К + каналов в закрытом состоянии |
Проводимость для натрия G Na на единицу площади
рассчитать сложнее, поскольку, как уже было упомянуто, в потенциал-зависимых Na + каналов, кроме закрытого / открытого состояний, переход между которыми параметром, еще инактивированный / никак инактивированный состояния, переход между которыми описывается через параметр
| , | , |
| где: | где: |
| am — Коэффициент трансфера из закрытого в открытое состояние для Na + каналов [1 / s]; | ah — Коэффициент трансфера из инактивированного в не-инактивированный состояние для Na + каналов [1 / s]; |
| bm — Коэффициент трансфера из открытого в закрытое состояние для Na + каналов [1 / s]; | bh — Коэффициент трансфера из не-инактивированного в инактивированный состояние для Na + каналов [1 / s]; |
| m — Фракция Na + каналов в открытом состоянии; | h — Фракция Na + каналов в не-инактивированном состоянии; |
| (1 — m) — Фракция Na + каналов в закрытом состоянии | (1 — h) — Фракция Na + каналов в инактивированном состоянии. |
История
Основные положения мембранной теории возбуждения сформулированы немецким нейрофизиологом Ю.Бернштейном
В 1902 году Юлиус Бернштейн выдвинул гипотезу, согласно которой клеточная мембрана пропускает внутрь клетки ионы К +, и они накапливаются в цитоплазме. Расчет величины потенциала покоя по уравнению Нернста для калиевого электрода удовлетворительно совпал с измеренным потенциалом между саркоплазме мышцы и окружающей средой, который составил около — 70 мВ. Согласно теории Ю.Бернштейна, при возбуждении клетки ее мембрана повреждается, и ионы К + выходят из клетки по концентрационном градиента до тех пор, пока потенциал мембраны не становится равным нулю. Затем мембрана восстанавливает свою целостность, и потенциал возвращается к уровню потенциала покоя.
Эту модель развили в своей работе 1952 Алан Ллойд Ходжкин и Эндрю Хаксли в которой описали электрические механизмы, обусловливающие генерацию и передачу нервного сигнала в гигантском аксоне кальмара. За это авторы модели получили Нобелевскую премию в области физиологии и медицины за 1963 год. Модель получила название модель Ходжкина-Хаксли
В 2005 году Томасом Геймбургом и Анрю Д. Джексоном предложена солитонном модель, основанная на предположении, что сигнал по нейронам распространяется в виде солитонов — устойчивых волн, распространяющихся по клеточной мембране.
Влияние некоторых веществ на потенциал действия
Некоторые вещества органического или синтетического происхождения могут блокировать образование или прохождения ПД:
- Батрахотоксин найден у некоторых представителей рода листолазов. Устойчиво и необратимо повышает проницаемость мембран для ионов натрия.
- Понератоксин был найден в муравьях рода Paraponera. Блокирует натриевые каналы.
- Тетродотоксин найден в тканях рыб семейства Скелезубови, из которых готовят японский деликатес Фугу. Блокирует натриевые каналы.
- Механизм действия большинства анестетиков (Прокаин, Лидокаин) базируется на блокировании натриевых каналов и соответственно на блокировании проведении импульсов по чувствительным нервным волокнам.
- 4-Аминопиридин — обратно блокирует калиевые каналы, удлиняет срок потенциала действия. Может использоваться в терапии рассеянного склероза.
- ADWX 1 — обратно блокирует калиевые каналы. В условиях опыта облегчал течение острого рассеянного энцефаломиелита у крыс.