Атеросклероз. Эпизод I: скрытая угроза бляшек
«O pessimum periculum quod opertum latet. Самой страшной является скрытая опасность» Публилий Сир
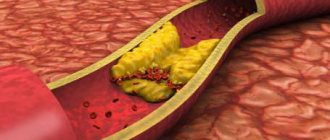
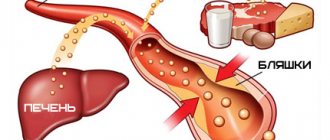
Атеросклероз — хроническая сосудистая патология, которая является причиной большинства ишемических повреждений сердечно-сосудистой системы. Термин «атеросклероз» был введен в 1904 году Маршаном и обоснован экспериментальными исследованиями Н. Н. Аничкова, поэтому также его называют болезнью Маршана-Аничкова. «Жертвами» становятся преимущественно артерии эластического и мышечно-эластического типа. Эволюция патологического каскада включает формирование эндотелиальной дисфункции, массивное отложение липидов в интиме, обострение врожденных и адаптивных иммунных реакций, пролиферацию гладких миоцитов сосудистой стенки и ремоделирования внеклеточного матрикса. Эти процессы приводят к образованию атеросклеротической бляшки (АСБ) — морфологического субстрата атеросклероза (рис.1) [1]. .
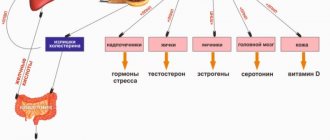
Рисунок 1 | Схема этиопатогенеза атеросклероза
Воздействие факторов риска сердечно-сосудистых заболеваний (ФР ССЗ) вызывает эндотелиальную дисфункцию и увеличивает проницаемость сосудистой стенки, обеспечивая вторжение атерогенных фракций липидов (липопротеинов низкой (ЛПНП) и очень низкой плотности (ЛПОНП)). Эндотелиопатия также способствует рекрутированию, миграции и адгезии моноцитов. Оказавшись в интиме, моноциты дифференцируются в макрофаги и поглощают модифицированные липиды, превращаясь уже в пенистые клетки. Одновременно на этой первой стадии заболевания гладкомышечные клетки (ГМК) мигрируют в интиму, где они синтезируют элементы внеклеточного матрикса (ВКМ) и способствуют образованию фиброзной капсулы. В процессе роста атеросклеротической бляшки (АСБ) количество ГМК уменьшается и пенистые клетки подвергаются апоптозу, высвобождая активные металлопротеиназы, которые разрушают фиброзную оболочку, увеличивая восприимчивость бляшки к разрыву. Происходит смена стабильного подтипа АСБ на нестабильный. Иммунная система (врожденный и приобретенный иммунитет) активно участвует в этом процессе и играет ключевую роль в уязвимости бляшек [1].
В ней выделяют липидное, или, если быть точнее, атероматозное (греч. athḗra, «кашица»), ядро, построенное из модифицированных липидов, белков, продуктов их распада, кристаллов холестерина, обломков макрофагов и гладкомышечных клеток с разрастанием вокруг него соединительной ткани (sklḗrōsis, «затвердевание») — фиброзной покрышки [2].
В ходе атеросклеротического процесса обнаруживается стадийность, с характерными патоморфологическими проявлениями (табл.1) [2].
Таблица 1 | Патоморфологическая классификация атеросклеротических повреждений. Сопоставление макро- и микроскопических стадий процесса [2]
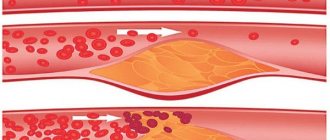
Морфологические особенности бляшки определяют степень ее «опасности» для организма. Нарушение целостности АСБ приводит к возникновению тромбогенных повреждений. В целях прогнозирования и определения верной стратегии терапии сформированные АСБ подразделяют на стабильные и нестабильные (рис. 2, 3). Основными характеристиками для классификации являются структура фиброзной покрышки и размеры липидного ядра [3]. .
Рисунок 2 | Срезы коронарной артерии с поврежденными, нестабильными и стабильными атеросклеротическими бляшками
Слева: разрыв фиброзной покрышки бляшки (красная стрелка) с наложением атероматозных масс и образованием тромба (Tр). В центре: атеросклеротическая бляшка (АСБ) с истонченной фиброзной покрышкой — нестабильный подтип. Внутри бляшки наблюдается большое атероматозное ядро (АЯ) с кровоизлияниями (геморрагиями). Белые стрелки указывают на самую тонкую часть фиброзной покрышки. Справа: стабильная АСБ, покрышка в основном состоит из фиброзной ткани с частичной кальцификацией (черные стрелки) [3].
Рисунок 3 | Микрофотографии просвета коронарной артерии с различной степенью тяжести стеноза
А-С: атеросклеротическая бляшка (АСБ) с разрывом покрышки при легком, умеренном и тяжелом стенозе соответственно (степень тяжести стеноза рассчитывалась по диаметру просвета (люминальный стеноз)). A: неокклюзионный тромб. В и С: окклюзионный тромб. D –F: нестабильная АСБ с легким, умеренным и тяжелым стенозом соответственно. Атероматозное ядро (АЯ) покрыто тонкой фиброзной покрышкой, тромбы в просвете не выявляются. G-I: стабильная АСБ с легким, умеренным и тяжелым стенозом соответственно. АЯ отсутствует или незначительного размера, часто наблюдается кальцификация (Ca++) [3].
Стабильные бляшки имеют хорошо выраженную плотную фиброзную покрышку без истончения на всем протяжении, а также небольшое атероматозное ядро. Часть бляшек вместо атероматозного ядра имеет в основании отложение солей кальция (петрификаты). Утолщенный фиброзный покров бляшки свидетельствует о хорошей репаративной функции гладкомышечных элементов интимы. Покрышка стабильных бляшек в основном представлена плотной соединительной тканью с компактно расположенными коллагеновыми волокнами, со скудным количеством липидов и клеточных элементов [4].
Расположенные в АСБ активированные макрофаги секретируют деструктивные металлопротеиназы, расщепляющие коллаген и эластин фиброзной покрышки бляшки. Преобладание этой функции усугубляет деструктивные процессы в ядре бляшки. Так формируется уязвимая нестабильная АСБ (vulnerable unstable plaque) (рис. 4) [5]. В такой бляшке высока вероятность образования тромбогенного участка. Критерии нестабильной уязвимой бляшки: наличие тонкой фиброзной покрышки (менее 65 мкм) с выраженной инфильтрацией воспалительными клетками (Т-лимфоцитами и макрофагами), крупное липидное ядро, занимающее более 30 % общей площади бляшки, массивная неоваскуляризация, с возникновением кровоизлияний из патологически сформированных неососудов, обильная инфильтрация пенистыми клетками. Также предполагается, что наличие множественных участков микрокальцификации (в отличие от обширных гомогенных очагов кальцификации) в фиброзной покрышке может увеличить риск ее разрыва. .
Рисунок 4 | «Виртуальная гистология» — данные оптической когерентной томографии
A: Тонкокапсульная фиброатерома (желтые стрелки) — атеросклеротическая бляшка с фиброзной покрышкой <65 мкм, покрывающей выраженное липидное ядро. B: Поврежденная бляшка — с разрывом фиброзной покрышки (красные стрелки) и образованием полости (красная звездочка) внутри бляшки. C: Микроканалы (белые стрелки). D: Скопления макрофагов в виде ярких пятен с высокой дисперсией сигнала (желтые стрелки). Е: Кристаллы холестерина — тонкие линейные участки высокой интенсивности сигнала внутри бляшки (красные стрелки). F: Тромб — неоформленная масса, выступающая в просвет сосуда, размер ≥ 250 мкм (белые стрелки) [5].
Уязвимые нестабильные бляшки различаются по своему «слабому звену». Выделяют фиброатерому с тонкой фиброзной покрышкой (липидный тип), бляшки с повышенным содержанием протеогликана и выраженной воспалительной реакцией, что приводит к эрозированию и тромбозу (воспалительно-эрозивный тип) и бляшки с некрозом/кальцинозом (дистрофически-некротический тип) [6].
Своевременное визуальное исследование структуры АСБ позволяет уйти от концепции «симптомных» и «бессимптомных» бляшек, формируя представление о потенциале конкретной бляшки до развития критической ситуации. Наиболее важно выяснить состояние фиброзной покрышки и уровень активности некротических процессов в ядре бляшки. Предикторами наиболее высокого риска ишемических осложнений служат наличие кровоизлияний, изъязвлений и истончений покрышки АСБ, тромбов и другого эмбологенного материала (иногда это могут быть фрагменты кальцификатов) на люменальной (обращенной к просвету сосуда) поверхности бляшки.
Источники:
- Badimon L., Vilahur G. Thrombosis formation on atherosclerotic lesions and plaque rupture. J Intern Med. 2014;276(6):618-32.
- Simionescu M., Sima A.V. Morphology of Atherosclerotic Lesions. In: Wick G., Grundtman C. (eds) Inflammation and Atherosclerosis. Springer, Vienna.2012:19-37.
- Tian J. Distinct morphological features of ruptured culprit plaque for acute coronary events compared to those with silent rupture and thin-cap fibroatheroma: a combined optical coherence tomography and intravascular ultrasound study. J Am Coll Cardiol. 2014;63(21):2209-16.
- Rognoni A. et al. Pathophysiology of Atherosclerotic Plaque Development. Cardiovasc Hematol Agents Med Chem. 2015;13(1):10-3.
- Narula J. et al. Histopathologic characteristics of atherosclerotic coronary disease and implications of the findings for the invasive and noninvasive detection of vulnerable plaques. J Am Coll Cardiol. 2013;61(10):1041–1051.
- Lee K.Y., Chang K. Understanding Vulnerable Plaques: Current Status and Future Directions. Korean Circ J. 2019;49(12):1115-1122.
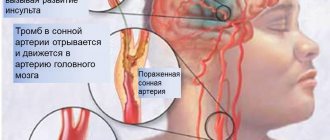
Удаление холестериновых бляшек в сонной артерии
Удаление холестериновых бляшек на сонной артерии на второй стадии (фиброза) и на третьей (кальционоза) может происходить несколькими способами:
- нагнетанием кровяного (артериального) давления – но этот путь чреват образованием новых повреждений кровеносных сосудов и, как следствие, образованием новых атеросклеротических отложений;
- расширением кровеносных сосудов, однако этот метод малоэффективен на сонной артерии и применяется чаще при варикозном расширении сосудов конечностей;
- повышением тонуса кровеносных сосудов;
- очищением крови от холестерина – однако, этот метод не столько разрушает уже существующие бляшки, сколько служит профилактикой образования новых.
Цена удаления холестериновых бляшек на сонной артерии медикаментозными средствами целиком определяется стоимостью используемых препаратов. Цена оперативного лечения (каротидная эндартерэктомия, ангиопластика, стентирование) еще выше, если делается не по страховому полюсу. К оперативному лечению прибегают, когда консервативные методы оказываются бессильны.
Под консервативными методами удаления холестериновых бляшек является прием специализированных медикаментозных препаратов, увеличение в рационе доли продуктов, очищающих сосуды от холестерина, выполнение (ежедневное) лечебных упражнений при атеросклерозе и прием статинов иди других препаратов от высокого холестерина.
Как удалить холестериновые бляшки из сонной артерии безопасно? Оперативное вмешательство имеет некоторые риски, а медикаментозное лечение – противопоказания и побочные эффекты. Медикаментозное лечение может быть направлено на снижение уровня синтеза холестерина печенью, увеличение энергетического обмена в клетках – так удается удалить из крови и сонных артерий избыточный холестерин. Альтернативой являются настои, травы от холестериновых бляшек, но их эффективность остается недоказанной.
Операция по удалению холестериновых бляшек на шее
Хирургическое вмешательство (операция) по удалению холестериновых бляшек в сосудах шеи назначается, когда медикаментозные методы лечение не принесли (или не могут принести) эффекта, или если основное заболевание привело к осложнениям. Операция по удалению холестериновых бляшек на шее не ведет к полному выздоровлению, т.к. устраняется не причина заболевания, а его следствие.
Операция по удалению холестериновых бляшек на сонной артерии называется шунтированием сонной артерии. Назначение процедуры, как и определение возможных рисков для здоровья и жизни пациента осуществляется хирургом, кардиохирургом и сосудистым хирургом. В результате операции восстанавливается проходимость сосудов для крови, т.е. выполняется реваскуляризация.
Альтернативой операции по удалению холестериновой бляшке в сонной артерии является стентирование кровеносного сосуда – это малотравматическая процедура, при которой в артерии устанавливается стент, расширяющий просвет сосуда, и специальные мембранные фильтры. Мембраны фильтруют кровь от микротромбов, но не препятствуют кровообращению в мозгу.