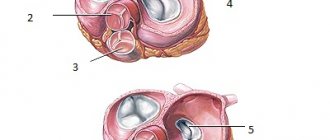
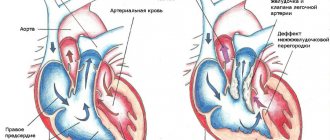
Сердечные клапаны и их дефекты
У сердца четыре камеры: по два предсердия и желудочка. Из предсердий кровь попадает в желудочки, а затем через клапаны, с помощью сокращений сердечной мышцы, поступает в артерии. Клапаны обеспечивают ток крови в нужном направлении и количестве. Если они закрываются или открываются не полностью, это препятствует нормальной циркуляции крови.
В результате сердце постепенно увеличивается в объеме и растягивается, компенсируя дефицит крови и работая с постоянной перегрузкой. Изнурительная работа сердца может стать причиной развития серьезных сердечно-сосудистых заболеваний, например, аритмии или сердечной недостаточности. Кроме того, пороки клапанов сердца могут вызвать осложнения на фоне некоторых протекающих инфекционных заболеваний.
Чаще всего пороки сердца диагностируют у пациентов старше шестидесяти лет. Причина в том, что с возрастом створки клапанного аппарата теряют эластичность, а сердце увеличивается в размерах. В результате уменьшается приток крови, и она неравномерно заполняет полости сердца — развивается сердечная недостаточность.
Существует четыре разновидности сердечных клапанов, и каждый выполняет определенную функцию:
- Аортальный: предотвращает отток крови из аорты в левый желудочек сердца.
- Митральный: предотвращает отток крови из левого желудочка сердца в левое предсердие в тот момент, когда мышца сердца сокращается, а кровь выталкивается в сосуды.
- Легочный: предотвращает отток крови из легочной артерии в правый желудочек сердца.
- Трикуспидальный: вентиль между правым желудочком сердца и правым предсердием.
Если клапаны расширены, сужены, неплотно смыкаются или надорваны, им становится трудно закрываться, а кровь при каждом сокращении сердца возвращается обратно. В результате сердце испытывает огромную нагрузку и со временем теряет свою работоспособность.
По форме заболевания пороки сердечных клапанов могут проявляться в виде:
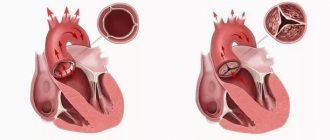
- стеноза – сужение просвета (отверстия) сосудов, по которым идет кровь. Это значительно увеличивает нагрузку на сердце, так как затрудняет выталкивание крови.
- недостаточности – повреждения створок сердечного клапана, выражающееся в их неспособности полностью закрыться. Кровь в таких случаях протекает обратно.
- сочетания стеноза и недостаточости — пораженные клапаны образуют препятствие прохождению крови. В этом случае часть крови проходит через отверстие, но возвращается обратно в следующую фазу сердечного цикла.
Публикации в СМИ
Единственный желудочек сердца (ЕЖС) — отсутствие перегородки между желудочками сердца. Основной признак — сообщение обоих предсердий через митральный и трёхстворчатый клапаны с общим желудочком. Строение сердца трёхкамерное. Частота — 1,7% всех врождённых пороков сердца (ВПС).
Классификация • Тип А — единственный правый желудочек (отсутствует приточная часть правого желудочка) • Тип В — единственный левый желудочек (отсутствует приточная часть левого желудочка) • Тип С — неразделённый или общий желудочек (отсутствует межжелудочковая перегородка) • Тип D — анатомия ЕЖС неопределённая (отсутствуют приточные части обоих желудочков и межжелудочковая перегородка).
Гемодинамика. В единственной желудочковой камере происходит смешивание артериальной и венозной крови. В аорте и лёгочной артерии (ЛА), отходящих непосредственно от желудочка, — одинаковое давление, что приводит к развитию лёгочной гипертензии.
Клиническая картина • Жалобы — одышка, тахикардия, частые респираторные заболевания, более выраженные при отсутствии стеноза ЛА • Осмотр •• Цианоз, симптомы «часовых стёкол» и «барабанных палочек», более выраженные при стенозе ЛА •• «Сердечный горб» •• Систолическое дрожание по левому краю грудины •• Аускультация — II тон над ЛА акцентирован при отсутствии её стеноза; систолический шум в III–IV межрёберных промежутках; систолический шум над верхушкой сердца (относительная митральная недостаточность); грубый систолический шум над основанием сердца соответственно уровню стеноза.
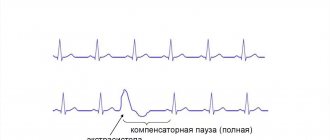
Методы исследования • ЭКГ (отклонение ЭОС вправо, гипертрофия ЕЖС: наличие ЭКГ-признаков гипертрофии одновременно правого и левого желудочков) • Рентгенологическое исследование органов грудной клетки (увеличение тени сердца в поперечнике, усиление лёгочного рисунка) • Катетеризация сердца (в полости ЕЖС высокое давление, равное давлению в аорте; повышение оксигенации крови в полости желудочка по сравнению с правым предсердием) • Ангиокардиографическое исследование позволяет определить анатомическое строение ЕЖС, расположение магистральных сосудов, выявить сопутствующие пороки • ЭхоКГ помогает выявить отсутствие межжелудочковой перегородки и наличие двух предсердно-желудочковых клапанов, открывающихся в ЕЖС.
Дифференциальная диагностика • Тетрада Фалло • Открытый общий АВ-канал • ДМЖП • Транспозиция магистральных сосудов.
ЛЕЧЕНИЕ
Медикаментозное лечение — см. Недостаточность сердечная.
Хирургическое лечение. Показания — все больные с ЕЖС.
• Паллиативные операции выполняют у детей раннего возраста и пациентов с невозможностью радикальной коррекции из-за множества сопутствующих пороков •• Хирургическое сужение ЛА проводят при резко увеличенном лёгочном кровотоке и высокой лёгочной гипертензии •• Аортолёгочный анастомоз по Блелоку–Тауссиг проводят при тяжёлом стенозе ЛА и выраженной гипоксемии.
• Радикальная операция необходима при нарастающем ухудшении состояния пациента, обусловленном прогрессирующим увеличением размеров сердца, сопротивления сосудов лёгких. В основе радикальной коррекции лежит принцип анатомического восстановления структуры сердца — создание перегородки, разделяющей ЕЖС на артериальную и венозные камеры, и устранение сопутствующих пороков сердца. Необходимыми условиями для успешного проведения операции являются достаточно большие размеры полости ЕЖС, правильно сформированные предсердно-желудочковые клапаны, нормальное расположение магистральных сосудов или синистротранспозиция аорты по отношению к лёгочному стволу. В связи с тем что имплантируемая перегородка не растёт вместе с сердцем, оптимальный возраст для операции — 10–13 лет. Если невозможно выполнить радикальную коррекцию (из-за «сидячего верхом» трёхстворчатого клапана или из-за недостаточности, гипоплазии или атрезии одного из предсердно-желудочковых клапанов) или она сопряжена с высоким риском, выполняют гемодинамическую коррекцию Фонтена (см. Атрезия трёхстворчатого клапана).
Осложнения • Сердечная недостаточность • Лёгочная гипертензия • Нарушения сердечного ритма • Послеоперационные осложнения (нарушения ритма; почечная недостаточность; частичное отхождение заплаты, разделяющий ЕЖС).
Течение и прогноз. Прогноз неблагоприятный. На первом году жизни погибает 75% больных. Средняя продолжительность жизни при естественном течении порока составляет 6–7 лет. Летальность после радикальной коррекции — до 40%, после гемодинамической коррекции при соблюдении всех критериев Шюсса (см. Атрезия трёхстворчатого клапана) — до 10%. Отдалённая смертность — 8–10%.
Синонимы • Общий желудочек • Трёхкамерное сердце с единственным желудочком • Одножелудочковое сердце • Трёхкамерное сердце с двумя предсердиями
Сокращения • ЕЖС — единственный желудочек сердца • ЛА — лёгочная артерия
Причины и симптомы
Пороки клапанов сердца могут быть врожденными и приобретенными. Главной причиной развития пороков сердечных клапанов являются ревматизм, инфекции, болезни миокарда и сердечно-сосудистой системы.
Врожденные пороки клапанов сердца развиваются еще до рождения и зависят от того, как протекала беременность. Врожденные пороки клапанов сердца — крайне редкий диагноз, который ставится лишь в 1% случаев. К врожденным дефектам относятся пороки аортального и легочного клапанов, которые лечат путем хирургического вмешательства в первые годы жизни больного.
Приобретенные. К приобретенным порокам клапанов сердца относятся трансформации клапанной структуры из-за инфекций, воспалений, перенесенных инфарктов и т.д. Большинство из них возникает вследствие постепенного изменения структуры сердца, в некоторых случаях к пороку приводит перенесенный ревматизм. У всех врожденных и приобретенных пороков смежные симптомы, которые могут проявиться в любом возрасте:
- учащение сердцебиения,
- одышка,
- отеки,
- другие проявления сердечной недостаточности.
Изначально они появляются во время физических нагрузок, но по мере развития патологий начнут возникать и в спокойном состоянии. Среди видов пороков клапана сердца чаще всего встречается пролапс митрального клапана. Он возникает во время сокращений сердца, когда происходит отвисание клапанных створок в левом предсердии. Стенки клапана теряют эластичность и он «протекает». Пролапс может быть первичным и вторичным:
- Первичный пролапс относится к врожденным клапанным порокам. Патологии соединительной ткани в этом случае являются генетической предрасположенностью.
- Вторичный пролапс — приобретенный порок. Он возникает вследствие травмирования грудной клетки, ревматизма или инфаркта миокарда.
Пролапс не несет тяжелых последствий для здоровья, а его симптомы не мешают жизнедеятельности. Однако они могут не проявляться достаточно долго и чаще всего беспокоят в пожилом возрасте, из-за чего их списывают «на возраст». Если вовремя не обратить внимание на симптомы, то могут возникнуть осложнения, например, аритмия и сердечная недостаточность.
Среди симптомов также наблюдаются жалобы на болезненные ощущения в области сердца. Они возникают на фоне переживаний, не связаны с физической нагрузкой и не снимаются медикаментозно. Боли неинтенсивные, но длительные, сопровождаются тревогой и учащенным сердцебиением.
Аритмогенная дисплазия правого желудочка
По клинической картине выделяют 4 типичные формы течения этого заболевания: скрытая форма, при которой ВСС вследствие фибрилляции желудочков является первым проявлением заболевания; аритмическая форма, характеризующаяся наличием документированных симптоматичных желудочковых тахиаритмий (желудочковой экстрасистолии и желудочковой тахикардии) с конфигурацией комплекса QRS по типу блокады левой ножки пучка Гиса; «paicisymptomatic form» – форма с симптомами средней степени тяжести, такими как приступы сердцебиения, боль в области сердца; форма, проявляющаяся сердечной недостаточностью (СН), преимущественно правожелудочковой, с наличием или отсутствием нарушений ритма сердца.
Наиболее частыми проявлениями АДПЖ являются желудочковые аритмии с ЭКГ морфологией по типу блокады левой ножки пучка Гиса, изменения деполяризации и реполяризации миокарда желудочков, выявляемые в правых прекордиальных отведениях, а также нарушения глобальной и/или локальной сократимости ПЖ и изменения структуры его миокарда по данным электрокардиографии (ЭхоКГ), магнитно-резонансной томографии (МРТ). Следует отметить, что существует немало случаев бессимптомного течения заболевания, когда первым и, возможно, единственным его проявлением бывает внезапная смерть.
У значительной части больных АДПЖ остается нераспознанной, несмотря на имеющиеся клинические и инструментальные признаки. Заболевание может прогрессировать и приводить со временем к вовлечению в патологический процесс миокарда ЛЖ. В клинической картине у таких больных доминируют признаки недостаточности кровообращения наряду с желудочковыми аритмиями.Островки фиброзно-жировой ткани, обнаруживаемые при АДПЖ, формируют аритмогенный субстрат, несущий в себе электрофизиологические условия развития повторного входа волны возбуждения (re-entry), лежащего в основе злокачественных желудочковых тахиаритмий (ЖТ).
Аритмии индуцируются при адренергической стимуляции, например, при инфузии катехоламинов или при физической нагрузке. 80% больных демонстрируют появление желудочковой экстрасистолии либо ЖТ на фоне инфузии изопротеренола. При анализе холтеровских мониторных записей ЭКГ пациентов с устойчивой ЖТ отмечается увеличение частоты синусового ритма, предшествующее пароксизму ЖТ, как отражение активации симпато-адреналовой системы. Желудочковая тахикардия у пациентов с АДПЖ обычно имеет ЭКГ морфологию блокады левой ножки пучка Гиса, что указывает на происхождение аритмии из миокарда ПЖ. Нередко регистрируется несколько морфологий ЖТ, так как при данном заболевании могут формироваться множественные аритмогенные очаги. Больные с АДПЖ и их родственники часто имеют в анамнезе указания на синкопальные состояния неуточненной этиологии. Обмороки, как проявление тяжелых аритмических событий, могут возникать задолго до развития характерных клинико-инструментальных признаков АДПЖ. В последующем в этих случаях наблюдаются прогрессирующие изменения ЭКГ и параметров ЭхоКГ, свойственные данному заболеванию.
Внезапная смерть может быть первым и единственным проявлением АДПЖ, особенно у молодых людей и спортсменов. Все пациенты с уже диагностированной АДПЖ или с подозрением на таковую должны расцениваться, как лица с повышенным риском внезапной смерти, даже при отсутствии документированных желудочковых нарушений ритма сердца. По данным американских авторов, АДПЖ посмертно диагностируется примерно в 5% случаев внезапной смерти среди лиц моложе 65 лет и в 3–4% случаев смерти молодых спортсменов во время соревнований или тренировок.
В регионе Венето в Италии, являющемся эндемичным для этой патологии, АДПЖ в 20% случаев служит причиной внезапной смерти у людей моложе 35 лет. Годовая частота случаев ВС при АДПЖ достигает 3% без лечения и может быть снижена до 1% при условии проведения ее первичной или вторичной профилактики средствами фармакотерапии. В подавляющем большинстве случаев механизмом ВС является акселерация ритма ЖТ и трансформация ее в фибрилляцию желудочков. Peters S. с соавт. проанализировали данные 121 пациента с верифицированным диагнозом АДПЖ и выявили следующие маркеры повышенного риска развития жизнеугрожающих желудочковых аритмий и ВС: мужской пол, максимальная продолжительность комплекса QRS в правых прекордиальных отведениях >110 мс, увеличение размеров ПЖ по данным ЭхоКГ, рентгенконтрастной вентрикулографии, признаки вовлечения в патологический процесс миокарда левого желудочка (ЛЖ), дисперсия интервала JT в левых прекордиальных отведениях > 30 мс, инверсия зубцов Т в прекордиальных отведениях ЭКГ далее V3, дисперсия продолжительности комплекса QRSі50 мс.Выявление этих признаков представляется наиболее значимым для бессимптомных пациентов с АДПЖ. Своевременное назначение таким больным средств профилактики развития фатальных аритмий позволяет существенно улучшить прогноз их жизни. Пациенты с АДПЖ могут демонстрировать симптомы изолированной правожелудочковой, реже бивентрикулярной СН, которые появляются, как правило, в возрасте 40–50 лет. АДПЖ – первичное заболевание миокарда, приводящее к правожелудочковой недостаточности в отсутствие легочной гипертензии. Патогенез развития правожелудочковой недостаточности при данной патологии состоит в дилатации, истончении стенки и прогрессивном снижении сократимости миокарда ПЖ вследствие его атрофии. Вовлечение в процесс папиллярных мышц сопровождается развитием трикуспидальной регургитации.
Признаки правожелудочковой недостаточности манифестируют, как правило, через 4–8 лет после появления полной блокады правой ножки пучка Гиса – одного из характерных электрокардиографических маркеров поражения миокарда ПЖ и его структур проводящей системы сердца. Диспластический процесс может захватывать и миокард ЛЖ, приводя к снижению его сократительной способности, однако левожелудочковая недостаточность менее свойственна данному заболеванию. Развитие левожелудочковой недостаточности может создавать предпосылки для диагностических ошибок. Например, часто вместо АДПЖ диагностируют идиопатическую дилатационную кардиомиопатию (ДКМП), либо ДКМП, как исход вирусного миокардита.
Левожелудочковая дисфункция при АДПЖ отражает бивентрикулярную дисплазию и должна быть дифференцирована от любых других первичных заболеваний миокарда, протекающих с вовлечением в патологический процесс обоих желудочков и проявляющихся развитием дилатации и снижением сократимости. Достоверная диагностика АДПЖ имеет принципиально важное значение вследствие высокой предрасположенности пациентов с этой патологией к возникновению злокачественных ЖТ, которые нередко бывают резистентны к медикаментозной терапии и требуют в значительной части случаев использования специальных методов нелекарственного лечения.
В некоторых случаях дополнительные диагностические трудности у больных с АДПЖ создают боли в области сердца, которые далеко не всегда возникают при нагрузке, но порой могут быть купированы применением нитратов. У таких пациентов гистологические исследования выявляют пролиферацию медии с почти полной обструкцией дистального коронарного русла, погруженного в жировую ткань. Данные изменения могут служить объяснением развития синдрома стенокардии при АДПЖ.
ТЕЧЕНИЕ И ПРОГНОЗ
Важной клинической особенностью заболевания, определяющей прогноз, являются желудочковые аритмии и правожелудочковая недостаточность. По данным Саги и соавт. (1993), при эффективной антиаритмической терапии, а также при использовании хирургических методов лечения (аблация аритмогенных зон) 10-летняя выживаемость составляет 77%. Lecleroq и соавт. (1991) сообщают о том, что летальность при аритмогенной дисплазии миокарда правого желудочка составляет 9% за 5 лет. При эффективной антиаритмической терапии, по данным серийного электрофизиологического тестирования, больные имеют хороший долговременный прогноз при продолжающемся приеме антиаритмического препарата и отсутствии прогрессирования патологического процесса в правом желудочке, правожелудочковой недостаточности. При неконтролируемой эмпирической терапии летальность возрастает до 20% в первые 10 лет (2,5% в год). Основная причина смерти больных — фибрилляция желудочков.
Диагностика и лечение
Если вы или ваши близкие испытываете описанные выше симптомы, рекомендуем пройти диагностику. Во время диагностики врач отслеживает показатели сердца в состоянии покоя и при физических нагрузках.
Пациенту назначают:
- суточное мониторирование ЭКГ,
- эхокардиографию (ЭХО-КГ),
- рентгенографию грудной клетки,
- КТ и МРТ на специальном оборудовании, позволяющем исследовать сердце фактически между ударами.
Такая диагностика осуществляется не только при первичном обследовании пациентов с подозрением на заболевание, но и в диспансерных группах больных с уже подтвержденным диагнозом.
В зависимости от результатов диагностики, врач назначает необходимое лечение: терапию или хирургическое вмешательство.
- Терапия направлена на предупреждение, профилактику и облегчение рецидивов того заболевания, которое стало первопричиной дефекта, а также лечение сердечной недостаточности.
- Хирургическое вмешательство — крайняя необходимость, которая в силу возраста или осложнений может быть назначена не всем пациентам.
Как правило, пороки клапанов сердца — механическая проблема, решить которую можно только с помощью проведенной хирургом операции. При стенозах показана операция по разделению сросшихся створок клапана и расширению атриовентрикулярного отверстия — комиссуротомия. При недостаточности проводят протезирование: замену на биологический или механический аналог.
Единственный желудочек сердца
Причины возникновения порока
В норме сердце имеет два хорошо развитых желудочка (правый и левый), которые работают как насосные камеры, изгоняя кровь в малый (к легким) и большой (к остальным органам) круги кровообращения. В случае, когда один желудочек развит неправильно или имеет недостаточный размер (гипоплазирован), хорошо развитый желудочек берет на себя его функцию и работает на оба круга кровообращения, что приводит к его перегрузке и быстрому истощению. При этом венозная (бедная кислородом) и артериальная (насыщенная кислородом) кровь смешиваются, и ко всем органам поступает кровь с недостаточным содержанием кислорода в крови, что и определяет наличие цианоза у этих детей.
Диагностика
Пациенты с единственным желудочком сердца требуют комплексного подхода в диагностике и лечении столь сложной сердечной патологии. Этим пациентам необходимо полное обследование всей сердечно-сосудистой системы для оценки анатомии порока и его гемодинамических характеристик.
Пациентам с подозрением на наличие данной патологии выполняется диагностическое исследование с использованием самых новых технологий и обязательно включает в себя трансторакальное ЭхоКГ (при необходимости чреспищеводное ЭхоКГ), катетеризация сердца с ангио-кардиографией и прямой тензиометрией, МСКТ.
Методы лечения
Все дети с диагностированным единственным желудочком сердца нуждаются в хирургическом лечении, основной целью которого является создание условий, позволяющих единственному желудочку работать только на большой круг кровообращения и доставлять кровь, насыщенную кислородом, ко всем органам, в то время как к легочным сосудам кровь поступает в обход сердца.
Рис. Двунаправленный кавопульмональный анастомоз (операция Гленна)
Первым этапом выполняется формирование двунаправленного каво-пульмонального анастомоза (ДКПА) (операция Гленна), направляя часть венозной крови, поступающей из верхней полой вены, непосредственно в легочные артерии. Это уменьшает приток крови к единственному желудочку, снижает на него нагрузку и обеспечивает лучшее насыщение крови кислородом.
Рис. Операция Фонтена
Следующим этапом формируется полный каво-пульмональный анастомоз (операция Фонтена), перемещая венозную кровь из нижней полой вены в легочные артерии с помощью сосудистого протеза. В результате вся венозная кровь сразу поступает к легким, где насыщается кислородом, минуя сердце. Из легких богатая кислородом кровь поступает в камеры сердца, и единственный желудочек выбрасывает ее в большой круг кровообращения ко всем органам и жизненно-важным системам организма. Это процедура позволяет максимально снизить нагрузку на единственный желудочек и обеспечивает хорошее насыщение крови кислородом (нет смешивания крови).
Таким образом, операция Фонтена
заключается в гемодинамической коррекции, которая позволяет направить венозную, необогащённую кислородом кровь, напрямую в лёгочную артерию.
Наблюдение пациентов в послеоперационном периоде
Поддержание сбалансированного легочного и системного кровотоков является залогом хорошего результата операции, поэтому после выполнения каждого из этапов лечения (ДКПА, ПКПА) всем пациентам необходимо регулярное наблюдение и полное обследование, для выявления проблем со стороны единственного желудочка и легочных сосудов.