- Как проявляется?
- Из-за чего скапливается жидкость?
- Факторы риска
- Классификация и виды
- Как лечить?
- Клинический случай
- Из-за чего при раке развивается асцит?
- Особенности лечения асцита у онкобольных
- Консервативная терапия
- Хирургическое лечение
- Методы диагностики
- Возможные осложнения
- Прогноз
- Профилактика
- Цены
Врачи «Евроонко» специализируются на работе с пациентами, имеющими асцит. У нас следующие особенности лечения данного заболевания:
- Мы проводим комплексное лечение. При лапароцентезе (проколе брюшной стенки для удаления жидкости из живота) мы устанавливаем временные или постоянные перитонеальные катетеры, а также порт-системы. Это позволяет не ограничивать пациента в движении.
- Если это показано, пациенту назначают специальное питание с ограничением водно-солевой нагрузки.
- Если данное состояние возникло на фоне онкологического заболевания, может быть проведена химиотерапия. Благодаря этому мы достигаем улучшения состояния таких пациентов при прогрессирующем раке яичников и толстой кишки.
- Эффективна внутриполостная химиотерапия. После удаления жидкости в брюшную полость вводится химиопрепарат. Примерно в половине случаев повторная эвакуация жидкости не требуется, как минимум 2 месяца.
Когда пациент с онкологическим заболеванием и асцитом переходит на комплексную терапию, лапароцентез требуется в 2–3 раза реже, чем обычно.
Как проявляется?
Наличие в брюшной полости небольшого количества жидкости никак не проявляет себя клинически. Кроме того, в норме в сутки организм человека производит и поглощает в брюшной полости примерно 1,5 л жидкости. При начальной стадии данного состояния особых жалоб у пациентов нет, и обнаружить жидкость можно только во время ультразвукового исследования.
Когда заболевание прогрессирует, жидкости в брюшной полости становится больше, человек чувствует тяжесть в области живота, а в нижней его части — тупые ноющие боли. Впоследствии возникает затруднение дыхания, расстройство пищеварения (тошнота, отрыжка, нарушения стула) и нарушение мочеиспускания. В наиболее тяжёлых формах значительно ухудшается самочувствие, в животе появляются неприятные ощущения, возникает одышка, происходит раннее насыщение, формируется пупочная грыжа, появляются отеки нижних конечностей.
В брюшной полости может скопиться 5–10 л жидкости, а иногда и 20 л. Из-за этого сильно сдавливаются внутренние органы, повышается внутрибрюшное давление, и диафрагма оттесняется в грудную полость. Это влечёт за собой сильное затруднение дыхания. Из-за того, что в органах брюшной полости увеличивается сопротивление кровотоку, возникает сердечная недостаточность. Следствием длительно существующего асцита становится нарушение дренирования лимфатической системы. Из-за этого также возникает нарушение лимфооттока в нижних конечностях и, как следствие, их отёк. Также может произойти обратный ход лимфы во внутренние органы. В результате раковые клетки попадают в здоровые органы из поражённых лимфоузлов. Это может спровоцировать развитие метастазов в печени, желудке, поджелудочной железе и других органах. [4,8]
Когда в брюшной полости находится более одного литра жидкости, это можно заметить при обычном осмотре: живот увеличен или деформирован, в вертикальном положении выглядит отвисшим, в лежачем положении живот распластан, боковые отделы выглядят набухшими (так называемый «лягушачий живот»). У худых пациентов нередко выпирает пупок. У человека может также возникнуть гидроторакс — присутствие жидкости в плевральной полости. Обычно это состояние развивается у пациентов с застойной сердечной недостаточностью при длительно существующем асците.
Небольшой или умеренный асцит развивается у 15–50 процентов пациентов на ранних стадиях рака. Тяжелый встречается на поздних стадиях у 7–15 процентов пациентов. [1]
У пациентов с распространенным раком на поздней стадии чаще всего встречается экссудативный плеврит.
Запись на консультацию круглосуточно
+7+7+78
Лечение отечного синдрома при хронической сердечной недостаточности
Для цитирования. Ефремова Ю.Е. Лечение отечного синдрома при хронической сердечной недостаточности // РМЖ. 2015. № 27. С. 1622–1624.
Согласно рекомендациям Европейского общества кардиологов, сердечная недостаточность определяется как следствие нарушений структуры и функции сердца, которые приводят к неспособности сердца доставлять кислород со скоростью, сопоставимой с метаболическими потребностями тканей, несмотря на нормальное давление наполнения [1]. Хроническая сердечная недостаточность (ХСН) – это синдром, к которому приводят различные причины поражения миокарда. Основными причинами ХСН являются ишемическая болезнь сердца и артериальная гипертония (АГ), реже – кардиомиопатии, клапанные пороки сердца, болезни перикарда и др. Частота распространенности ХСН в возрастной группе 25–54 лет составляет 1%, в группе 65–74 лет – 4–5%, около 10% – у лиц старше 75 лет. По сравнению с периодом 20-летней давности имеются данные о 4-кратном увеличении госпитализаций по поводу ХСН. Частично это объясняется увеличением средней продолжительности жизни [2]. По результатам российского эпидемиологического исследования ЭПОХА-ХСН, распространенность ХСН в России составляет в среднем 7,9%, в т. ч. клинически выраженная – 4,5%, увеличиваясь от 0,3% в возрастной группе от 20 до 29 лет до 70% у лиц старше 90 лет [3]. Наличие сердечной недостаточности повышает риск смерти в 4 раза. Лечение пациентов с ХСН – сложная задача современной медицины, поскольку сердечная недостаточность является лишь синдромом, который может развиться как осложнение многих заболеваний сердечно-сосудистой системы. Терапия больного с ХСН в первую очередь должна включать в себя лечение основного заболевания. Основная цель лечения ХСН – снижение смертности, а также [2]: – уменьшение клинических симптомов ХСН; – уменьшение частоты развития основных осложнений; – поддержание или улучшение качества жизни больного; – улучшение функции левого желудочка; – увеличение переносимости физической нагрузки; – уменьшение потребности в госпитализации; – предотвращение побочных эффектов терапии. Медикаментозное лечение ХСН включает в себя большое количество препаратов, самыми распространенными из которых являются ингибиторы ангиотензин-превращающего фермента (ингибиторы АПФ); блокаторы рецепторов к ангиотензину II; диуретики; β-адреноблокаторы и антагонисты рецепторов минералокортикоидов (антагонисты альдостерона). Применение определенного препарата при лечении ХСН направлено на решение конкретных задач. Рассмотрим подробнее лечение отечного синдрома при ХСН с помощью диуретической терапии. Периферические отеки при сердечной недостаточности являются следствием задержки жидкости, вызванной сниженным почечным кровотоком и нейрогормональными изменениями. Преимущественно они развиваются на нижних конечностях. При значительной задержке жидкости возможно наличие асцита и/или гидроторакса. Для лечения отечного синдрома применяются диуретики. Препараты этого класса показаны всем больным при клинических симптомах ХСН, связанных с избыточной задержкой натрия и воды в организме [4]. Диуретики применяются для симптоматического лечения ХСН. Они препятствуют задержке жидкости в организме, увеличивают экскрецию соли и воды, что приводит к уменьшению застойных явлений. На фоне их использования снижается общее периферическое сосудистое сопротивление, уменьшается пред- и постнагрузка, в связи чем уменьшается дилатация левого желудочка. Существуют 5 классов мочегонных средств (табл. 1), которые действуют на различные части петли Генле. При начальных стадиях ХСН возможно применение тиазидных диуретиков. При тяжелой ХСН возможна комбинация петлевых и тиазидных диуретиков, что приводит к усилению мочегонного эффекта. При выраженном отечном синдроме и/или декомпенсации ХСН целесообразно введение диуретиков парентерально. Петлевые диуретики фуросемид и торасемид являются наиболее часто используемыми диуретиками при ХСН.
Торасемид используется в клинической практике с 1980-х гг. При отечном синдроме данный препарат назначается по 5 мг утром после еды; при необходимости дозу увеличивают до 20 мг 1 р./сут. По сравнению с фуросемидом торасемид характеризуется более высокой биодоступностью, которая не уменьшается при отечном синдроме, меньше влияет на концентрацию в плазме калия, магния, действует длительнее и обладает антиальдостероновыми свойствами (блокада рецепторов альдостерона на мембранах эпителиальных клеток почечных канальцев и снижение секреции альдостерона в надпочечниках). К плейотропным свойствам торасемида относят способность данного препарата ингибировать синтез и депозицию коллагена 1 типа в миокарде у пациентов с ХСН. Кроме того, в отличие от пациентов, получающих фуросемид, у пациентов в группе торасемида снижается концентрация в сыворотке крови C–терминального пропептида проколлагена 1 типа (маркера миокардиального фиброза) [6]. Торасемид снижает смертность, а также частоту и продолжительность госпитализаций по поводу ХСН. Кроме того, он приводит к повышению переносимости физической нагрузки, улучшает функциональный класс (ФК) ХСН (по NYHA) и качество жизни пациентов. В исследовании TORIC среди 1377 пациентов с ХСН торасемид привел к достоверному снижению сердечно-сосудистой смертности в сравнении с фуросемидом [7]. В этом исследовании были проанализированы результаты 9–месячного сравнительного лечения торасемидом в суточной дозе 10 мг и фуросемидом 40 мг больных с ХСН. В группе больных, получавших терапию торасемидом, значительно чаще улучшился ФК недостаточности кровообращения и достоверно снизилась сердечно-сосудистая и общая смертность. В последнее время на российском рынке лекарственных средств появился торасемид замедленного высвобождения – Бритомар
®. Препарат обеспечивает постепенное высвобождение активного вещества. Благодаря этому снижаются колебания концентрации препарата в крови по сравнению с обычной формой. Бритомар® – таблетка на основе гидрофильной матрицы из гуаровой камеди, которая является натуральным водорастворимым полимером, получаемым из семян растения семейства бобовых. В фармацевтической промышленности гуаровая камедь широко используется при создании лекарственных форм с пролонгированным высвобождением. В желудочно-кишечном тракте она образует подобие губки, которая обеспечивает замедленное высвобождение препарата. Лекарственное вещество высвобождается более длительно, благодаря этому диурез начинается примерно через 1 ч после приема препарата, достигая максимума через 3–6 ч, длится эффект от 8 до 10 ч. Замедленное высвобождение препарата позволяет добиться дополнительных клинических преимуществ в лечении отечного синдрома при ХСН. Торасемид при долгосрочном применении не вызывает изменений уровня калия крови, не оказывает заметного влияния на уровень кальция и магния, показатели гликемического и липидного профиля [8]. Препарат не взаимодействует с антикоагулянтами (варфарином), сердечными гликозидами или органическими нитратами, другими препаратами, наиболее часто применяемыми при лечении ХСН, такими как β-адреноблокаторы, иАПФ, блокаторы рецепторов к ангиотензину II и антагонисты рецепторов минералокортикоидов. Торасемид пролонгированного действия в сравнении с другими мочегонными препаратами изучался в ряде исследований. Так, в российском одноцентровом рандомизированном открытом исследовании изучалась сравнительная эффективность торасемида пролонгированного действия и фуросемида у пациентов с ХСН II–III ФК, отечным синдромом и повышенным уровнем натрийуретических пептидов [9]. В исследование были включены 40 пациентов с ХСН ишемической этиологии с фракцией выброса левого желудочка менее 40%, разделенных методом рандомизации на 2 равные группы: 1-я получала торасемид пролонгированного действия (Бритомар®), 2-я – фуросемид. В обеих группах на фоне лечения наблюдали достоверное улучшение переносимости физической нагрузки, улучшение качества жизни больных, снижение концентрации натрийуретических гормонов. В группе торасемида замедленного высвобождения были выявлены тенденция к более значимому улучшению качества жизни (р=0,052) и достоверно более значимое снижение уровней NT-промозгового натрийуретического пептида (р<0,01). Это может быть связано с тем, что пролонгированное высвобождение торасемида характеризуется медленным началом действия, не приводит к развитию императивных позывов к мочеиспусканию и отличается большей длительностью действия по сравнению с лекарственной формой стандартного высвобождения [9]. Также в этом исследовании изучались данные о влиянии схем диуретической терапии на электролитный профиль пациентов. Концентрацию калия и натрия определяли исходно, через 2, 4 и 12 нед. лечения. В группе торасемида замедленного высвобождения не было отмечено случаев изменений электролитного профиля по сравнению с нормальными значениями. В группе фуросемида у 3 (15%) пациентов наблюдалось уменьшение содержания калия ниже нормальных границ (3,5 ммоль/л), в 1 случае потребовавшее коррекции дозы антагонистов альдостерона и внутривенной инфузии солей калия. Несомненно, снижение частоты гипокалиемии также оказывает свое влияние как на самочувствие пациентов, так и на частоту потенциальных осложнений терапии. На фоне приема пролонгированного торасемида можно избежать феномена повышенной постдиуретической реабсорбции натрия. Отсутствие быстрого увеличения объема выделяемой мочи не вызывает резкого изменения объема циркулирующей крови, а значит, не потенцирует избыточный синтез А–II и норадреналина, которые приводят к снижению скорости клубочковой фильтрации и ухудшению почечной функции. Преимущества торасемида замедленного высвобождения в сравнении с торасемидом со стандартным высвобождением были показаны в ряде исследований. В исследовании M.J. Barbanoj et al. проводилась сравнительная оценка биодоступности и биоэквивалентности и оценивались фармакокинетика и фармакодинамика торасемида замедленного и стандартного высвобождения [11]. Сравнивались 2 дозы пролонгированного торасемида с аналогичными дозировками торасемида. В исследовании приняли участие 20 здоровых волонтеров (2 группы, 10 человек в каждой). В результате торасемид замедленного высвобождения показал достоверно более длительное tmax в сравнении с таковым торасемида. Количество торасемида, выявленного в моче через 24 ч после введения, было выше в группе торасемида замедленного высвобождения при обеих дозировках. Объем мочи и экскреция электролитов с мочой были меньше в группе торасемида замедленного высвобождения в течение первого часа после приема, однако натрийурез в этой группе был достоверно больше. Таким образом, несмотря на то, что обе формы показали сходное системное распределение (AUC), у торасемида замедленного высвобождения был меньший уровень абсорбции (меньшее C (max) и удлиненный t (max)). В пилотном исследовании Г.П. Арутюнова и соавт. также проводилось сравнение торасемида замедленного высвобождения с торасемидом стандартного высвобождения [12]. В данное открытое рандомизированное сравнительное клиническое исследование в параллельных группах были включены пациенты с ХСН I–II ФК (NYHA) и эссенциальной АГ II–III степени. Методом случайных чисел пациенты были распределены на 2 группы лечения – лечения Бритомаром и торасемидом стандартного высвобождения. Период лечения длился 40 дней. В результате было показано, что суммарный натрийурез в 1-е сут назначения Бритомара и торасемида стандартного высвобождения был больше во второй группе, однако важно, что в группе Бритомара наблюдался плавный натрийурез в течение суток без пиков, в отличие от стандартной формы торасемида, при назначении которого возникают пикообразное повышение натрийуреза на 3 ч и резкое его снижение уже на 6 ч с дальнейшим прогрессирующим снижением. Также было показано, что натрийурез вслед за однократным приемом петлевого диуретика длился лишь несколько часов, а через 5–6 ч экскреция натрия с мочой приближалась к уровню, сопоставимому с уровнем при применении плацебо, т. е. с 6 по 24 ч даже торасемид неэффективен, а кумулятивный его натрийурез сопоставим с таковым гидрохлортиазида именно за счет наличия антинатрийуретического периода. Было продемонстрировано благоприятное влияние Бритомара на показатели центральной гемодинамики, что авторы связывают с отсутствием рикошетной ретенции натрия при применении данного диуретика, а значит, повышения жесткости сосудистой стенки. Таким образом, торасемид с замедленным высвобождением вследствие своих фармакодинамики и фармакокинетики является препаратом высокой степени эффективности в лечении отечного синдрома при ХСН и позволяет улучшить качество жизни больных и переносимость терапии.
Из-за чего скапливается жидкость?
Патологическое скопление жидкости в брюшной полости происходит при некоторых заболеваниях, при которых нарушается регуляция водно-солевого обмена и нормальная циркуляция. Причиной могут быть:
- Онкологические заболевания: вторичный канцероматоз брюшины, лимфома и лейкоз, метастазы в области ворот печени, первичная мезотелиома.
- Болезни печени и её сосудов: рак печени, портальная гипертензия, цирроз печени, вено-окклюзионная болезнь, болезнь Бадда — Киари.
- Перитонит (воспаление брюшины) различного происхождения: панкреатический, грибковый, паразитарный, туберкулёзный.
- Застойная сердечная недостаточность, констриктивный перикардит.
- Другие болезни: опухоли и кисты яичников (синдром Мейгса), киста поджелудочной железы, болезнь Уиппла, саркоидоз, системная красная волчанка, микседема.
В «Евроонко» проводится лечение асцита различного происхождения. Но так как основная наша работа связана с лечением злокачественных новообразований, значительную часть наших пациентов составляют онкобольные. [4,5]
Причины патологии у взрослых
Во многих случаях, патология развивается как симптом ряда заболеваний, среди которых:
- Портальная гипертензия;
- Цирроз;
- Гепатиты;
- Тромбоз вен печени.
Не исключена, как причина патологии и онкология крови, а также патологии, природа которых с опухолью ничего общего не имеет. Сердечная недостаточность также может стать причиной патологии.
Проблемы, связанные с лимфообращением, деятельностью таких органов, как щитовидная железа, почки, также могут стать причинами патологии.
Белковая недостаточность
Факторы риска
Среди факторов риска развития асцита наибольшее значение имеют патологии, способные приводить к циррозу печени. В первую очередь, это вирусные гепатиты B и C, алкогольный гепатит. Другие наиболее распространенные факторы риска:
- застойная сердечная недостаточность;
- почечная недостаточность;
- ожирение;
- сахарный диабет II типа;
- повышенный уровень «плохого» холестерина в крови. [11]
Рисковые факторы
Главным рисковым фактором выступает злокачественная опухоль. Сама брюшина выглядит как листок, покрытый слизистой оболочкой, и является идеальным местом для развития метастазов.
Они проникают туда через кровеносные сосуды, оторвавшись от опухолевого очага, и вынуждают серозу к воспроизводству избыточной жидкой массы.
К тому же в лимфососудах атипичные клетки разрастаются и перекрывают их, тем самым нарушают всасывание жидкой массы.
К факторам, которые способствуют скоплению избыточной жидкой массы при онкологии, являются:
- Цирроз;
- Дисфункция печени как результат заболевания хронического характера либо токсического гепатита;
- Болезни сердца, которые замедляют кровоток;
- Сбой выделительной функции почек как результат химиотерапии;
- Повышенное тромбообразование сосудов полости брюшины;
- Изменение белкового состава крови как следствие карциномы ЖКТ.
Классификация и виды
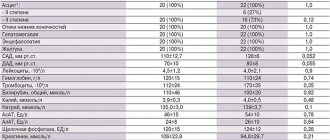
Классически, в зависимости от уровня белка в асцитической жидкости, асцит делят на экссудативный (25 г/л и более) и транссудативный (< 25 г/л). Это позволяет косвенно судить о причинах. В настоящее время применяют более точный показатель — градиент «сывороточный альбумин — альбумин асцитической жидкости» (SAAG):
- При SAAG более 1,1 причиной асцита, как правило, являются такие патологии, как цирроз, застойная сердечная недостаточность, болезнь Бадда — Киари. Они связаны с повышением давления в воротной вене.
- При SAAG менее 1,1 можно предположить, что скопление жидкости в животе вызвано панкреатитом или онкологическим заболеванием.
По клиническому течению выделяют следующие разновидности асцитов:
- В зависимости от тяжести течения:
- 1 степень. Клинические проявления отсутствуют, диагноз устанавливают по данным УЗИ (определение уровня свободной жидкости в брюшной полости).
- 3 степень. Значительное визуальное увеличение живота.
2 степень. Небольшое визуальное увеличение живота.
- Резистентный к диуретикам: неэффективно лечение мочегонными препаратами в сочетании с диетой, при которой потребление хлорида натрия ограничено до менее 2 г в сутки (отсутствие результата после 1 недели терапии).
Неконтролируемый диуретиками: невозможно применять мочегонные средства, потому что они вызывают выраженные побочные эффекты. [6,7]
Диета
Очень важная цель – восстановление питательного статуса и нормализация уровня белков, которые были утрачены при эвакуации жидкой массы.
Требуется ограничение потребления жидкости и соли. Из рациона больного необходимо исключить консервы, маринады и фастфуд, так как в них соль в избытке.
Недостаточный уровень белка компенсируется капельницами и подобранным рационом питания. Пациентам с раковыми заболеваниями необходимо потреблять белок из расчёта полтора грамма на каждый килограмм веса.
Как лечить?
Есть несколько основных методов лечения асцита у пациентов с онкологическими заболеваниями:
- консервативная терапия (антагонисты альдостерона, мочегонные препараты) — направлена на нормализацию водно-солевого обмена и уменьшение образования жидкости в брюшной полости;
- лапароцентез — прокол брюшной стенки под контролем ультразвука; используется не только для выведения жидкости, но и для установки дренажа, который будет служить для продолжительного вывода жидкости;
- паллиативные хирургические операции — перитонеовенозный шунт, оментогепатофренопексия, деперитонизация стенок брюшной полости и другие. [1,9]
Народные методы лечения асцита, возникшего на фоне онкологического заболевания, не имеют доказанной эффективности и безопасности, поэтому в «Евроонко» не применяются.
Если вы обратились в нашу клинику по поводу асцита на фоне рака, мы рекомендуем получить «второе мнение» касательно лечения основного заболевания у наших клинических онкологов и химиотерапевтов.
Клинический случай
В клинику «Евроонко» обратилась за помощью женщина Ш. 59 лет с диагнозом рак (аденокарцинома) яичников IV стадия, асцит, хронический болевой синдром 2 б по ШВО. Пациентка обратила внимание на увеличение живота в объеме до 120 см в окружности, затруднение дыхания, потерю веса. В специфическом лечении по месту жительства было отказано. Со слов пациентки её «отправили домой умирать». Читать далее…
В клинику «Евроонко» обратилась за помощью женщина Ш. 59 лет с диагнозом рак (аденокарцинома) яичников IV стадия, асцит, хронический болевой синдром 2 б по ШВО.
Пациентка обратила внимание на увеличение живота в объеме до 120 см в окружности, затруднение дыхания, потерю веса. В специфическом лечении по месту жительства было отказано. Со слов пациентки её «отправили домой умирать». Больная Ш. была экстренно госпитализирована в специализированное отделение «Евроонко», после проведения активной симптоматической терапии, направленной на нормализацию показателей крови и восстановление водно-электролитного баланса, был установлен перитонеальный порт. Под контролем уровня белка плазмы проведено разрешение асцита. Использование перитонеальных портов позволяет осуществить удаление асцитической жидкости дробно, дозированно, что в конечном итоге исключает возникновение серьезных осложнений в виде геморрагического синдрома, связанных с гемодилюцией и коагулопатией в результате массивного поступления асцитического содержимого в венозное русло.
После стабилизации общего состояния, на фоне нутритивной поддержки, противорвотной и антисекреторной терапии пациентка Ш. получила специфическое химиотерапевтическое лечение с хорошим эффектом. По факту разрешения асцита при наличии перитонеального порта стало возможным проведение внутрибрюшной химиотерапии.
Спустя шесть месяцев после описанной госпитализации пациентка вернулась к привычному для нее образу жизни, продолжает получать системное лечение в амбулаторном режиме под контролем команды специалистов «Евроонко». Ответ на лечение расценивается как положительный, при отсутствии асцита и суммарным уменьшением размеров очагов более чем на 70%. Комбинированное лечение в формате системной и локальной (внутрибрюшной) терапии с имплантацией порт-системы является оптимальным режимом ведения данной группы пациентов. В практике врачей «Евроонко» подобные случаи встречаются на регулярной основе. Скрыть
Из-за чего при раке развивается асцит?
Чаще всего к накоплению жидкости приводят следующие онкологические заболевания:
- рак яичников (у 25–30 процентов пациентов),
- рак молочной железы,
- рак матки,
- рак желудка,
- рак толстой кишки. [2]
Накопление жидкости в брюшной полости при раке происходит из-за того, что поражается брюшина (оболочка, выстилающая изнутри стенки брюшной полости и покрывающая расположенные в ней органы). На её париетальном и висцеральном листках поселяются опухолевые клетки, в результате чего происходит нарушение лимфатического дренажа. Это и вызывает ухудшение всасывания жидкости. Обычно причиной становятся опухоли желудочно-кишечного тракта и асцит при раке яичников.
Когда в печени образуется опухоль или метастазы, причина скопления жидкости в брюшной полости в другом: сжимается венозная система печени и нарушается естественный венозный отток от кишечника. Такое состояние развивается быстро, и обычно течёт дольше и тяжелее. 15 процентов случаев при онкологических заболеваниях приходится именно на эту его форму.
Лимфома брюшной полости вызывает асцит через закупорку и выпот (просачивание) лимфы из внутрибрюшных лимфатических протоков. [2,6]
Причины
Основой развития заболевания становится патология: при нормальном функционировании полости брюшины выделений значительного количества жидкой массы не происходит. Оно лишь незначительное, ровно только для того, чтобы избежать спаек от скольжения петель кишечника. Выделяемая для этого жидкость постоянно отходит обратно.
Когда же нарушается привычная работа данного механизма, дестабилизируется функция секреции жидкой массы, а также функция ее оттока. Последствие такой дестабилизации – скопление внутри живота избытка жидкой массы.
Особенности лечения асцита у онкобольных
В лечебных учреждениях, которые не специализируются на лечении онкологических заболеваний, подход к пациентам с асцитом может быть неэффективным из-за особенностей этого состояния. Например, основное лечение может заключаться в применении мочегонных препаратов, антагонистов альдостерона, изменении диеты для ограничения водной и солевой нагрузки. Эффективность этого подхода для уменьшения портальной гипертензии относительна, у онкобольных скопление жидкости в брюшной полости вызвано канцероматозом брюшины. Поэтому консервативная терапия не может быть основным методом лечения у таких пациентов.
Обычно жидкость удаляется из брюшной полости с помощью лапароцентеза (абдоминального парацентеза). Это хирургическая процедура, которая проводится хирургом и анестезиологом-реаниматологом. [3,10]
Асцит
shutterstock.com/Getty Images
Поделиться
Асцитом называют скопление в брюшной полости жидкости.
Причины возникновения асцита
Наиболее часто асцит возникает при болезнях почек, сердечной недостаточности, алиментарной дистрофии, циррозе печени, вследствие поражения лимфатического грудного протока, брюшины (туберкулезное, раковое обсеменение и так далее), в результате сдавления ствола воротной вены печени или тромбозе ее ветвей. У новорожденных асцит развивается при скрытых кровопотерях или при наличии у плода гемолитической болезни. У детей до трех лет асцит обычно связан с болезнями печени, но может быть и результатом экссудативной энтеропатии, хронических расстройств питания, а также проявлением нефротического синдрома. Возникновению асцита способствуют нарушения водно-солевого обмена.
Клинические признаки асцита
Скапливающаяся в брюшной полости в больших количествах жидкость (иногда более 20 литров) вызывает оттеснение в грудную полость диафрагмы и повышение внутрибрюшного давления. Результатом этого становится ограничение движения легких (вплоть до дыхательной недостаточности), нарушаются функции сердца, развивается белковая недостаточность. Определить асцит клинически можно только при наличии не менее одного литра жидкости в брюшной полости. При осмотре отмечают увеличение живота, его отвисание, выпячивание пупка. У больного, в лежачем положении выбухают боковые отделы живота, он распластан («лягушачий живот»). На коже живота хорошо заметна венозная сеть. Извитые, набухшие и расширенные вены концентрируются вокруг пупка и в виде лучей отходят от него, образуя так называемую «голову Медузы». При перкуссии брюшной полости над ее боковой или отлогой частью слышен тупой звук. Когда положение тела меняется, меняется и граница тупости. Ладонью, приложенной сбоку с одной стороны живота, можно почувствовать толчки, возникающие при постукивании пальцами другой руки по противоположной стороне (так называемый симптом флюктуации). Рентгенологическим исследованием и перкуссией определяют ограничение подвижности диафрагмы. У больных с асцитом, осложненным сердечной недостаточностью нередко наблюдают гидроторакс (жидкость в плевре).
Диагностика асцита
Главной диагностической задачей является установление основного заболевания, результатом которого стал асцит. При циррозе часто асцит сочетается с кровотечениями из вен пищевода и сопровождается развитием под кожей живота коллатералей. При сердечной недостаточности, осложненной асцитом, наблюдают отеки стоп и голеней, акроцианозы. При почечной недостаточности распространены отеки подкожной клетчатки и кожи.
Для диагностики большое значение имеет пункция брюшной полости с дальнейшим исследованием полученной жидкости. У пациентов с сердечной недостаточностью и циррозом печени жидкость прозрачная, содержит в основном клетки эндотелия, белковая концентрация не более 2,5%. При раке брюшины в жидкости обнаруживают раковые клетки. У детей до трех лет асцит необходимо дифференцировать от псевдоасцита, который можно наблюдать при муковисцидозе и глютеновой болезни.
Лечение асцита
Направлено на устранение основной болезни. Для снижения количества жидкости применяют антагонисты альдостерона, мочегонные средства, нормализуют водно-солевой обмен. Если медикаментозные методы неэффективны, показана пункция брюшной полости. К хирургическому лечению асцита прибегают для уменьшения портальной гипертензии и создания необходимых условий для всасывания жидкости близлежащими тканями. Прогноз основной болезни при осложнении асцитом ухудшается.
Консервативная терапия
Консервативная терапия применяется в лечении небольших асцитов и средней степени выраженности. Другими словами, если не возникают утомляющие и истощающие симптомы: боль, частое дыхание (тахипноэ) и др. До 65% пациентов имеют улучшение состояния при терапии мочегонными препаратами – так можно выводить до 1 литра жидкости в день. [5]
На поздних стадиях онкологического заболевания уменьшение потребления соли и воды может снизить качество жизни. Поэтому в «Евроонко» такая коррекция диеты назначается редко.
Запись на консультацию круглосуточно
+7+7+78
Образование
Излишнее скопление жидкой массы происходит не сразу, поэтому органы человека в ходе данного процесса приспосабливаются к изменению внутрибрюшинного давления.
Международная классификация выделяет три степени патологии:
- Степень первая характеризуется минимальным объемом жидкой массы, что обнаруживается при УЗИ полости брюшины;
- Степень вторая – скопления жидкой массы определяется литрами, живот увеличивается;
- Степень третья называется напряженным асцитом, состояние человека оценивается как тяжелое.
Как правило, напряженный асцит характеризуется скоплением в полости брюшины более 10 литров жидкости.
Хирургическое лечение
Асцит при онкологическом заболевании необходимо лечить хирургическим путём, когда это:
- Рефрактерный, то есть не поддающийся консервативному лечению.
- Большой, то есть если необходимо вывести до 6–10 л жидкости за один раз (эта тяжёлая процедура проводится по строгим медицинским показаниям).
- Гигантский. В этом случае нужна комбинированная операция, которая включает выведение большого объёма жидкости (до 5–7 л) в первые сутки и выведение остального объёма со скоростью не больше, чем 1 л в сутки в течение 7–10 дней.
В классическом варианте лапароцентез проводится на пустой мочевой пузырь, пациент садится, тяжелобольного человека укладывают на бок. [4]
Без соблюдения правил асептики и антисептики проводить лапароцентез опасно. Поэтому выпуск жидкости проводится только в специализированном лечебном учреждении с лицензией на выполнение хирургических вмешательств и имеющим стационар. Если пациент находится в тяжелом состоянии, ему сложно передвигаться, для него вызывают бригаду скорой медицинской помощи.
Сначала выполняется местная анестезия, затем под контролем ультразвука делается прокол троакаром (инструментом в виде тонкой трубки с острым концом) по средней линии живота или по линии, соединяющей пупок с гребнем подвздошной кости. Обычно за один раз выводится не более 5–6 л жидкости. Чтобы артериальное давление резко не упало и не случился коллапс сосудов, жидкость выпускается медленно.
В соответствии с классической методикой пациенту необходимо лежать в течение нескольких часов на свободном от пункции боку. Если в это время незначительное количество жидкости продолжает выделяться, то накладывают резервуар, который убирают через сутки или двое.
Если требуется удалить большое количество жидкости, то происходит потеря белка и солей, что становится причиной белковой недостаточности. Для предотвращения такого осложнения больному вводят альбумин. При повторной пункции может возникнуть ещё одно осложнение — сращение сальника (части брюшины) или кишки с передней стенкой живота. Из-за этого работа кишечника значительно ухудшается, а при последующих пункциях могут развиться тяжёлые осложнения. [4,6]
При современном подходе к проведению лапароцентеза отвод жидкости происходит преимущественно через постоянный перитонеальный катетер. Одновременно дефицит объёма циркулирующей крови замещается плазмаэкспандерами (от англ. plasma expander — увеличивающий объём плазмы). Обычно для этого используются 10–20-процентные растворы альбумина.В некоторых случаях вместо альбумина можно использовать аминостерил, полиглюкин, реополиглюкин (декстран-40), гемацелл и новые препараты на основе крахмала (рефортан, стабизол, ХАЕС-стерил). Такая альтернатива помогает лишь возместить дефицит жидкости в крови, но на дефицит белка эти препараты не влияют.
Некоторым больным с асцитом проводят оментогепатофренопексию. Это лапароскопическая операция, при которой сальник подшивается к участкам поверхности печени и диафрагмы. Благодаря тому, что между сальником и печенью возникает контакт, появляются условия для всасывания асцитической жидкости находящимися рядом тканями. Если у пациента есть канцероматоз брюшины, операция выполняется ограниченно. Обычно у таких больных оментогепатофренопексия становится частью паллиативного лечения. [6,7]
Методы диагностики
Если жидкости в животе скопилось более 500 мл, симптомы может выявить врач во время осмотра. Для подтверждения диагноза применяют УЗИ. Иногда асцит обнаруживают случайно во время ультразвукового исследования или компьютерной томографии живота, которые проводят по другому поводу.
В «Евроонко» действует комплексная скрининговая программа «ЖКТ», которая помогает оценить состояние органов пищеварительной системы. В неё, в частности, входит УЗИ брюшной полости с определением уровня свободной жидкости. Это помогает диагностировать асцит на ранней стадии.
Важно не только выявить жидкость в брюшной полости, но и разобраться в причинах её скопления — это помогает оценить прогноз и назначить эффективное лечение. В большинстве случаев обследование включает следующие лабораторные исследования:
- Биохимический анализ крови — полная биохимическая панель. Она помогает оценить состояние и функции печени, почек, уровни электролитов.
- Исследование свертываемости крови.
- Исследование асцитической жидкости, полученной во время лапароцентеза. Для анализа ее нужно немного — обычно 20 см³, меньше столовой ложки. В ней изучают уровень эритроцитов и лейкоцитов, общего белка, альбумина, амилазы, глюкозы, исследуют на патогенные микроорганизмы. Проводят цитологическое исследование, которое помогает выявить раковые клетки. [6]
Возможные осложнения
Если в брюшной полости скапливается много жидкости, то нарушается работа внутренних органов, возникают затруднения во время дыхания, так как ограничивается подвижность диафрагмы, образуется выпот в плевральной полости.
При повышенном давлении в воротной вене бактерии из кишечника могут самопроизвольно проникать в асцитическую жидкость и вызывать спонтанный бактериальный перитонит.
В редких случаях развивается очень тяжелое осложнение — гепаторенальный синдром. Под этим термином понимают нарушение функции почек при серьезном поражении печени, вплоть до тяжелой почечной недостаточности. Точный механизм развития этого состояния неизвестен, считается, что оно возникает из-за нарушения почечного кровотока, чрезмерного применения мочегонных средств и внутривенного введения контрастных препаратов. [4]
Стадии тяжести
Выделяют три стадии водянки брюшной полости в зависимости от количества скопившейся жидкости:
- Начальная стадия – в брюшной полости скапливается до полутора литров жидкости;
- Умеренный асцит – проявляется увеличением размеров живота, отёками нижних конечностей. Пациента беспокоит выраженная одышка, тяжесть в животе, изжога, запоры;
- Тяжёлая водянка – в брюшной полости скапливается от 5 до 20 литров жидкости. Кожа на животе натягивается, становится гладкой. У пациентов возникают перебои в работе сердца, развивается дыхательная недостаточность. При инфицировании жидкости развивается асцит-перитонит (воспаление листков брюшины).
Прогноз
Асцит при онкологических заболеваниях значительно ухудшает прогноз. С момента диагностики в течение 1–4 месяцев остается в живых только половина больных. Средняя продолжительность жизни составляет от 20 до 58 недель. Улучшить выживаемость помогает своевременное лечение в клинике, которая специализируется на работе с такими пациентами. Если скопление жидкости в брюшной полости вызвано циррозом печени, когда нет онкологического заболевания, прогноз лучше, а если хронической сердечной недостаточностью, при соответствующем лечении, может прожить еще годы. [6]
Симптомы
Основное проявление асцита – значительное увеличение размеров и патологическое вздутие живота. Признаки водянки брюшной полости могут нарастать стремительно или в течение нескольких месяцев. Асцит проявляется следующими клиническими симптомами:
- Чувством распирания в брюшной полости;
- Болевыми ощущениями в области живота и таза;
- Повышенным газообразованием (метеоризмом);
- Отрыжкой;
- Изжогой;
- Нарушением пищеварения.
Визуально у больного увеличивается живот, в горизонтальном положении он свисает и начинает «расплываться» по бокам. Пупок постепенно все более выпячивается, а на растянутых кожных покровах просматриваются кровеносные сосуды. По мере развития асцита пациенту становится тяжело наклоняться, появляется одышка.
Врачи клиники онкологии проводят оценку клинических проявлений заболевания и проводят дифференциальную диагностику рака с другими болезнями, проявлением которых является асцит.
Цены
В «Евроонко» действует специальное предложение на дренирование асцита в условиях дневного стационара – 63300 руб.
Программа включает:
- Осмотр и консультацию хирурга-онколога.
- Общий анализ крови, биохимический анализ крови, ЭКГ.
- УЗИ органов брюшной полости с определением уровня свободной жидкости
- Проведение лапароцентеза с УЗИ навигацией.
- Комплексную медикаментозную терапию, направленную на восстановление водно-электролитного баланса.
Запись на консультацию круглосуточно
+7+7+78
Список литературы:
- Фармакотерапия опухолей. Посвящается памяти Михаила Лазаревича Гершановича // А.Н. Стуков и коллектив авторов / Под р ед. А.Н. Стукова, М.А. Бланка, Т.Ю. Семиглазовой, А.М. Беляева. СПб: Издательство АНО «Вопросы онкологии», 2021, 512 с.
- Виллерт А.Б., Коломиец Л.А., Юнусова Н.В., Иванова А.А. Асцит как предмет исследований при раке яичников. Сибирский онкологический журнал. 2019; 18 (1): 116–123. – doi: 10.21294/1814-4861-2019-18-1-116-123.
- Виллерт А. Б., Коломиец Л. А., Юнусова Н. В. Асцит как микроокружение опухоли при раке яичников: взаимосвязь прогноза и химиорезистентности. Успехи молекулярной онкологии 2019;6(2):8–20.
- Ю.М. Степанов, И.Н. Кононов, Т.А. Скороход, Асцит, ассоциированный с внутрибрюшинным разрывом мочевого пузыря и мочевым перитонитом. Клінічний випадок сучасна гастроентерологія, 4 (66) • 2012.
- Т.А.Баева, Д.Н.Андреев, Е.М.Миронова, Д.Т.Дичева — Асцит: дифференциальная диагностика и лечение. — Справочник поликлинического врача. No2, 2021.
- Алексейчик, С. Е. Асцит. Дифференциальная диагностика: метод. рекомендации / С. Е. Алексейчик. – Мн.: БГМУ, 2005. – 28 с.
- В.Т. Ивашкин, М.В. Маевская, Ч.С. Павлов, Е.А. Федосьина. Клинические рекомендации Российского общества по изучению печени и Российской гастроэнтерологической ассоциации по лечению осложнений цирроза печени. Рос журн гастроэнтерол гепатол колопроктол 2016; 26(4).
- J.T.Tamsma, H.J. Keizer, A. E. Meinders. Pathogenesis of malignant ascites: Starling’s law of capillary hemodynamics revisited. — Annals of Oncology 12: 1353-1357. 2001.
- Rony A Adam, Yehuda G Adam. — Malignant ascites: past, present, and future. — VOLUME 198, ISSUE 6, P999-1011, JUNE 01, 2004. DOI:https://doi.org/10.1016/j.jamcollsurg.2004.01.035
- Michelle Meier, Frank V. Mortensen, Hans Henrik Torp Madsen. — Malignant ascites in patients with terminal cancer is effectively treated with permanent peritoneal catheter. — Acta Radiologica Open 4(7) 1–7. DOI: 10.1177/2058460115579934.
- R.C. Oey, H.R. van Buuren, R.A. de Man. — The diagnostic work-up in patients with ascites: current guidelines and future prospects. OCTOBER 2021, VOL. 74, NO. 8