Тромбоцитопения
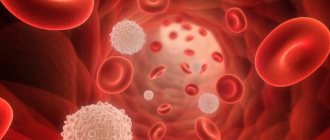
– патологическое состояние, для которого характерны снижение количества тромбоцитов в единице объема крови и вызванная этим повышенная кровоточивость. Тромбоциты играют важную роль в остановке кровотечений. Молекулы наружной мембраны этого плоского форменного элемента крови способны распознавать повреждённые участки сосудов и встраиваться в структуру капилляров, превращаясь в своеобразную «заплатку». Уменьшение концентрации тромбоцитов в кровяном русле приводит к возникновению большого количества точечных кровоизлияний.
Классификация заболевания
Тромбоцитопения имеет свою классификацию, сформированную на основе ряда факторов, симптомов и проявлений. Механизм зарождения и развития тромбоцитопении может быть связан с особенностями жизненного цикла кровяных пластинок:
- пониженное образование тромбоцитов в красном костном мозге.
- повышенное разрушение тромбоцитов.
- перераспределение тромбоцитов в системе кроветворения в связи с воспалительными процессами в организме человека.
Согласно этиологии выделяют первичную и вторичную тромбоцитопению. Первый тип
проявляется как самостоятельный недуг.
Второй тип
– как последствие патологических отклонений. Тромбоцитопения может иметь острое и хроническое течение. Острое состояние длится непродолжительное время (до 6 месяцев) и характеризуется яркой клинической картиной. Хроническое состояние может протекать с постепенным нарастанием симптомов. Тяжесть заболевания зависит от количества тромбоцитов в крови и условно делится на три степени – лёгкую, среднюю и тяжёлую. Каждая из них имеет свои проявления – от частых носовых кровотечений до геморрагической сыпи (пурпуры) и обширных кровотечений во внутренние органы.
Тромбоцитопения при беременности
Тромбоцитопения, или сниженное количество тромбоцитов в крови, встречается в 7-12% случаев беременности. Среднее количество тромбоцитов во время беременности снижается (213 000 / мкл против 250 000 / мкл) и уменьшается по мере прогрессирования беременности. Изменение количества тромбоцитов связано с гемодилюцией, повышенным потреблением тромбоцитов и повышенной агрегацией тромбоцитов, вызванной повышенным уровнем тромбоксана А2. Тромбоцитопению можно определить как количество тромбоцитов менее 150000 / мкл или количество тромбоцитов ниже 2,5-го процентиля для беременных (116 000 / мкл).
Легкая тромбоцитопения составляет 100 000-150 000 / мкл. Умеренная тромбоцитопения составляет 50000-100000 / мкл. Тяжелая тромбоцитопения составляет <50000 / мкл. При нормальной беременности 7,6% женщин имеют легкую тромбоцитопению во время беременности, и 65% из них не будут связаны с какой-либо патологией.
Ретроспективное исследование, проведенное Shin et al., показало, что у беременных с апластической анемией акушерские осложнения чаще встречаются у пациентов с тяжелой тромбоцитопенией, чем у пациентов с легкой тромбоцитопенией. Повышенное разрушение тромбоцитов включает гестационную тромбоцитопению и иммунологическую тромбоцитопению.
Неиммунологически связанная тромбоцитопения может включать следующее: преэклампсия / эклампсия, синдром HELLP, тромботическая тромбоцитопеническая пурпура, гемолитический уремический синдром, острый гепатоз беремнности, гепарин — индуцированная тромбоцитопения, сосудистые мальформации, гиперспленический синдром.
Также можно отметить снижение выработки тромбоцитов и при других патологических состояниях , включая витамин B-12 и дефицит фолата, а также подавление костного мозга, которое может быть вызвано следующими причинами: действием лекарственного средства, апластической анемией, пароксизмальной ночной гемоглобинурией, инфекционным заболванием, инфильтрацией костного мозга (гематологическая злокачественность, негематологическая злокачественность).
Секвестрация селезенки может быть вызвана следующими причинами: портальная гипертензия, заболевание печени, тромбоз воротной или печеночной вены, миелопролиферативные расстройства, лимфопролиферативные заболевания , болезни накопления ( болезнь Гоше ), инфекция ( малярия)
Иммунологическая тромбоцитопения, включает в себя: иммунную тромбоцитопеническую пурпуру , системную красную волчанку, антифосфолипидный синдром, коллагенозы, медикаментозную тромбоцитопению, вирусные инфекции ( ВИЧ, вирсус Эпштейн — Барр ) , лимфому.
Наиболее распространенные причины тромбоцитопении у беременных: гестационная тромбоцитопения (70%), преэклампсия (21%), иммунная тромбоцитопеническая пурпура (3%), другое (6%). Патогенез гестационной тромбоцитопении неизвестен, но выделяется два основных фактора : ускоренная активация тромбоцитов происходит при плацентарной циркуляции, ускоренное потребление тромбоцитов связано с уменьшением продолжительности жизни тромбоцитов во время беременности. Никакого патологического значения для матери или плода не отмечено. Никакого риска кровотечения или осложнений кровотечения у плода не наблюдается. Количество тромбоцитов нормализуется в течение 1-2 месяцев после родов.
Причины возникновения тромбоцитопении
Среди разных причин, вызывающих это серьёзное заболевание, основными считаются:
Симптомы тромбоцитопении
Клиническая картина тромбоцитопении зависит от причины, вызвавшей данную патологию, а также степени тяжести недуга. Основными признаками являются множественные кровоизлияния на кожных покровах, а также спонтанные кровотечения – носовые, лёгочные, маточные. Другие проявления болезни:
Тромбоцитопеническая пурпура и беременность
Автор: Бузян Лидия Олеговна, врач терапевт-гемостазиолог сети центров репродукции и генетики «Нова Клиник».
Чуть менее ста лет назад Мошковиц впервые описал у шестнадцатилетней девушки необычное заболевание с анемией, мелкими кровоизлияниями на коже, закончившееся в итоге развитием паралича и комы. Его именем и названа эта болезнь – тромботическая тромбоцитопеническая пурпура (болезнь Мошковица).
В последние десятилетия, благодаря активному изучению и поиску эффективных методов лечения, это довольно редкое (в США 3,7 случаев на 1 миллион человек) заболевание значительно реже приводит к смерти пациентов. После того, как в лечении стали применять терапию плазмой, смертность пациентов снизилась с 80% до 10%. Однако исход напрямую зависит от того, как быстро поставлен правильный диагноз и начато специфическое лечение. К сожалению, в связи с низкой специфичностью симптомов и редкими случаями заболевания в практике большинства рядовых врачей быстро разобраться в ситуации получается не всегда.
При болезни Мошковица поражаются жизненно важные органы – мозг и почки. Поражение происходит вследствие тромбирования микрососудов, питающих эти органы. А массивное тромбообразование, как следствие, ведет к тому, что запас тромбоцитов и эритроцитов в крови истощается – они задерживаются и накапливаются в тромботических массах; поэтому в общем анализе крови будет наблюдаться снижение тромбоцитов и гемоглобина (анемия и тромбоцитопения).
Причины развития заболевания складываются из сочетания наследственной предрасположенности и пускового провоцирующего фактора. Врожденные генетические дефекты приводят к снижению активности специфического фермента – ADAMTS-13, вследствие чего при воздействии некого пускового механизма (триггера) тромбообразование у таких людей активируется в значительно большей степени, чем у других, закупориваются мелкие сосуды и появляются симптомы поражения почек или головного мозга.
Провоцировать развитие тромботической пурпуры могут следующие факторы:
- беременность (по разным данным, от 12% до 30% всех случаев заболевания приходятся на период беременности);
- инфекционные заболевания (активацию тромбообразования могут вызывать вирусы, бактериальные токсины – в частности, токсин стрептококка при пневмонии, токсин шигеллы при кишечных инфекциях у детей);
- вакцинация;
- прием некоторых лекарственных препаратов (оральные контрацептивы, противоопухолевые препараты, иммуносупрессоры после пересадки органов и тканей, разжижающий препарат клопидогрел);
- хирургические вмешательства;
- наличие аутоиммунных заболеваний (в частности, системной красной волчанки, антифосфолипидного синдрома).
Во время беременности проявления болезни Мошковица нетрудно спутать с преэклампсией или эклампсией. Может повышаться артериальное давление, появляется белок в моче, могут быть головные боли, судороги, вплоть до развития комы (при тяжелом течении и отсутствии лечения). Поражение мозга также может проявляться инсультами или ишемическими атаками. Примерно три четверти случаев заболевания приходятся на третий триместр. Значительное снижение тромбоцитов в анализе крови (обычно менее 100 и даже менее 60) в сочетании с анемией (гемоглобин ниже 100 г/л, а у 40% пациенток ниже 65 г/л) – повод заподозрить наличие болезни Мошковица и, при наличии соответствующих клинических симптомов, незамедлительно провести дополнительную диагностику. Поскольку анемия при тромбоцитопенической пурпуре является следствием разрушения эритроцитов, то в крови может быть повышена концентрация непрямого билирубина и фермента ЛДГ. Помогает в диагностике проба Кумбса, результат которой подтверждает или исключает наличие гемолиза (разрушения эритроцитов).
Специфическим и подтверждающим методом диагностики является определение активности фермента ADAMTS-13 в крови, однако этот метод доступен весьма ограничено, как и генетическое определение мутаций в гене ADAMTS-13.
Если диагноз подтвержден или максимально вероятен, немедленно начинается лечение. При тромботической пурпуре это, в первую очередь, плазмаферез, а при невозможности его проведения – переливание свежезамороженной плазмы. Обычно требуется несколько процедур, так как после завершения лечения патологический процесс вскоре активируется снова. У 30-60% пациентов наблюдаются рецидивы заболевания, тогда для их профилактики переливание плазмы повторяется каждые 2-3 недели.
Течение беременности и возможность ее сохранения зависят от тяжести заболевания. Разумеется, при жизнеугрожающих состояниях требуется в первую очередь спасти жизнь женщине, родоразрешение в этом случае практически неизбежно. Ребенок при этом может быть рожден вполне жизнеспособным. В то же время даже появление симптомов заболевания на малом сроке беременности, при условии хорошего ответа на терапию, не является абсолютным показанием для ее прерывания.
При легкой форме заболевания бывает достаточно переливания свежезамороженной плазмы, при среднетяжелой и тяжелой обязательно требуется плазмаферез. Если пораженные почки не справляются с фильтрацией мочи, добавляется гемодиализ. При повышении артериального давления применяются антигипертензивные препараты, а при тяжелой анемии – переливание эритроцитарной массы. Необходимо также следить за состоянием свертывающей системы крови, при необходимости могут быть назначены разжижающие препараты. Только при отсутствии эффекта от всех возможных лечебных мероприятий выполняется родоразрешение. Также после родов может потребоваться удаление селезенки для профилактики рецидивов.
Стоимость консультации при тромбоцитопении?
| Наименование услуги | Цена (руб.) |
| Прием врача-кардиолога первичный | 2000 руб. |
| Приём врача кардиолога повторный | 1500 руб. |
| Прием врача-терапевта первичный | 2000 руб. |
| Прием врача-терапевта повторный | 1500 руб. |
| Назначение лечения (составление индивидуальной схемы лечения) | 1500 — 3000 руб. |
Все наши услуги и цены
Диагностика и лечение
Повышенная кровоточивость
– повод немедленно обратиться за консультацией к специалисту (гематологу), который составит подробный анамнез и назначит необходимые обследования. Основным способом диагностики является клинический анализ крови, определяющий количественный состав тромбоцитов. Пациенту может быть также рекомендованы пункция костного мозга для оценки качества данного вида кроветворения, УЗИ селезёнки, рентген грудной клетки, тесты на наличие антител. При беременности тромбоцитопения диагностируется при помощи коагулограммы (исследования на свёртываемость крови), позволяющей установить количественный состав тромбоцитов в крови женщины.
Лечить такое серьёзное заболевание, как тромбоцитопения, следует только под контролем врача. После получения результатов всех обследований специалист подбирает каждому пациенту индивидуальные терапевтические мероприятия. При выраженном геморрагическом синдроме требуется срочная госпитализация и оказание неотложной помощи. При сильных кровотечениях показаны трансфузии тромбоцитов, а также назначаются ангиопротекторы и ингибиторы фибринолиза. Исключается приём ацетилсалициловой кислоты и антикоагулянтов. При дефиците витамина В12 или фолиевой кислоты назначаются медикаменты с высоким содержанием данных элементов. Это значительно улучшает общее состояние больного и результаты его анализов. Если диагностирована иммунная тромбоцитопения, потребуется курсовой приём преднизолона. Дозировка определяется индивидуальными особенностями пациента и его организма. При неэффективности лекарственной терапии и возникающих повторных кровотечениях показана спленэктомия (удаление селезёнки). При тромбоцитопениях неиммунного характера рекомендуется проводить симптоматическую гемостатическую терапию.
Специальной диеты при тромбоцитопениях нет, однако стоит придерживаться принципов рационального, сбалансированного питания. Следует ввести в рацион больше овощей, фруктов, зелени, обезжиренных молочных продуктов, растительных масел, бобовых, морепродуктов. Употребление алкоголя строго запрещено. Нежелательные продукты: белый рис, сахар, сдобная выпечка, маринады и соления.
После консультации с лечащим врачом можно воспользоваться средствами народной медицины – настоями и отварами из лечебных трав, кунжутным маслом.
При тяжелом течении COVID-19 у беременных количество тромбоэмболических осложнений возрастает в разы. Это обусловлено, с одной стороны, физиологическими изменениями в системе гемостаза в сторону гиперкоагуляции — постепенное, по мере увеличения сроков беременности, увеличение плазменного уровня фибриногена, факторов VII, фон Виллибранда, VIII, концентрации D-димеров; антитромбин III незначительно снижается, фибринолитическая активность снижается.
С другой стороны, инфицирование SARS-CoV-2 также вызывает ряд патофизиологических реакций, значительно влияющих на систему гемостаза. Тромбообразование у пациентов с COVID-19 запускается в основном по внешнему пути активации процесса свертывания крови (через соединение тканевого фактора с фактором VII).
Ольга Светлицкая, доцент кафедры анестезиологии и реаниматологии БелМАПО, кандидат мед. наук.Повреждение альвеолярно-капиллярного барьера
Вирус SARS-CoV-2 проникает в легочную ткань благодаря соединению с рецептором АСЕ2, который экспрессируется в большом количестве на поверхности пневмоцитов 2-го типа и эндотелиоцитов, выстилающих капиллярное русло.
С момента проникновения вируса и начала репликации клетка перестает выполнять свойственные ей функции, начинает продуцировать белки, свойственные вирусу, с формированием новых вирионов, после чего разрушается. На это реагируют альвеолярные макрофаги и циркулирующие в капиллярном русле легочной ткани моноциты. Они начинают вырабатывать в большом количестве интерлейкины ИЛ-1, ИЛ-6 и другие провоспалительные цитокины.
Чем больше происходит размножение вирионов, тем больше разрушается пневмоцитов 2-го типа и эндотелиоцитов и тем серьезнее нарушения альвеолярно-капиллярного барьера, что клинически проявляется снижением сатурации. Нарастание выработки макрофагами и моноцитами провоспалительных цитокинов существенно влияет на активацию системы гемостаза.
Вырабатываемые интерлейкины, в частности ИЛ-1 и ИЛ-6, увеличивают синтез тканевого фактора на поверхности эндотелиоцитов, которые еще не повреждены SARS-CoV-2. Кроме того, ИЛ-6 блокирует синтез ингибитора пути тканевого фактора. Накопление тканевого фактора глобально активирует процесс свертывания крови по всему сосудистому руслу.
Начинается массивная агрегация тромбоцитов в просвете легочных капилляров и формирование сгустков. Чем у́же просвет сосуда, тем меньше вероятность образования в нем полноценных тромбов, чаще в них наблюдаются тромбоцитарные сладжи. ФНО-а (фактор некроза опухоли альфа) блокирует фибринолиз.
Таким образом, при COVID-19 точно так же, как и при септических состояниях, параллельно происходят два серьезных патофизиологических процесса в системе гемостаза: глобальная активация тромбообразования на фоне угнетения фибринолиза.
Сложности антикоагулянтной терапии при COVID-19
Все пациенты, в т. ч. беременные женщины, должны получать профилактические и лечебные дозы НМГ, рассчитанные на фактическую массу тела.
Подбор дозы гепарина недопустимо проводить на глазок, потому что это может привести к осложнениям. Всех пациентов с COVID-10 при госпитализации необходимо взвешивать на уровне приемного отделения и четко указывать массу тела и рост в истории болезни.
Что делать, если нет возможности определить уровень D-димеров?
Во-первых, надо помнить, что исследование уровня D-димеров, широко практикуемое среди общей популяции пациентов с COVID-19, у беременных имеет невысокую клиническую значимость, поскольку разброс показателей уровня D-димеров при нормально протекающей беременности значительный и до сих пор не удалось установить достоверные референсные значения D-димеров при беременности. Поэтому оценку уровня D-димеров нужно обязательно проводить в динамике, обращая внимание не только на абсолютный уровень, но и на ежесуточный прирост.
В ситуациях, когда по каким-либо причинам нет возможности срочно определить уровень D-димеров, следует оценить уровень ЛДГ (лактатдегидрогеназы). Повышение ЛДГ в динамике, особенно >1 000 Ед/л, у пациента с COVID-19 может выступать косвенным лабораторным признаком ТЭЛА и/или инфаркта легких. Данный тест является высокочувствительным, но неспецифичным, однако поскольку при COVID-19 зоной поражения прежде всего являются легкие, мы можем предположить, что катастрофа происходит именно там.
Косвенно подтверждают наличие ТЭЛА: ЭКГ (признаки перегрузки правых отделов сердца), УЗИ сердца (расширение правых отделов, увеличение среднего значения ДЛА) и вен нижних конечностей (наличие тромбов).
Перечисленные косвенные признаки позволяют заподозрить ТЭЛА или высокий риск ТЭЛА и своевременно назначить адекватные дозы гепаринов.
Что делать, если не получается достичь целевого уровня RАЧТВ?
В первую очередь следует проверить правильность выполнения номограммы (расчет и коррекция болюса и вводимой дозы нефракционированного гепарина на фактическую массу тела). Если вы уверены, что выполнили все правильно, а RАЧТВ все равно не достигло целевых значений — определить уровни антитромбина III и/или анти-Ха активности.
Антитромбин III (AT III) и что делать при его снижении
Гепарин является кофактором AT III, он трансформирует AT III в антикоагулянт немедленного действия, усиливая его эффекты в 1 000 и более раз в зависимости от того, в какой дозе и с какой скоростью он вводится. Дефицит AT III уменьшает способность гепарина ингибировать факторы свертывания крови IIа и Ха.
Средний нормальный уровень AT III — 80–120 %. У беременных он естественным образом постепенно снижается и к концу 3-го триместра в норме не должен снизиться менее чем до 65 %. Практика показывает, что 60–65 % являются вполне управляемой ситуацией. Более низкие показатели (55–50 % и ниже) должны насторожить специалиста.
При остром воспалении уровень AT III всегда повышается, а вот при развитии тромбоза, сепсиса, ДВС-синдрома, введении гепаринов — снижается. Поэтому снижение уровня AT III у пациента с COVID-19 — это плохой прогностический признак, который говорит о развитии серьезных осложнений и требует принятия мер.
При дефиците AT III решение принимается индивидуально.
Для коагуляционной коррекции уровня AT III существует три подхода:
1.Перевод пациента на лечебные дозы НМГ. В условиях дефицита AT III мы концентрируемся на связывании фактора Ха, учитывая тот факт, что связывание 1 единицы Ха предотвращает образование 50 единиц IIа (тромбина).
2. Восполнение AT III с помощью свежезамороженной плазмы (СЗП) или концентрата AT III. Оба варианта не рекомендуются при COVID-19. Переливание СЗП на фоне ОРДС увеличивает риск еще большего повреждения легких за счет возможного развития синдрома TRALI (острое повреждение легочной паренхимы в ответ на трансфузию крови и ее компонентов). Введение концентрата АТ III (в случаях, если его уровень не снижался менее 65 %) может привести к повышенной кровоточивости, что нежелательно при ведении беременных женщин в критическом состоянии.
3. Перевод пациентов на прямые ингибиторы тромбина (независимых от АТ III) — прямой ингибитор фактора IIа (дабигатран) или прямой ингибитор фактора Ха (ривароксабан). Этот метод применяется в общей группе пациентов и не применяется у беременных.
Определение Анти-Ха активности (МЕ/мл)
В настоящее время возможность определения анти-Ха активности появилась во многих стационарах, и важно уметь правильно интерпретировать результаты (рекомендуемые уровни см. в табл. 1).
Забор крови на это исследование осуществляется через 3–4 часа после подкожного введения НМГ. Лучше всего делать это через 4 часа, поскольку именно на этом временном интервале отмечается максимальный уровень концентрации введенного НМГ в плазме крови (анти-Ха активность).
Таблица 1. Классические рекомендуемые уровни анти-Ха активностиС учетом того, что при госпитализации пациентов с ковидными пневмониями в основном выставляется высокий риск ТЭЛА, следует поддерживать уровень анти-Ха активности в пределах 0,5–1,0 МЕ/мл.
Принцип коррекции доз НМГ по анти-Ха активности приведен в табл. 2.
Таблица 2. Коррекция дозы НМГ для терапевтической концентрации 0,5–1,0 МЕ/мл
Что делать, если уровень D-димеров не снижается?
Один из самых часто задаваемых вопросов: все делаем правильно, но уровень D-димеров как был, так и остается высоким. В такую ловушку попадают стационары, в которых лаборатории выдают по D-димерам ответ «больше какого-либо значения», например «>5 000 нг/мл».
В таком случае нужно связаться с лабораторией и, если есть возможность, уточнить фактический уровень D-димеров на момент поступления пациента в реанимацию. Вполне возможно, он был 7 000, 10 000 или даже 20 000 нг/мл и на фоне лечения медленно снижается.
Также для верной оценки ситуации следует выполнить: контроль уровня АТ III и/или анти-Ха активности; УЗИ сердца с подсчетом среднего ДЛА; УЗИ вен нижних конечностей (ищем тромбы).
На фоне титрования НФГ тромбы постепенно разрыхляются и распадаются, поддерживая повышенный уровень D-димеров. Поэтому если у беременной женщины выявлен тромбоз вен нижних конечностей, необходимо периодически повторять УЗИ и проверять длину тромба. Если она уменьшается, значит, все хорошо.
Не нужно забывать, что иногда источником повышенного уровня D-димеров может быть гематома, которая медленно уходит, иногда на протяжении нескольких недель.
Что делать, если уровень D-димеров снова стал расти?
В ситуации резкого прироста необходимо провести диагностические мероприятия:
- контроль тромбообразования: УЗИ сосудов нижних конечностей, УЗИ сердца (расширение правых полостей сердца + среднее значение ДЛА);
- контроль выраженности воспалительного синдрома (наиболее доступный способ — определение С-реактивного белка (СРБ)).
Повышение уровня СРБ в динамике свидетельствует об острой фазе воспаления. Под действием ИЛ-1, ИЛ-6 и ФНО-а синтез СРБ увеличивается через 6 часов, достигает максимальной концентрации через 24–48 часов.
Если на фоне лечения происходит резкий подъем уровня D-димеров, параллельно начинает повышаться уровень СРБ, коррелируя с ростом уровня ЛДГ, это указывает на факт катастрофы в легочных сосудах.
Как понять, есть ли ТЭЛА, в условиях отсутствия КТ-ангиографии?
Повышенный уровень D-димеров сам по себе в данной ситуации не подтверждает ТЭЛА, но важна динамика этого показателя. Следует оценить клинические признаки ТЭЛА, в частности перфузионную дыхательную недостаточность (снижение периферической сатурации <� 90 %, компенсаторное тахипноэ, тахикардия, гипотензия и др.).
Применить доступные на данном уровне оказания медицинской помощи методы инструментальных исследований: выполнить ЭКГ (перегрузка правых отделов сердца), УЗИ сердца (дилатация правых отделов), измерить среднее значение ДЛА (при ТЭЛА оно может достигать 35–60 и более мм рт. ст.), УЗИ вен нижних конечностей (ищем тромбы).
Что делать, если пациент «закровил» или появилась гематома, а D-димеры повышены?
При активной кровоточивости нужно остановить введение НФГ и восстановить нормокоагуляцию. При необходимости восполнить дефицит факторов свертывания крови путем переливания одногруппной свежезамороженной плазмы или концентрата факторов протромбинового комплекса.
Дальнейший возврат к гепаринам возможен только при достижении нормокоагуляции в скрининговой коагулограмме и отсутствии признаков активного кровотечения.
Дозировка НМГ определяется индивидуально с учетом причины кровоточивости (диффузная кровоточивость, послеоперационное кровотечение и др.), уровня тромбоцитов, динамики и причины повышения уровняD-димеров.
Ознакомиться с материалом «COVID-19: особенности течения и лечения у беременных» можно пройдя по ссылке здесь.