Гиперхромная анемия
– группа заболеваний крови с цветовым показателем выше 1,15, характеризующихся нарушением функции кроветворения.
Гиперхромная макроцитарная анемия включает в себя следующие заболевания:
— В12-дефицитная анемия;
— Фолиеводефицитная анемия;
— Миелопластический синдром.
- Симптомы фолиеводефицитной анемии
- Симптомы миелодиспластического синдрома
Макроцитарная анемия
Анемия – патологический синдром, характеризующийся снижением уровня гемоглобина в крови, вызывающий нарушение функции кроветворной системы и транспорта кислорода, развитие гипоксии.
Для макроцитарной анемии характерно аномальное увеличение эритроцитов (макроцитоз) до объема ≥ 100 фл/кл (фемтолитров на клетку) при норме 80–100 фл. Из-за увеличения эритроцитов в размерах снижается их концентрация в крови, что приводит к уменьшению содержания гемоглобина. В результате, кровь недополучает нужное количество кислорода.
Степень насыщения эритроцитов гемоглобином определяют по цветовому показателю кровяных телец. В норме он составляет 0,86–1,1. По отклонениям от коэффициента патологию делят на 2 вида:
- Макроцитарная гипохромная анемия – цветовой показатель ниже 0,86. Подразделяется на талассемию и железодефицитную анемию.
- Гиперхромная макроцитарная анемия – цветовой показатель более 1,1. Подразделяется на миелодиспластический синдром, фолиеводефицитную и витамин B12-дефицитную анемии.
Также выделяют нормохромную анемию, при которой ЦП в пределах нормы, но в организме есть другие патологические процессы, например, кровотечение, болезнь костного мозга, внекостномозговая опухоль и др. В эту категорию входят постгеморрагические и гемолитические анемии.
Роль цветового показателя ЦП
Если возникает бледность, или гипохромия эритроцитов, то они становятся весьма бледными, а величина светлой окраски в центре эритроцитов, и ширина этой зоны значительно увеличена. Количественно определить степень гипохромии эритроцитов помогает цветовой показатель, или мера насыщенности красных кровяных телец гемоглобином.
В том случае, если цветовой показатель крови меньше, чем 0,8, то можно ставить с уверенностью этот морфологический диагноз. В том случае, если:
- кровь «здорова», и не содержит гипохромных эритроцитов, то значение цветового показателя будет выше 0,85 и ниже 1,05. Это приемлемое содержание гемоглобина, которое способно производить нормальный газообмен;
- цветовой показатель меньше 0,8, и эритроцитов содержится нормальное количество — это значит, что в каждом из них или почти во всех их гемоглобина меньше, чем нужно и есть наличие гипохромии;
- Иногда возникает и противоположная картина — гиперхромия, когда цветовой показатель выше, чем 1,1.
Когда цветовой показатель очень высок и превышает норму, составляя 1,4 и больше, то можно говорить о дефиците цианокобаламина (витамина B12). Такая гиперхромная анемия является показателем витаминной недостаточности, и называется пернициозной.
Причины макроцитарной анемии
Обычно заболевание развивается вследствие дефицита витамина B12 (цианкобаламина) или B9 (фолиевой кислоты).
Недостаток этих соединений часто возникает при несбалансированном питании. К фактору риска относится вегетарианство, поскольку цианкобаламин содержится преимущественно в продуктах животного происхождения.
У некоторых людей витамины поступают в организм, но не усваиваются. Возможные причины такой патологии:
- аутоиммунные нарушения;
- воспалительные болезни тонкого и толстого кишечника;
- кишечная мальабсорбция;
- злокачественные образования;
- чрезмерное употребление алкоголя;
- наркомания.
Острая и хроническая макроцитарная анемия возможна на фоне следующих заболеваний:
- гипотиреоз;
- нарушения обмена веществ;
- болезни печени (например, цирроз) и селезенки;
- лейкоз;
- редкие метаболические нарушения;
- приобретенная сидеробластная анемия.
К группе риска относятся люди с наследственной предрасположенностью, алкоголизмом, курящие, беременные женщины и пациенты, принимающие лекарственные препараты, нарушающие синтез ДНК (противоопухолевые средства и иммуносупрессанты).
По причине происхождения макроцитоз условно делят на две большие группы:
- Мегалобластный – возникает при витаминной недостаточности.
- Немегалобластный – развивается на фоне разных заболеваний и клинических состояний, которые не до конца изучены. Обычно это нарушения, связанные с увеличением площади мембраны эритроцитов, что свойственно хроническим патологиям печени и селезенки.
Механизмы повреждения кроветворения
Витамин В12 и фолаты (соли фолиевой кислоты) выполняют важную функцию в синтезе ДНК клеток: они являются незаменимыми ферментами, без которых биохимический процесс останавливается. Накопить достаточное количество в печени невозможно. Организм нуждается в постоянном пополнении необходимых компонентов.
Патология развивается постепенно, когда все запасы исчерпаны. В процессе кроветворения нарушается деление клеток эритробластов. Они превращаются в мегалобласты. Подобный вид эритроцитарного ростка был у человека в состоянии эмбриона.
Симптомы
На начальной стадии болезни какие-либо симптомы отсутствуют. Они развиваются постепенно, по мере снижения в крови нормальных эритроцитов. Независимо от формы основные проявления патологии одинаковые:
- общая слабость;
- быстрая утомляемость;
- частые головные боли;
- головокружение;
- нарушения сна;
- шум в ушах;
- мелькание «мушек» перед глазами;
- учащенное сердцебиение;
- одышка, особенно при физической нагрузке;
- ухудшение аппетита;
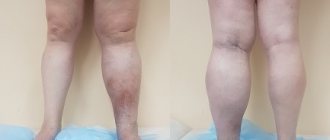
- бледность кожных покровов;
- снижение концентрации внимания;
- депрессия;
- обмороки.
При дефиците B12 нередко наблюдаются такие нарушения: снижение памяти, покалывание или онемение рук, мышечная слабость, неустойчивость походки, парестезии, трудности при ходьбе.
При мегалобластной анемии возможно появление глоссита, расстройство желудка, развитие анорексии.
В12-дефицитная анемия пожилых, или «у стариков всегда мерзнут ноги»
Анемия, обусловленная недостатком витамина В12 известна медицине давно, и раньше считалась неизлечимой, приводя к гибели больного несколько месяцев. Сегодня проблему составляет не лечение, а выявление патологии у пожилых, для которых она характерна. Ведь для этой категории пациентов большинство симптомов В12-дефицитной анемии – «обычное следствие старости», а значит и поводом для обследования не является.
У пожилых в 10 раз чаще
В12-дефицитная анемия в молодом возрасте – явление достаточно редкое, обусловленное в основном полным отказом от «животных» продуктов или нарушением всасывания витамина В12 и встречающееся примерно у 0,1% населения.
У пожилых распространенность этой патологии в 10-20 раз больше, и составляет уже 1-2% в возрасте до 75 лет, и около 4% — среди представителей старшей группы.
При этом этот В-12 обусловленная анемия – заболевание довольно многофакторное, а среди основных причин ее развития:
- недостаток внутреннего фактора Касла (вырабатываемого желудком и необходимого для усвоения В12 из пищи),
- дефицит В12 в питании
- выраженный дисбактериоз кишечника или гельминтозы.
Недостаточность внутреннего фактора Касла
Эта патология не зря занимает первое место среди причин В12-дефицитной анемии пожилых, ведь всасывание В12 в кишечнике возможно только в комплексе с «желудочным» фактором.
Иными словами, усвоение витамина В12 сильно нарушается при атрофии (атрофический гастрит) или резекции (удаление части органа) желудка. В то время как атрофический гастрит встречается у пожилых с частотой в 70-80%.
Причины же атрофического гастрита также отличаются разнообразием. Но у пожилых, значимую роль в этом играет аутоиммунная агрессия.
Антитела к обкладочным клеткам желудка или непосредственно самому фактору Касла встречаются у 90% пациентов с атрофией слизистой желудка. Однако на сегодня не ясно – являются ли они самостоятельной причиной таких гастритов, или развиваются как на фоне уже имеющегося нарушения.
Наследственность
Многие клиницисты обращают внимание на «преемственность» риска В12-дефицита среди близких родственников. Ведь у 20-30% пациентов с анемией и атрофическим гастритом в семье уже были (или есть) аналогичные заболевания.
Кроме того, среди пациентов без семейной предрасположенности средний возраст дебюта В12-анемии составляет 66 лет, а с отягощенной наследственностью — 51 год.
Дефицит В12 в питании
Не секрет, что у пожилых людей часто появляется склонность к растительной пище. Тогда как потребление мясных и молочных продуктов, а также яиц – сильно снижается или вообще прекращается. А ведь именно эти продукты являются незаменимым источником витамина В12, что также объясняет частоту В12-анемии у вегетарианцев.
Дисбактериоз кишечника или «глисты»
Дефицит витамина В12 может обусловлен и «простой конкуренцией», поскольку бактерии и паразиты довольно «прожорливы» в его отношении.
При этом, «ускоренному» размножению бактерий способствуют склонность пожилых к запорам и частота дивертикулеза кишечника. А среди глистных инвазий, наибольшее значение имеет широкий лентец.
Как заподозрить дефицит В12
Слабость, утомляемость, учащенное сердцебиение и другие «классические» (железодефицитные) признаки анемии, при недостатке В12 выражены очень слабо. И, в большинстве случаев, заставляют обратиться к врачу только по достижении тяжелой степени тяжести (гемоглобин на уровне 60-40 г/л и меньше).
При этом среди жалоб, провоцирующих обратиться за помощью – симптомы ухудшения сопутствующих заболеваний (стенокардия, аритмия, ИБС и другие), декомпенсация которых обусловлена длительным кислородным голоданием тканей (гипоксия) и нарушением «текучести» крови.
Еще одним, почти обязательным, признаком В12-дефицитной анемии пожилых является поражение периферических нервов, или фуникулярный миелоз.
Правда, признаки такой нейропатии выявляются только при тщательном осмотре, ведь:
- слабость в конечностях
- постоянное ощущение холода в ногах,
- онемение,
- покалывания
- и нарушение чувствительности
по мнению самих пожилых пациентов – «явление в этом возрасте нормальное», и «ноги у стариков мерзнут всегда». А значит и поводом для обследования такие симптомы быть «точно» не могут.
Обследование
1. Клинический анализ крови
«Картина крови» при В12-дефиците характеризуется снижением эритроцитов, гемоглобина, увеличением эритроцитарных индексов (MCV, MCH), а также недостатком тромбоцитов и лейкоцитов.
Эритроциты, при этом, характеризуются неправильной формой и/или размером (макроцитоз). А появление таких отклонений обусловлено колоссальным значением витамина В12 для нормального синтеза ДНК.
При дефиците В12, очевидно, сильнее «страдают» наиболее активно делящиеся клетки, и одной из таких систем как раз и является кроветворная.
2. Анализ крови на витамин В12
Появление характерных отклонений в общем анализе крови, необходимо уточнить причину их возникновения. Поскольку не все макроцитарные анемии имеют В12-дефицитное происхождение.
3. Подтвержденный дефицит витамина В12, очевидно, нуждается в определении причин, от которых, очевидно, зависит эффективность дальнейшего лечения:
- обследование желудка комплекс «Гастрокомплекс» (0.H84.201) для выявления атрофии слизистой (лабораторный «аналог» ФГДС),
- анализ крови на антитела к обкладочным (париетальным) клеткам желудка (0.A56.201) и фактору Касла (9.0.A57.201);
Диагностика
Ввиду отсутствия специфических клинических проявлений болезни единственный способ установить диагноз – лабораторные исследования:
- общий анализ (мазок) обнаруживает низкий уровень гемоглобина, гипо-, нормо- или гиперхромию;
- биохимический анализ позволяет определить наличие или отсутствие дефицита фолиевой кислоты или цианкобаламина;
- мазок периферической крови выявляет высокий уровень распределения эритроцитов и макроцитарные изменения в красных кровяных клетках.
Поскольку макроцитарную анемию могут вызвать разные патологии и заболевания (по сути, она является их симптомом), проводят комплексную диагностику для установления точной причины – УЗИ, КТ, МРТ, рентген, эндоскопию, гастроскопию и ряд других исследований. Достаточно часто анемия выявляется случайно при обследовании пациента по другому поводу.
Гиперхромная анемия при миелодиспластическом синдроме
Синдром миелодисплазии выделен в связи с характерными гиперхромными изменениями в крови после применения химиотерапии, лучевого воздействия на костный мозг в лечении опухолей, лейкозов.
В этом случае происходит токсическое действие на процесс кроветворения в клетках мозга. На фоне тяжелых симптомов основного заболевания у пациента появляется:
- одышка;
- повышенная утомляемость;
- резкое головокружение и тахикардия при малейшей нагрузке.
Диагноз ставится на основании типичной картины крови.
Лечение макроцитарной анемии
Терапевтическая схема разрабатывается индивидуально для каждого пациента в зависимости от тяжести состояния и причины патологии.
При легких формах, обусловленных витаминной недостаточностью, достаточно коррекции режима питания. Диета должна содержать большое количество белка животного происхождения, витаминов и железа. Пациентам назначают витаминные препараты для лечения макроцитарной анемии, такие как B12 Анкерманн (источник цианкобаламина), Фолацин (источник фолиевой кислоты).
При среднетяжелых и тяжелых формах пациента госпитализируют и вводят витамины парентерально.
Если анемия является следствием какого-либо заболевания, обязательно требуется проведение соответствующей терапии.
При чрезмерном снижении уровня гемоглобина осуществляют переливание эритроцитарной массы.
Профилактика
Соблюдение принципов здорового питания, поддержание хорошего уровня витаминов В9 и В12, железа – самый простой и важный способ защиты от гиперхромного малокровия, особенно для беременных. Диета, используемая для его лечения, одновременно носит и профилактический характер. Дополнительно стоит:
- регулярно посещать гастроэнтеролога;
- заниматься спортом;
- отказаться от курения;
- не контактировать с ядохимикатами;
- гулять на свежем воздухе;
- своевременно лечить инфекционные заболевания, выводить паразитов;
- принимать витаминно-минеральные комплексы.
Осложнения
Низкий уровень гемоглобина означает также и недостаток кислорода. Из-за этого развиваются тахикардия, повышается артериальное давление. Если не начать лечение, это может привести к дистрофии тканей и органов, нарушению кровообращения, миокардиодистрофии с увеличением размера сердца, сердечной недостаточности.
Дефицит витамина B12 вызывает различные неврологические заболевания.
Если патология обусловлена патологиями костного мозга, есть риск развития лейкемии.
Картина крови
В периферической крови обнаруживается:
- резкое снижение количества нормальных эритроцитов;
- умеренная лейкопения и тромбоцитопения;
- в мазке крови видны различные измененные по строению, размерам и форме эритроциты (мегалоциты, мегалобласты), в них опытный лаборант находит типичные ядерные тельца Жолли и кольца (из-за пристеночного расположения ядра).
Язык отличается не только малиновым оттенком, но и сглаженностью рисунка, отечностью
Стадии дефицита железа
В настоящее время выделяют несколько стадий дефицита железа:
1. Предрасположенность к развитию железодефицита (вегетарианство, подростковый возраст в сочетании с нарушением менструального цикла у девочек, частые роды, наличие хронических заболеваний ЖКТ или женской репродуктивной системы, связанных с кровопотерей).
2. Предлатентный дефицит железа. На этой стадии нет никаких лабораторных критериев дефицита железа, однако можно определить повышение абсорбции 59Fe3+ в ЖКТ, которое может превышать 50 % (в норме 10–15 %).
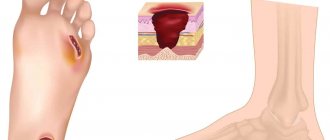
3. Латентный дефицит железа. Характеризуется развитием сидеропенического синдрома, снижением запасов железа в организме по данным лабораторных исследований.
4. ЖДА . Диагноз устанавливается при снижении концентрации гемоглобина до менее 120 г/л у женщин и 130 г/л у мужчин.
Последствия для здоровья
В детском возрасте гиперхромная анемия опасна задержкой умственного и физического развития. Ребенок будет в большей степени подвержен различным заболеваниям, его иммунитет не в состоянии справляться с инфекциями. Такие дети болеют долго и тяжело.
Опасна анемия для беременных женщин, у которых могут начаться преждевременные роды. Плод будет страдать от нехватки питательных веществ, ребенок может родиться с недовесом и аномалиями развития. Поэтому во время беременности нужно регулярно посещать акушера-гинеколога.
К иным последствиям анемии относят: кардиомиопатию, тахикардию, сердечную недостаточность. Поэтому лечение данного нарушения должно быть своевременным.
Автор статьи:
Шутов Максим Евгеньевич | Гематолог
Образование: В 2013 году закончен Курский государственный медицинский университет и получен диплом «Лечебное дело». Спустя 2 года окончена ординатура по специальности «Онкология». В 2021 году пройдена аспирантура в Национальном медико-хирургическом центре имени Н. И. Пирогова. Наши авторы
Эпидемиология
Впервые ЖДА описал немецкий врач Й. Ланге в 1554 г., а препараты для ее лечения впервые применил Т. Сиденгам в XVII в. Анемии, развивающиеся в результате дефицита железа в организме, наиболее широко распространены в клинической практике. По данным ВОЗ, около 2,5 млрд человек на Земле имеют скрытый дефицит железа и 1 млрд человек страдает ЖДА.
У женщин она наблюдается в 2–5 раз чаще, чем у мужчин , на 2-м месте по частоте встречаемости дети .
Достоверно доказано влияние ЖДА на увеличение частоты материнской и детской смертности. ЖДА встречаются у 12–13 % детей в возрасте от 6 мес. до 2 лет. В развивающихся странах этот показатель значительно выше: в Индии и странах Африки он достигает 72–76 %. В развитых странах Европы и Северной Америки ЖДА выявляется у 7,5–11 % всех женщин детородного возраста, а у 20–25 % наблюдается скрытый тканевой дефицит железа. Значительно большая частота ЖДА в странах Азии, Африки и Латинской Америки, где она достигает эпидемических величин и составляет 45–60 %. Из всех анемий, встречающихся в клинической практике, около 80 % являются железодефицитными. В Российской Федерации сведений по частоте ЖДА нет, однако, по нашим данным, в Москве ее частота составляет 30–35 % среди женщин детородного возраста, а скрытого дефицита железа — до 60 %.