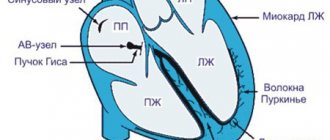
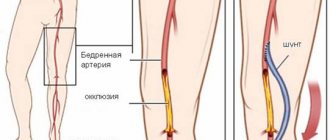
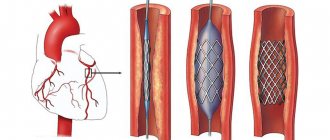
Операция аортокоронарного шунтирования — хирургическое вмешательство, которое выполняется при снижении кровотока коронарных артерий более 50%, и заключается в создании обходного анастомоза (шунта) пораженного участка. Цель операции — восстановление кровообращения сердечной мышцы. Это единственный радикальный путь лечения синдрома стенокардии при ишемической болезни.
Обходное соустье выполняется методом пересадки участка вены с нижней конечности, предплечья либо грудной мышцы. Во многих странах операция проходит под общим наркозом с использованием искусственного кровообращения. Для аортокоронарного шунтирования сердца в Германии используются только инновационные методики кардиохирургии, что позволяет проводить подобные операции на «работающем» сердце.
Эти малоинвазивные методики позволяют производить хирургическое вмешательство через небольшой разрез на грудной клетке. Манипуляция выполняется без аппарата искусственного кровообращения, что исключает риск развития сосудистых осложнений, инфицирования и сокращает восстановительный период.
Операция аортокоронарного шунтирования устраняет загрудинную боль при средних и тяжелых формах стенокардии. Это самый эффективный метод, позволяющий пациентам выполнять физическую нагрузку без боли и одышки и продолжать вести активный образ жизни.
Показания для хирургического лечения коронарных сосудов
Аортокоронарное шунтирование — формирование обходного кровотока стенозированных сосудов — производится по специфическим показаниям:
- сужение левой коронарной артерии более чем на 50%;
- устойчивость к терапевтическим методам лечения стенокардии;
- нарушение сокращения миокарда;
- обширная зона ишемии;
- атеросклеротическое поражение нескольких сосудов;
- поражение артерий у пациентов с сопутствующей патологией;
- сужение коронарных сосудов более 70%.
2.Подготовка к шунтированию
Перед проведением шунтирования головного мозга необходимо проведение медосмотра и некоторых стандартных тестов: ЭКГ, общий и клинический анализ крови и мочи, флюорографию. Специальными обследованиями перед проведением шунтирования мозга является следующее:
- МР, КТ или внутриартериальная ангиография;
- Баллонное обследование окклюзии артерии;
- Допплерография артерий мозга.
За 2 недели до операции пациенту нельзя курить, пить и принимать наркотики. Также необходимо приостановить приём нестероидных противовоспалительных препаратов.
Посетите нашу страницу Нейрохирургия
Шунтирование сердца в клиниках Германии: план обследования
Исследование функционального состояния миокарда состоит из следующих процедур:
- осмотр кардиохирурга (составление тактики лечения, объясняется суть операции);
- электрокардиографическая (ЭКГ) регистрация состояния сердца;
- определение работы сердца в условиях нагрузки (запись ЭКГ после велоэргометрии);
- суточное наблюдение за работой миокарда (холтеровское мониторирование);
- УЗИ сердца;
- доплер-исследование периферических сосудов;
- суточный мониторинг кровяного давления.
Затем производится коронарография, которая определяет состояние каждого сосуда сердечной мышцы. В клиниках Германии коронарография чаще всего проводится с одновременным шунтированием сосудов. В России эти манипуляции проводят последовательно, что требует повторного хирургического воздействия на организм.
Коронарография осуществляется введением пластиковой трубки с камерой в поврежденный сосуд. На мониторе визуально определяется уровень проходимости коронарной артерии. Процедура может выполняться с одновременными лечебными манипуляциями. Выявление ишемической болезни миокарда является показанием для шунтирования сердца.
Ожидаемые эффекты
Эффективность процедуры разнится, зависит от исходных данных. Как правило, после оперативного лечения пациент может рассчитывать на значительное улучшение состояния.
- Количество приступов стенокардии после шунтирования коронарных артерий падает до нуля. Нет не болевых ощущений, ни прочих симптомов. Это серьезно сказывается на уровне жизни. В положительном ключе.
- Вероятность инфаркта также становится существенно меньше. По разным оценкам, успешное шунтирование сосудов сердца снижает вероятность острого нарушения кровообращения в миокарде в 3-4 раза. Риски выравниваются и становятся примерно такими же, как у здоровых людей.
- Повышается физическая выносливость, переносимость нагрузок. Это результат адекватного питания самого миокарда, мышечной, нервной ткани. Пациент может самостоятельно ходить, в том числе без проблем поднимается по лестницам.
Однако, больным с шунтом все же не рекомендуется превышать допустимую, рекомендуемую норму. Как часто, с какой интенсивностью можно заниматься физической активностью, лучше уточнить у своего кардиохирурга.
- Количество препаратов постепенно уменьшается. Нет необходимости принимать лекарства в прежнем объеме. Хотя определенный минимум все-таки сохраняется. Это поддерживающая мера.
- Риск внезапной смерти также становится ниже.
- Пациент может работать. Выполнять обязанности по дому.
Операция устраняет все возможные риски. Позволяет вернуться к здоровой жизни.
Преимущества операции на коронарных сосудах в Германии
Хирургическое вмешательство при ишемии в немецких клиниках выполняется минимально инвазивным методом на работающем сердце без использования искусственного кровообращения. Доступ делается через переднебоковую поверхность грудной стенки. В третьем или четвертом межреберье делают разрез длиной до 10 см, затем выполняется аортокоронарное шунтирование.
Методика операции без отключения сердца от системы кровообращения заключается в отделения участка грудной артерии. Затем отрезают участок сосуда для имплантации и сшивают рассеченные концы. После этого переходят к наложению анастомозов. Преимущества шунтирования сердца:
- отсутствие рисков, которые случаются при использовании искусственного кровообращения;
- минимальное повреждение сердечной мышцы;
- незначительные объемы перелитой крови;
- короткие сроки лечения и восстановительного периода;
- отсутствие мозговых сосудистых осложнений и инфицирование послеоперационной раны.
Аортокоронарное шунтирование, выполняемое в немецких кардиологических клиниках, позволяет пациенту уже через 7-10 дней приступить к работе и активной жизни. Развитие кардиологической хирургии в Германии дает шансы тяжелым пациентам на выздоровление. После многих лет страданий приступами стенокардии и одышки при незначительных нагрузках больные избавляются от боли на следующий день после шунтирования.
Послеоперационные осложнения
Осложнения после операции могут развиться как со стороны сердечно-сосудистой системы, так и со стороны других органов и систем. Последние, как правило, зависят от возраста пациента и наличия хронических заболеваний. К ним относятся: декомпенсация сахарного диабета, обострение бронхиальной астмы, инсульт и так далее. Сердечная недостаточность, острый инфаркт миокарда и некроз миокарда – послеоперационные последствия со стороны сердца. Если вас интересует вопрос о том, сколько живут после операции, то ответ будет неоднозначным. Длительность жизни после операции зависит от многих факторов – это возраст больного, наличие хронических заболеваний, образ жизни после операции и так далее.
На приеме кардиолог расскажет, как избежать осложнений и какую группу инвалидности после шунтирования получит больной.
Кардиологические операции без аппарата ИК
Аортокоронарное шунтирование без остановки сердца выполняется только при наличии специального оборудования, которое сводит сокращения миокарда к минимуму. Соустье делается из грудной артерии либо вены. Использование инновационной методики в Германии позволяет снизить риски, связанные с остановкой сердца и прохождением крови через аппарат ИК.
Однако бывают случаи в немецкой практике, когда по медицинским показаниям врачи вынуждены проводить пациентам шунтирование с применением аппарата искусственного кровообращения.
Реабилитация
{banner_banstat10}
На раннем этапе восстановления пациент находится в реанимации от 2-х до 10 суток. Плюс-минус по потребности. Все это время врачи обрабатывают швы.
- На период до полугода пациенту запрещены тяжелые физические нагрузки. Максимум 3-4 кг без наклона, распределяя вес на обе руки. Поскольку кости грудины только срастаются. Не стоит создавать себе дополнительные проблемы. Чтобы облегчить состояние можно надевать специальные бандажи.
- Ходить нужно, но перетруждаться — запрещено. Медленный шаг. При этом, чтобы избежать венозно-лимфатического застоя рекомендуется надевать специальные компрессионные чулки.
- В течение пары месяцев нужна диета с высоким содержанием железа, витаминов и белка, но переедание исключено, это повышенная нагрузка на сердце.
Внимание:
Пока человек находится в больнице, не может нормально передвигаться, рекомендована дыхательная гимнастика. Так пациент предотвратит воспаление легких.
- После выписки физические нагрузки повышают постепенно. Как только кости грудины срастутся, можно заниматься ЛФК.
Реабилитация продолжается после выписки в специальном центре. Раз в год пациенту рекомендуется посещать санаторий.
Кардиологические операции с искусственным кровообращением (ИК)
Доступ при традиционном методе выполняется по средней линии грудины. Сердце выключается из круга кровообращения. Жизнедеятельность поддерживается с помощью аппарата ИК, который подсоединяется к аорте и полым венам. Кровь насыщается кислородом и попадает в организм. Процесс газообмена происходит в самом аппарате ИК, где кровь также сохраняет необходимую температуру и фильтруется.
Аортокоронарное шунтирование выполняется на неработающем сердце. Хирург делает анастомоз между здоровым участком коронарных сосудов и веной. Минимальное время для выполнения операции составляет от трех до пяти часов. Сердце включают в кровообращение после окончания оперативного вмешательства на всех пораженных сосудах.
Аортокоронарное шунтирование бывает различной степени сложности. Это зависит от количества пораженных артерий и общего состояния пациента. Поэтому продолжительность процедуры определяется индивидуально. Чем больше анастомозов следует имплантировать, тем больше времени занимает процедура.
Результаты
Экспериментальная часть
Были использованы тимпанальные шунты, производимые ЗАО «МедСил» (Мытищи, Россия) из силиконовой резины, импрегнированной наночастицами серебра (1—3%). Эта композиция позволяет дополнить гидрофобные свойства материала бактерицидными, что немаловажно при длительно «открытой» барабанной полости [11].
Разработаны два вида функциональных тимпанальных шунтов (ФТШ), отличающихся типом щелевого клапана на закрытом фланце вентиляционной трубки, обращенном в наружный слуховой проход. I тип щелевого клапана имел вид вертикального разреза, проходящего через центр силиконовой мембраны, плотно закрывающей фланец шунта. II тип представлял две неполные мембраны, перекрывающие друг друга по типу «закрытой диафрагмы фотоаппарата» (рис. 1). По нашему мнению, в статичной ситуации створки клапана должны быть закрыты, а при барометрических изменениях должны пропускать воздух, уравновешивая разницу воздушного давления между барабанной полостью и наружной средой.
Рис. 1. Схема щелевых клапанов. а — клапан I типа, б — клапан II типа.
Для объективной оценки работы щелевых клапанных механизмов ФТШ была разработана экспериментальная модель. Наружный слуховой проход с БП был представлен силиконовой трубкой длиной 1,3 см. В закрытый дистальный конец трубки запаивали шунт. В зависимости от использованного типа ФТШ получили два вида модели. На экспериментальной модели № 1 изучали работу обычного щелевого клапана, на модели № 2 — диафрагмального. Модели плотно соединяли с ушным вкладышем, закрепленным на пробнике компьютерного анализатора АТ 235 h («Interacustics», Дания), и проводили тест в режиме ETF2 (рис. 2). Аппарат нагнетал воздух и фиксировал барометрический показатель, при котором происходит сброс давления. Эксперимент повторяли 10 раз и вычисляли среднее значение барометрического показателя.
Рис. 2. Подготовка к проведению эксперимента (модель зафиксирована на пробнике компьютерного анализатора АТ 235 h).
В результате проведенных экспериментов было отмечено, что при нагнетании воздуха в модель № 1 (режим ETF2) не происходит подъема давления — изучаемый показатель постоянно равен 0 даПА. Это косвенно свидетельствует о том, что у данной конструкции щелевого клапана отсутствует барометрический порог резистентности. Аналогичный эксперимент с моделью № 2 приводил к подъему давления до 123,06 даПА, после чего происходило резкое его падение до исходного «нулевого» порога (рис. 3). Полученные нами результаты свидетельствуют о том, что модель № 2 работает как барометрический клапан. Диафрагмально-щелевой клапан открывается, когда разница давления составляет 123,06 даПА. С учетом результатов, полученных в эксперименте, и особенностей физиологических механизмов пассивного открытия СТ в клинической части работы был применен ФТШ, оснащенный диафрагмально-щелевым клапаном (клапан II типа).
Рис. 3. Результаты эксперимента в режиме ETF2. а — модель № 1; б — модель № 2.
Клиническая часть
Предоперационное обследование больных (n
=104) показало, что все пациенты предъявляли жалобы на одностороннее снижение слуха и ощущение заложенности в ухе. У 86 (82,7%) больных воспаление среднего уха носило рецидивирующий характер. Длительность последнего эпизода заболевания составила 67,85±8,27 сут (
р
<0,05). При этом проведенное консервативное лечение (катетеризация СТ с введением противовоспалительных препаратов, пневмомассаж БП, деконгестанты и прицельная анемизация слизистой оболочки устья СТ, интрамиатальные компрессы и физиотерапевтическое воздействие) было не эффективно. Эндоскопическое исследование полости носа выявило выраженную деформацию перегородки носа и увеличенные задние концы нижних носовых раковин, которые доходили до устья С.Т. При диагностической анемизации задние отделы нижних носовых раковин не сокращались. С помощью ПАРМ у 100% пациентов было выявлено выраженное нарушение носового дыхания: снижение суммарного объемного потока — 280,22±11,03 см3/с и повышение суммарного сопротивления — 0,58±0,03 Ра (
р
<0,05). При отомикроскопии у 52 (50%) больных (52 уха) было выявлено втяжение и истончение БП, наличие единичных петрификатов с участками атрофии. У 52 (50%) пациентов (52 уха) наблюдали контуры экссудата в барабанной полости. У всех больных камертональный опыт Ринне (C128) был отрицательным. При опыте Вебера — латеризация в больное ухо — у 82,7% пациентов, без четкого смещения — у 17,3%. Результаты опыта Федеричи (С128, 512) были сомнительными у 93 (89,4%) пациентов, у 11 (10,6%) — положительными. По данным ТПА у 61 (58,7%) больного была выявлена низкочастотная кондуктивная, у 43 (41,3%) — смешанная тугоухость, при этом костно-воздушный интервал (КВИ) составил 29,84±4,56 дБ. При акустической тимпанометрии наблюдалось изменение показателей градиента и комплеанса. У 52 (50%) пациентов (52 уха) компьютерный анализатор среднего уха АТF 235 h зафиксировал тип С тимпатограммы, у 52 (50%) больных (52 уха) — тип В. При этом давление в барабанной полости составило — 266,37±11,08 даПА (
р
<0,05). При исследовании функции СТ с проведением функциональных проб в режиме ETF1 в 100% исследований (104 уха) положительной динамики в значениях интратимпанальной компрессии выявлено не было. Таким образом, у 52 (50%) больных (52 уха) выявлен катаральный средний отит, у 52 (50%) пациентов (52 уха) — экссудативный. Патологический процесс в 100% случаях (104 уха) был связан с выраженной длительной ДСТ.
Для последовательного решения поставленных перед нами задач и в соответствии с принципом рандомизации все больные были разделены на две клинические группы, отличающиеся способом лечения длительной ДСТ (вид тимпанального шунта). В 1-й клинической группе (n
=52) при катаральной и экссудативной форме среднего отита шунтирование БП проводили стандартными шунтами (СШ). Во 2-й клинической группе (
n
=52) при экссудативном отите использовали СШ, в стадии катара или при прекращении процесса экссудации — ФТШ, оснащенный диафрагмально-щелевым клапаном. Виды тимпанальных шунтов, которые применялись в клинической части работы, представлены на рис. 4.
Рис. 4. Силиконовые тимпанальные шунты. (слева — ФТШ, справа — С.Ш. На заднем фоне «лапка» пинцета).
В зависимости от формы воспалительного процесса в среднем ухе в каждой клинической группе было выделено по две подгруппы (по 26 человек/ушей в каждой): подгруппы, А составили пациенты с катаральным средним отитом; подгруппы В — с экссудативной формой воспаления в среднем ухе. Эффективность проводимого лечения оценивали по местным клиническим проявлениям, срокам восстановления вентиляционной функции СТ и остроты слуха, по характеру и частоте осложнений.
Риски применения аппарата ИК
Шунтирование сосудов с открытым доступом и остановкой сердца связано с опасностью развития следующих осложнений:
- возможность кровотечения;
- некроз участка сердечной мышцы;
- неполное заращение грудного разреза;
- почечная недостаточность;
- венозная тромбоэмболия;
- инсульт мозговых артерий;
- амнезия (потеря памяти);
- большие рубцы на грудной клетке;
- выраженный болевой симптом.
После операции, до полного заживления послеоперационной раны, нельзя принимать ванну, пользоваться гелями, тереть в области шва. Не следует принимать горячий душ, пользоваться лосьонами.
Прогнозы и сроки службы шунтов
Перспективы в целом благоприятные. Вероятность инфаркта снижаются в 2-4 раза, то же касается внезапной смерти.
Если сердце не изменено, можно вернуться к полноценной жизни с небольшими ограничениями в физических нагрузках. Операция никак не влияет на ее продолжительность, а уменьшает риски неотложных состояний.
Шунт в идеальных условиях служит около 10-15 лет. Но существуют погрешности. Поэтому стоит рассчитывать на сроки в 7-8 лет или около того.
После ― вновь возникают показания к операции по шунтированию сосудов сердца и нужна вспомогательная терапия.