Анемия может стать причиной огромного количества проблем: от усталости и выпадения волос до сердечной недостаточности и даже онкологических заболеваний в долгосрочной перспективе. По оценкам ВОЗ, в мире разными видами анемии страдают более полутора миллиарда человек, что составляет четверть всего населения Земли. Причем зачастую патологии встречаются у детей дошкольного возраста – 50%, а реже всего у мужчин – 12%.
В большинстве случаев люди даже не обращают внимания на основные признаки анемии (постоянную усталость, сухость кожи, бледность), считая их недостаточным поводом для обращения к врачу. Конечно, такие симптомы действительно не всегда свидетельствуют о заболевании, его нельзя диагностировать лишь по наличию этих симптомов. И тем более нельзя самостоятельно начинать прием железосодержащих препаратов – это может привести к тяжелым осложнениям. При этом для полноценной диагностики анемии недостаточно просто сдать кровь на гемоглобин. Например, у курящих людей уровень гемоглобина и эритроцитов, как правило, в норме: моноокись углерода, которая содержится в сигаретах, при соединении с гемоглобином образует вещество карбоксигемоглобин, не способный переносить кислород. Поэтому для компенсации кислородного голодания уровень гемоглобина повышается. Получается, что необходимо комплексное исследование, отражающее истинное состояние системы кроветворения и здоровья организма в целом. К тому же важно знать, чем именно вызвана анемия. У пожилых людей, например, она часто возникает на фоне опухолевого процесса в желудочно-кишечном тракте. Есть разновидность анемии, связанная с плохим усвоением витамина B12 и для ее выявления следует определить уровень витамина В12 в сыворотке крови и оценить показатели морфологии эритроцитов. Для оценки состояния системы кроветворения и диагностики истинных причин анемии эксперты лабораторной диагностики ДІЛА разработали комплексную скрининговую программу 175 «Определи причину анемии». Она позволит исключить или подтвердить наличие и характер анемии, установить ее причины и степень тяжести.
Кому рекомендовано обследование?
- в профилактических целях: людям с повышенной физической активностью и спортсменам, детям в периоды активного роста и полового созревания, донорам крови, людям, придерживающимся вегетарианской диеты, детям и взрослым с диагностированными паразитарными заболеваниями;
- женщинам на этапе планирования и во время беременности;
- мужчинам, женщинам и детям при наличии жалоб, которые сопровождаются характерными признаками анемии, после сильных кровопотерь, при ранее диагностированной анемии для контроля лечения;
- детям с врожденным дефицитом железа.
Программа может быть использована для первичной диагностики анемии и дифференциальной диагностики анемий, обследования пациентов с высокими рисками развития заболевания и оценки эффективности лечения.
О заболевании
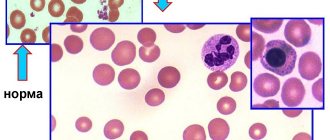
Что это? Анемия (малокровие) – это уменьшение содержания гемоглобина и/или снижение количества эритроцитов в единице объема крови, приводящее к снижению снабжения тканей кислородом.
Чем вызвана? Причины анемий разнообразны и могут быть тесно связаны со следующими факторами:
- Соматические заболевания – болезни печени и почек, аутоиммунные, инфекционные и воспалительные процессы.
- Острая и хроническая потеря крови. Острой считается кровопотеря с объемом крови более 500-700 мл (у взрослых), которая возникает в течение короткого промежутка времени. Она бывает видимой (кровотечение из раны, кровавая рвота, маточные и носовые кровотечения) и первоначально скрытой (кровотечение в кишечник, в полость живота и/или плевры, обширные гематомы). Хронические потери крови развиваются на фоне незначительных, но продолжительных кровопотерь (обильных и длительных менструаций, язвы желудка, рака, геморроя, процедур гемодиализа). С течением времени даже незначительные потери истощают запасы железа в организме, когда количество теряемого организмом железа превышает его поступление с пищей. В результате железодефицита нарушается синтез гемоглобина
- Неполноценное питание, нехватка витаминов и микроэлементов. Анемия развивается на фоне дефицита железа, витамина В12 и фолиевой кислоты. Это может быть связано как с недостатком необходимых организму веществ в рационе (например, при жестких диетах или у вегетарианцев), так и со снижением всасывания железа в результате различных заболеваний двенадцатиперстной кишки и начальных отделов тонкой кишки (энтериты, опухоли, состояния после операций на тонком кишечнике). При состояниях, вызывающих снижение уровня белков крови, которые являются переносчиками железа (нефротическом синдроме, нарушении белково-синтетической функции печени, синдроме нарушенного всасывания, алиментарной недостаточности), также может наблюдаться снижение количества железа и, как следствие, анемия.
- Нарушение кроветворения. Анемия возникает при недостаточном формировании эритроцитов в костном мозге (к примеру, при истощении костного мозга или его поражении токсическими веществами, ионизирующей радиацией), на фоне преждевременного и чрезмерного разрушения эритроцитов в кровяном русле (например, при гемолизе). Также анемия может возникать при образовании вторичных очагов (метастазов) опухолевых клеток в костном мозге, нарушении выработки небелковой части гемоглобина (гема) и накоплении его токсичных продуктов, а также нарушении регуляции синтеза эритроцитов (уменьшение продукции гормона, который стимулирует рост и размножение эритроцитов – эритропоэтина).
В зависимости от причин, анемия классифицируется на железодефицитную, вызванную кровопотерей или недостаточным поступлением или усвоением железа; В12-дефицитную и фолиеводефицитную, вызванную недостаточным поступлением в организм или усвоением соответственно цианокобаламина и фолиевой кислоты; апластическую, вызванную нарушением образования в костном мозге эритроцитов; и гемолитическую, при которой эритроциты в организме разрушаются слишком быстро. Самой распространенной формой анемии является железодефицитная – ее диагностируют у 80-90% пациентов, у которых снижено количество эритроцитов и/или гемоглобина в крови. Железодефицитные состояния развиваются постепенно. Вначале создается отрицательный баланс железа, при котором потребности организма в нем и его потери превышают объемы его поступления с пищей. Это может быть обусловлено потерей крови, беременностью, грудным вскармливанием, скачками роста в период полового созревания, нарушением всасывания микроэлементов в ЖКТ или недостаточным употреблением продуктов, содержащих железо, как при вегетарианстве.
В норме железо всасывается в тонком отделе кишечника, однако при некоторых хронических заболеваниях ЖКТ возникает синдром мальабсорбции – нарушение всасывания из пищи витаминов, микроэлементов и других полезных веществ. В крови железо транспортируется белком трансферрином в места его расходования или накопления. При железодефицитных состояниях количество свободного трансферрина в крови повышается, а уровень сывороточного железа снижается. Выработка гемоглобина в костном мозге происходит не так активно, в результате чего и развивается железодефицитная анемия со всеми клиническими проявлениями малокровия.
Основные причины дефицита железа
В целом ряде случаев наблюдаются признаки недостатка железа в организме, приводящие в конечном итоге к анемии. К самым частым причинам низкого уровня железа относят следующие:
- уменьшенное потребление с пищей;
- патология всасывания элемента в кишечнике;
- наличие хронической кровопотери;
- увеличенные потребности в железе во время беременности;
- избыток полифенолов в пище (например, при употреблении зелёного чая или кофе);
- большие кровопотери при травмах.
В группу повышенного риска развития железодефицитного состояния входят недоношенные дети и дети, в рационе питания которых наблюдается недостаток железа, девочки — подростки, в начале менструаций. В особую категорию людей с анемией выделяют беременных женщин, у которых многократно возрастает необходимость в железе. Доноры крови также могут отмечать признаки недостатка железа.
Низкое количество железа часто встречается у вегетарианцев по причине дефицитного приема элемента с пищей. У людей с заболеваниями пищеварительной системы, а также при развитии хронических инфекционных заболеваний анемия развивается из-за нарушения усвоения железа пищеварительной системой.
Следует учитывать, что анемия – это не всегда безобидное и легко корректируемое состояние. Под маской недостатка железа в крови часто скрываются достаточно серьёзные хронические заболевания. Анемия часто является одним из симптомов сердечно-сосудистых заболеваний, хронических болезней мочевыделительной системы, проявлением синдрома мальабсорбции (или нарушения всасывающей функции кишечника). Анемия у женщин может наблюдаться при обильных менструальных кровотечениях. Другими грозными патологиями, сопровождающимися дефицитом железа в крови, являются онкологические болезни и хронические воспалительные процессы в кишечнике.
Симптомы и осложнения
Степень выраженности анемии зависит от тяжести болезни и скорости ее развития. Чем ниже уровень гемоглобина и чем быстрее развивается анемия, тем более выражена клиническая картина.
Выделяют общие (неспецифические) признаки анемии и проявления, характерные для определенного типа заболевания. К неспецифическим признакам относят:
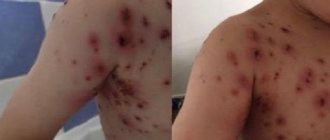
- бледность кожных покровов;
- слабость и повышенную утомляемость;
- сонливость;
- частые головокружения и обмороки;
- шум в ушах;
- «мушки» перед глазами;
- одышку и учащенное сердцебиение, учащенный пульс.
Отсутствие этих симптомов не исключает наличия анемии, поскольку при легкой и среднетяжелой форме болезни, а также ее медленном развитии, клиническая картина может быть смазанной.
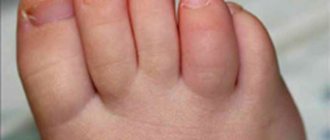
При железодефициной анемии наблюдают сухость и нарушение целостности кожи, ломкость ногтей и волос, появление изъязвлений и трещин в уголках рта, мышечную слабость. Может наблюдаться ощущение жжения языка, искажение вкуса в виде неукротимого желания есть мел, зубную пасту, землю, сырую крупу, сырое мясо, а также пристрастие к некоторым запахам (ацетона, бензина). К тому же при дефиците железа часто наблюдается поражение желудочно-кишечного тракта.
Нехватка витамина В12 может также проявляться проблемами с ЖКТ (в частности атрофическим гастритом) и неврологическими симптомами – к ним относятся парестезии, нарушения чувствительности, онемение конечностей. Крайне тяжелое течение анемии иногда сопровождается психическими нарушениями, галлюцинациями.
Клинические проявления при нехватке фолиевой кислоты весьма схожи с проявлениями дефицита витамина В12, но при этом отсутствуют неврологические симптомы и редко наблюдается воспаление языка.
Гемолитическим анемиям характерны желтушность кожи и слизистых, увеличение размера селезенки, склонность к формированию камней в желчных путях. При массивном гемолизе эритроцитов (гемолитическом кризе), помимо желтухи, анемии и ухудшения общего состояния, возможны тошнота, рвота, расстройства сознания, судороги, может развиваться острая почечная и/или сердечно-сосудистая недостаточность.
Апластическая анемия, возникающая на фоне угнетения пролиферации клеток костного мозга, характеризуется кровотечениями (носовыми, желудочно-кишечного тракта) и кровоизлияниями (преимущественно в области голеней, бедер и живота, а в местах инъекций образуются гематомы). Часто диагностируют бронхиты и пневмонии.
Как и симптомы, осложнения анемии могут быть общими и специфическими. К общим относятся:
- снижение артериального давления;
- ухудшение иммунитета и учащение инфекционных заболеваний;
- в период беременности – хроническая гипоксия плода, задержка внутриутробного развития;
- снижение интеллектуального и физического развития у детей.
Специфические осложнения развиваются при определенном виде анемии. К примеру, гемолитические анемии сопровождаются повышенными рисками развития желчнокаменной болезни, гемосидероза внутренних органов (чрезмерного отложения гемосидерина – пигмента, который образуется в процессе ферментативного расщепления гемоглобина), гемолитических кризов, увеличения размеров печени и селезенки.
Острые массивные кровопотери могут приводить к развитию полиорганной недостаточности (сердечно-сосудистой, почечной, дыхательной), ДВС-синдрома (расстройства гемостаза).
При дефиците витамина В12 осложнения часто затрагивают спинной мозг.
При анемиях, связанных с нарушением выработки или утилизации порфиринов (нарушение кроветворения), может развиваться сахарный диабет, недостаточность надпочечников, цирроз печени, проблемы с кровообращением.
Симптомы недостатка железа
Классическими клиническими признаками железодефицитного состояния считают:
Жалобы пациента на усталость и быструю утомляемость даже от привычной нагрузки. Основная причина заключается в недостаточном снабжение клеток и тканей организма кислородом. Слабость и отсутствие выносливости связано также с тем, что железо участвует в продукции энергии в виде молекул АТФ. В отсутствии достаточного количества кислорода, мышечная ткань переходит на анаэробные механизмы производства АТФ, что является менее эффективным и более обременительным для организма.Другими частыми симптомами анемии служат перепады настроения и раздражительность. Механизм этого процесса такой: недостаток железа в организме нарушает продукцию нейромедиатора дофамина и гормонов щитовидной железы, что приводит к гипотиреозу. Отсюда ощущение тревоги, стресса, раздражительность и перепады настроения.- Следующим симптомом железодефицитного состояния является снижение концентрации внимания. Как известно, кислород – один из факторов, обеспечивающих активность и высокую работоспособность головного мозга. Его недостаток при анемии – причина нарушения тонких когнитивных функций мозга. Многие пациенты с низким уровнем железа в организме испытывают приступы головокружения. Частые головокружения – также результат недостатка кислорода в эритроцитах. К этому же ряду симптомов анемии относят необъяснимые частые головные боли. Недостаток железа приводит не только к снижению содержания гемоглобина, но и нарушает образование ещё одного железосодержащего белка – миоглобина. Это приводит к болезненности м напряжению мышц лица, шеи и плеч, чем и объясняются частые головные боли при железодефицитном состоянии.
Ряд пациентов с анемией предъявляет жалобы на нарушение сна. Ферритин – основной белок, в котором находятся запасы железа, является одним из важнейших регуляторов сна. Бессонница при железодефицитном состоянии возникает при истощении резервов железа на самых ранних этапах развития патологического процесса, так как первым исчезает ферритин.- Видимые изменения при анемии у мужчин и у женщин приобретает кожа и ногти: поверхность губ выглядит сухой и потрескавшейся, ногти становятся хрупкими и продольно исчерченными. Ферритин является важнейшим компонентом, необходимым для нормального протекания процессов регенерации и обновления тканей, особенно кожи и её придатков (волосы, ногти). Истощение запасов ферритина приводит к ухудшению процессов клеточного восстановления в этих тканях. Кожа и слизистые оболочки пациентов с анемией, как правило, бледные, особенно это заметно при падении гемоглобина ниже 90 г/л. Прежде всего бледнеют те участки, где кровоток наиболее близок к поверхности кожи или слизистой оболочки: губы, конъюнктивы, ладони, ногтевые ложа.
- При показателях железа ниже нормы может наблюдаться синдром «беспокойных ног» или болезнь Уиллиса-Экбома. Недостаток элемента в организме приводит к нарушению баланса между синтезом дофамина и метаболизмом гормонов щитовидной железы. Для постановки такого диагноза необходимо наличие 4-х основных признаков: необходимость двигать ногами для преодоления неприятных ощущений в конечностях;
- неприятные ощущения в ногах возникают и усиливаются в состоянии покоя;
- неприятные ощущения частично или полностью исчезают в активном состоянии (бег, ходьба);
- необходимость двигать ногами и неприятные ощущения усиливаются к вечеру и часто являются причиной бессонницы.
Диагностика анемии
При появлении первых признаков заболевания важно обратиться к врачу для постановки точного диагноза. Важную роль в выявлении причин анемии играют сведения, полученные в ходе опроса пациента – возраст, наличие профессиональных факторов, характер рациона, наличие сопутствующих болезней, прием лекарств. Не менее важны и данные осмотра – цвет и состояние кожи, размер лимфоузлов, печени и селезенки, признаки поражения нервной системы.
Первый этап диагностики анемии обычно включает следующие исследования:
- Общий развернутый анализ крови. При анемии он показывает небольшие бледно окрашенные эритроциты, снижение показателей МНС (среднее содержание гемоглобина в эритроците), MCV (средний объем эритроцита), МСНС (средняя концентрация гемоглобина в эритроците), снижается концентрация гемоглобина и гематокрит. Общий анализ крови позволяет врачу оценить размер, форму и зрелость клеток крови.
- Ферритин. Этот биомаркер является наиболее специфичным и чувствительным параметром наличия запасов железа в организме, главным участником метаболизма железа и донором железа для клеток, которые испытывают в нем дефицит. Концентрация ферритина возрастает при железодефицитных анемиях, но может повышаться при заболеваниях печени и воспалении.
- Фолиевая кислота (витамин В9). Она способствует соединению глобина и гема в гемоглобине и миоглобине и является индикатором дифференциальной диагностики анемий, в частности для выявления или исключения фолиеводефицитной анемии.
- Железо – ключевой маркер диагностики железодефицитной анемии. При его нехватке в организме сывороточное железо очень быстро расходуется, при его избытке трансферрин полностью насыщается железом. Основной формой длительного хранения этого элемента является его комплекс с белком ферритином. Концентрация железа повышается при гемолитической, пернициозной и апластической анемии, снижается — при железодефицитной форме.
- Витамин В12 (цианокобаламин). Его дефицит может привести к развитию макроцитарной (мегалобластной) анемии.
В состав скрининговой программы 175 «Определи причину анемии» включен общий развернутый анализ крови и все указанные маркеры. Комплексное определение всех этих показателей позволяет врачу выявить точную причину анемии и дифференцировать ее от других опасных заболеваний.
Лабораторные исследования для первичной и дифференциальной диагностики анемий имеют важное значение и могут быть рекомендованы как с целью установки причины неспецифических симптомов, так и в качестве скринингового исследования, особенно в группах высокого риска развития анемий. В группу риска входят беременные и кормящие женщины, дети, лица с хроническими заболевания и болезнями желудочно-кишечного тракта, вегетарианцы, люди, испытывающих хронические стрессы.
Диагностика железодефицитного состояния
В настоящее время разработано несколько лабораторных тестов, необходимых для диагностики железодефицитного состояния. К основным из них относят определение следующих показателей крови:
- количество сывороточного железа;
- показатель общей железосвязывающей способности сыворотки (ОЖСС);
- процент насыщения железом трансферрина;
- количество ферритина;
- количество гемоглобина.
Важно понимать, что большой ошибкой служит выписка препаратов железа исключительно по результатам определения пониженного ферритина. При наличии мутации MTHFR, нарушающей переработку и усвоение железа, фолиевой кислоты, витамина В12, ферритин всегда оказывается низким, а сывороточное железо – высоким, что не позволяет назначать таким пациентам препараты железа.
Целями лабораторных тестов на железодефицитную анемию являются:
- выявление нарушения в обмене и метаболизме железа;
- определение природы анемии;
- оценка риска развития перегрузки организма железом.
Подготовка к лабораторным тестам на анемию несложная и достаточно стандартная. Сдавать кровь необходимо с утра, строго натощак (с 8-ми часовым перерывом после приёма пищи). За сутки перед проведением тестирования необходимо прекратить приём железосодержащих препаратов и/или мультивитаминов. Если накануне проводилась радиоизотопная диагностика, исследование метаболизма железа следует начинать не ранее, чем через 4-5 суток после её завершения. Также важно учитывать, что некоторые лекарственные средства могут искажать результаты тестирования. Например, эстроген или оральные контрацептивы могут повышать ОЖСС, а кортикостероиды и тестостерон, напротив, понижают ОЖСС.
Место препаратов железа при коррекции анемии у кардиологического больного
В случаях выявления истинной “коморбидной” ЖДА, не связанной с имеющейся кардиальной патологией (опухоли желудка и кишечника, кровоточащий геморрой, меноррагии у женщин, синдром мальабсорбции, гастроэзофагеальная рефлюксная болезнь, алиментарная недостаточность и др.), лечение должно быть направлено на устранение этой причины (по возможности) или коррекцию имеющихся нарушений (эрозивно-язвенных и опухолевых поражений ЖКТ, миомы матки, энтеритов и др.). При выявлении корригируемой причины ЖДА необходимы лечение (медикаментозное, хирургическое) основного заболевания и патогенетическая терапия препаратами железа (ПЖ). При наличии неустранимой или трудноустранимой причины (беременность, носовые кровотечения при наследственной геморрагической телеангиэктазии, меноррагии и др.) патогенетическая терапия ПЖ остается единственным способом коррекции дефицита Fe.
2.1. ПЖ при анемии у больных ИБС
В одном из исследований, посвященных проблеме сочетания ИБС с анемией, было показано, что у больных ИБС в сочетании с анемией легкой степени (Нв – 130–110 г/л) и латентным дефицитом Fe при коррекции показателей Hb, сывороточного Fe, общей железосвязывающей способности сыворотки на фоне применения препарата Сорбифер Дурулес (железа сульфат + АСК) уменьшились частота, длительность и интенсивность приступов стенокардии, снизилась потребность в приеме нитроглицерина, увеличилась толерантность к физическим нагрузкам, уменьшилась выраженность коморбидных клинических проявлений: отеки, одышка, ощущение сердцебиения, частоты сердечных сокращений [15].
2.2. ПЖ при анемии у больных ХСН
Лечение ПЖ анемии при ХСН вызывает достаточно большой интерес среди исследователей, т. к. оно относительно недорогое и имеются доказательства его эффективности, хотя остается немало нерешенных вопросов [58]. Заслуживают внимания результаты исследования, продемонстрировавшего эффективность внутривенного введения ПЖ 16 пациентам с ХСН без сопутствующей терапии ЭПО, на фоне чего были достигнуты достоверное увеличение среднего уровня Hb со 112 до 126 г/л, улучшение переносимости физической нагрузки по данным теста 6-минутной ходьбы и качества жизни в целом [59]. В другом исследовании на фоне лечения препаратами солей железа (Ферро-Фольгамма) и железосодержащих комплексов (Венофер) отмечены уменьшение выраженности клинических признаков сердечной недостаточности и переход пациентов в более благополучный ФК [60].
Было выполнено три рандомизированных плацебо-контролируемых исследования, посвященных применению ПЖ больными ХСН с наличием анемии. В одном из них 40 больных были рандомизированы и получали внутривенно ПЖ или плацебо [61]. Через 6 месяцев показатели Hb на фоне применения ПЖ повышались в среднем от 103 до 118 г/л и оставались стабильными в группе плацебо. Наряду с этим при лечении ПЖ отмечена положительная динамика концентрации натрийуретического пептида, показателей С-реактивного белка, ФВ ЛЖ и теста 6-минутой ходьбы. Другое исследование включило 35 больных ХСН, в течение 16 недель получавших внутривенно ПЖ или плацебо [62]. Было отмечено снижение ФК сердечной недостаточности по NYHA, улучшение общего состояния больных, по их самооценке, без улучшения толерантности к нагрузке, по данным тредмил-теста. Еще одно более масштабное рандомизированное плацебо-контролируемое исследование эффективности ПЖ среди больных ХСН включило 429 больных ХСН с наличием анемии [63]. Показано, что на фоне внутривенного введения препарата железополимальтозного комплекса наряду с повышением концентрации Hb отмечено значительное или умеренное улучшение состояния, по данным самооценки пациентов (50 и 28 %), уменьшение ФК ХСН по NYHA (47 и 30 %), улучшение показателей теста 6-минутной ходьбы и качества жизни по сравнению с пациентами, получавшими плацебо. Поскольку не у всех больных улучшение сопровождалось повышением уровня Hb, было высказано предположение, что эффект от ПЖ у пациентов ХСН не только связан с повышением показателей Hb, но и может быть обусловлен улучшением функции и работы мышц, в т. ч. сердечной. В пользу данного предположения свидетельствуют результаты экспериментальных исследований, в которых было показано, что у крыс, получавших ПЖ, улучшались показатели работы мышц [64, 65].
В исследовании И.Р. Ким и соавт. на фоне приема пероральных ПЖ в сочетании со стандартной терапией пациентов с сочетанием ХСН и ЖДА также была отмечена положительная динамика в виде не только увеличения концентрации Hb с 97,1 ± 3,7 до 106,7 ± 3,9 г/л, но и повышения толерантности к физической нагрузке (расстояние, пройденное за 6 минут, возросло с 284,8 ± 26,1 до 420,3 ± 31,4 метра) и улучшения клинического статуса пациентов. Были также отмечены изменения центральной гемодинамики в виде увеличения ФВ с 37,1 ± 3,6 до 49,04 ± 4,2 %, p < 0,05, и ударного объема от 43,7 ± 5,6 до 66,3 ± 6,2 мл [66].
В проведенном нами исследовании на фоне лечения коррекции анемии (ПЖ, витамин В12) у больных ХСН с выраженной анемией (Нb менее 70 г/л) в отличие от пациентов с исходно менее выраженной анемией было отмечено улучшение толерантности к нагрузке и сокращение доли больных с высоким ФК ХСН по NYHA, несмотря на уменьшение исходных показателей ФВ, ударного, конечного систолического объемов [43].
К проблеме ведения больных ХСН с наличием анемии, в частности тактики применения ПЖ, остается ряд вопросов [67], которые сводятся к следующему: • Необходимо ли всегда применять парентеральные ПЖ или такой же эффект оказывают ПЖ для приема внутрь? • Существует ли различие в ответе на терапию ПЖ у больных ЖДА и АХЗ? • Улучшается ли функция ЛЖ после лечения ПЖ? • Оказывают ли ПЖ многосторонний, не только “гематологический”, эффект на больных выраженной ХСН? • Необходимо ли более широко использовать ПЖ для внутривенного введения пациентам с наличием АХЗ? • Как долго можно применять парентеральные ПЖ пациентам с АХЗ и существуют ли опасения об отложении Fe в ткани печени или сердца при длительном введении ПЖ? Для ответов на эти вопросы необходимо проведение дальнейших исследований в этом направлении.
2.3. ПЖ при применении ЭПО больными ХСН с наличием анемии
Имеется ряд сообщений об успешном применении препаратов ЭПО пациентами с ХСН с наличием анемии. В рандомизированное плацебоконтролируемое исследование D. Mancini и соавт. [68], в котором 26 больных ХСН III–IV ФК по NYHA и Ht < 35 % наряду с ЭПО получали пероральный ПЖ (325 мг) и 1 мг/сут фолиевой кислоты, уровень Hb повысился с 110 ± 0,6 до 140 ± 1,2 г/л (р < 0,0001), а максимальное потребление кислорода возросло с 11 ± 0,8 до 12,7 ± 2,8 мл/мин/кг (р < 0,05).
В контрольной группе достоверных различий показателей не было. В другом исследовании [69] пациентов с ХСН и наличием анемии, получавших рекомбинантный человеческий ЭПО (50 МЕ/кг 2 раза в неделю внутривенно) в сочетании с парентеральным введением ПЖ, продемонстрировано не только достоверное увеличение уровня Hb, толерантности к физической нагрузке, по данным теста с 6-минутной ходьбой, и ФВ, но и достоверно лучшая выживаемость за 3-летний период наблюдения (16 из 29 человек по сравнению с 7 из 26, р < 0,05, ОР = 1,27).
Уменьшение ФК ХСН, снижение потребности во внутривенном введении диуретиков, уменьшение сроков госпитализации и стабилизации почечной функции в сочетании с достоверным увеличением ФВ на фоне терапии препаратами ЭПО в сочетании с парентеральным введением ПЖ были отмечены и в исследовании D. Silverberg и соавт. [70].
В большинстве исследований назначали ПЖ для внутривенного введения, которые, по мнению многих, имеют преимущество перед пероральными ПЖ. Однако эффективность ПЖ для приема внутрь во многом определяется биодоступностью конкретного препарата. Так, в одном из исследований не удалось отметить достоверных различий в динамике прироста уровня Hb у больных ЖДА, леченных препаратами солей Fe внутрь (Сорбифер Дурулес) или железосодержащими комплексами внутривенно (Феррум Лек) [71]. С учетом этих данных ПЖ для приема внутрь должны занять более широкое место в различных клинических ситуациях, требующих кор-рекции дефицита Fe, в т. ч. и в лечении ЭПО больных ХСН с наличием анемии.
2.4. ПЖ при анемии на фоне приема антиагрегантов
Проблема назначения ПЖ больным, получающим антиагреганты и антикоагулянты, имеет два клинических аспекта. С одной стороны, одним из осложнений антиагрегантной терапии больных ИБС являются кровотечения с развитием ЖДА, что требует своевременной диагностики и назначения ПЖ. Однако ПЖ получают только около половины (48,4 %) находящихся в стационаре больных ИБС с наличием ЖДА и значительно меньшее число (24 %) больных в отделении кардиореанимации. Что касается больных ЖДА легкой степени, то ПЖ получают лишь 6,5 % пациентов [12].
С другой стороны, имеющаяся анемия, особенно при значительном снижении показателей Hb (Ht), считается наряду с другими признаками (сахарным диабетом, сердечной недостаточностью, уровнем креатинина, величиной артериального давления и др.) одним из предикторов кровотечения при лечении антиагрегантами (шкала CRUSADE). Это, по понятным причинам, ограничивает врачей в использовании жизненно важных для больных ИБС антикоагулянтов и антиагрегантов.
Действительно, частота назначения антикоагулянтов пациентам с ОКС с и без подъема сегмента ST при наличии гипохромной анемии легкой степени составляет 97,1 и 93,1 %, в то время как при анемии средней тяжести и тяжелой ЖДА – 39,9 и 4,3 % соответственно [12].
Таким образом, наличие анемии у лиц с сердечно-сосудистой патологией представляет серьезную проблему как с точки зрения расшифровки патогенетической связи с основными заболеванием, так и при ведении данной категории пациентов. Независимо от того, является ли анемия истинной коморбидностью или оказывается патогенетически ассоциированной с кардиальной патологией, в каждой конкретной ситуации необходимы своевременная диагностика анемии, верификация патогенетического варианта и причины ее развития, адекватная коррекция с помощью антианемических, главным образом железосодержащих, препаратов.
Когда же нужно обратить внимание на свое здоровье?
Любой здоровый человек должен один раз в год проходить минимальное профилактическое обследование, в состав которого входит общий анализ в крови.
При уровне гемоглобина ниже 120 г/л нужно проконсультироваться с терапевтом.
Анемия с уровнем гемоглобина выше 100 г/л считается легкой и не представляет серьезной опасности для организма на момент выявления, однако все равно требует коррекции. При уровне гемоглобина 70-80 г/л и ниже необходимо экстренно принимать меры, т.к. такое состояние несет серьезные угрозы здоровью, а иногда и жизни!
По причинам развития анемий лидирующие позиции занимает железодефицитная анемия – каждый 12-й человек в мире страдает железодефицитной анемией, а среди всех анемий железодефицитные по частоте достигают 80%.
С чем связано развитие железодефицитной анемии? Причинами может стать элементарная недостаточность железа в пище, нарушение всасывания железа в желудочно-кишечном тракте (например, при гастритах с пониженной кислотностью) и хронические кровотечения.