Когда своему здоровью стоит уделять должное внимание?
Каждый без исключения обязан хотя бы раз в год записываться на прием к врачу для прохождения медицинского обследования, включающего общий анализ в крови.
По причинам развития анемий передовые строчки занимает как раз железодефицитная анемия – примерно 12% всего населения нашей планеты страдает от рассматриваемого явления.
Чем объясняется распространение железодефицитной анемии? Основанием может стать обычный дефицит железа в еде, нарушение проникновения железа в ЖКТ и кровотечения хронической формы.
Наиболее частыми причинами кровотечений являются:
- Геморрой хронической формы.
- Геморроидальный тромбоз.
- Сбой менструального цикла у представительниц женского пола, который находит свое отражение в интенсивных и продолжительных менструациях.
Тем не менее, железодефицитная анемия может являться одним из первичных показателей процессов развития новообразований. Приведем пример: рак толстой кишки – зоны распады новообразования выделяют кровь в просвет кишки, а сам человек этого попросту не может заметить!
лечится ли анемия
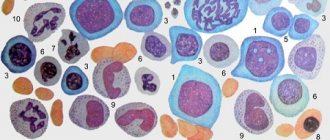
Симптомы анемии
Недостаток гемоглобина приводит к кислородному голоданию, проявляющегося такими типичными для анемии симптомами как:
Общая слабость
При анемии мышечная ткань не получает достаточного питания. Больной чувствует себя постоянно уставшим, у него не хватает сил на обычную жизнедеятельность.
Сонливость
Организму не достаёт сил, а значит ему требуется дополнительный отдых. Развивается сонливость. Человек, страдающий анемией практически никогда не бывает бодр; как правило, ему хочется спать.
Бледность
Бледность кожи при анемии вызвана снижением количества эритроцитов (красных кровяных телец) в крови.
Головокружения
При анемии головной мозг также получает недостаточное питание. Это может стать причиной головокружений.
Мелькание
Мелькание «мушек» перед глазами вызвано недостаточным питанием структур зрительного аппарата.
Обмороки
Если снижение гемоглобина значительно, возможны обмороки – эпизоды потери сознания.
Головная боль
При анемиях часто наблюдаются головные боли.
Подробнее о симптоме
Учащенное сердцебиение
Может наблюдаться сильное сердцебиение при незначительной физической нагрузке или в состоянии покоя.
Подробнее о симптоме
Одышка
Одышка при анемии вызвана тем, что организм пытается восполнить недостаток кислорода, увеличив его поступление. Дыхание становится более частым.
Подробнее о симптоме
Чем грозит исследуемая анемия?
Следует понимать, что даже легкая анемия способна значительно навредить организму человека. Продолжительная нехватка кислорода вызывает нарушение метаболизма, скопление вредоносных веществ в организме, чрезмерной нагрузке на внутренние органы. Многие люди, к сожалению, сегодня даже не знают, лечится ли анемия.
Для того, чтобы предотвратить развитие многочисленных хронических болезней, необходимо следовать элементарным указаниям:
Проходить регулярное медицинское обследование – здоровый человек в этом случае, как правило, сдает общий анализ крови и мочи, делает флюорографию, записывается на прием к терапевту, гинекологу и стоматологу.
В случае обнаружения признаков хронических недугов, которые в последующем могут привести к малокровию, необходимо незамедлительно обращаться к врачу за соответствующим лечением.
можно ли вылечить анемию
В большинстве своем это относится к представительницам слабого пола с проблемами в области гинекологии. Часто женщины просто не обращают внимания на обильные и болезненные менструации и считают, что это в порядке вещей! Стоит отметить, что это ошибочное мнение, так как после терапии возможен вариант восстановления нормального течения менструального цикла. Кроме этого, продолжительные и интенсивные менструации у женщин после 40 лет могут являться первичной симптоматикой раковых заболеваний! Поэтому не забывайте задавать вопрос самой себе: можно ли вылечить анемию и как это правильно сделать.
Современные подходы к лечению железодефицитной анемии у больных с гинекологической патологией
Анемия — патологическое состояние, характеризующееся уменьшением концентрации гемоглобина и нередко сопровождающееся снижением числа эритроцитов в единице объема крови [1]. Согласно данным Минздрава РФ за последние 10 лет частота анемий увеличилась в 6,3 раза, причем наиболее распространенной является железодефицитная анемия (ЖДА) (около 90% всех анемий). ЖДА — это гипохромная микроцитарная анемия, возникающая вследствие снижения содержания железа в организме и представляющая собой самостоятельную нозологическую форму [2].
В клинической практике наиболее распространена следующая классификация анемий:
1) анемия, обусловленная острой кровопотерей (постгеморрагические); 2) анемия вследствие нарушения продукции эритроцитов (апластические, железодефицитные, мегалобластные, сидеробластные и др.); 3) анемия вследствие повышенного разрушения эритроцитов (гемолитические).
В зависимости от выраженности снижения уровня гемоглобина выделяют три степени тяжести анемии:
- легкая — уровень гемоглобина выше 90 г/л;
- средняя — гемоглобин в пределах 90–70 г/л;
- тяжелая — уровень гемоглобина менее 70 г/л.
Распространенность у женщин детородного возраста железодефицитных состояний (ЖДС) в некоторых регионах Российской Федерации достигает 30–60%, а согласно данным Всемирной организации здравоохранения в мире общее число лиц с дефицитом железа составляет около 600 млн человек [3]. ЖДС выступают причиной увеличения восприимчивости к острым респираторным вирусным инфекциям и снижения работоспособности.
В гинекологии различают три стадии ЖДС в организме:
- Прелатентный дефицит железа — скрытый дефицит железа, организм аккумулирует железо при помощи ферритина — железосодержащего белка. Если его показатель низкий, то говорят о наличии прелатентного дефицита железа.
- Латентный дефицит железа — на данной стадии, наряду с ферритином, истощаются тканевые запасы железа при оптимальных показателях гемоглобина, не наблюдается клинических симптомов дефицита железа, в кишечнике происходит компенсаторное повышение всасывания железа, активность железосодержащих ферментов постепенно снижается.
- Явный дефицит железа характеризуется уменьшением числа эритроцитов и снижением уровня гемоглобина, который входит в состав эритроцитов и представляет собой вещество, транспортирующее кислород к тканям организма из легких, развитием дистрофических изменений в органах и тканях, а также повышенным количеством протопорфирина в эритроцитах [2, 4].
Высокая распространенность анемий среди женщин связана с тем, что женский организм испытывает всегда недостаток железа из-за регулярных кровопотерь. Человеческий организм устроен так, что может восстановить из пищи лишь 2 мг этого минерала в сутки, при условии полноценного питания (употребления в пищу достаточного количества овощей и мяса) [2]. Таким образом, менструальные кровопотери, несмотря на свою «объективность», могут послужить причиной развития дефицита железа в организме женщины. Во время менструаций нормальная кровопотеря составляет 30–50 мл, организм при этом теряет от 15 мг железа [4, 5]. А в случае если менструации обильные и длятся свыше 7 дней, то потери железа составляют более 50 мг. Как следствие, в таких случаях потребность в железе возрастает во много раз [6].
Дефицит железа наблюдается чаще у женщин в возрасте 30–40 лет. Как правило, это происходит в процессе беременности и кормления грудью (как плод, так и грудной ребенок непосредственно получают железо от матери). Также нельзя забывать о потере крови в течение родов. Женщины могут не подозревать о наличии у себя подобной проблемы, хотя регулярно сдают анализ крови во время беременности. Недостаток железа в организме диагностируется, к сожалению, лишь на третьей стадии. Большинство женщин достаточно быстро утомляются и чувствуют разбитыми себя уже при незначительном снижении уровня ферритина. В организме при недостатке железа возникает головокружение и головные боли.
Для того чтобы пополнить запасы железа и при нормальном эритропоэзе восстановить кровопотерю, достаточно содержащегося в пище железа. При заместительной гормональной терапии стимулирующими эритропоэз препаратами адекватное поступление в организм железа оптимизирует назначенное лечение. Следует отметить, что во многих случаях внутривенный путь введения железа более эффективен, чем пероральный, так как обеспечивает возможность быстрого насыщения организма необходимым ему железом [7]. Это особенно важно при лечении анемии, протекающей на фоне хронических заболеваний. Внутривенный путь введения железа помогает преодолеть блокировку всасывания железа из желудочно-кишечного тракта (ЖКТ) и создать его запас в организме.
ЖДА в настоящее время является социальным заболеванием с достаточно широкой распространенностью. У беременных женщин представляет собой состояние, обусловленное сокращением содержания железа в костном мозге и сыворотке крови в связи с его большими затратами на формирование фетоплацентарного комплекса, а также перераспределением в пользу плода. Естественным следствием дефицита железа выступает нарушение образования гемоглобина с развитием как гипохромной анемии, так и трофических расстройств тканей.
ЖДА остается серьезной патологией в современной гинекологии, так как частота данного заболевания не снижается. У беременных частота анемии варьирует в пределах 15–80%, а у 98% женщин анемия во время беременности носит выраженный железодефицитный характер [2, 8].
Сбалансировать в женском организме содержание железа способны только железосодержащие препараты.
Нехватка ферментов, содержащих в своем составе железо, может в организме беременной женщины вызвать разнообразные трофические изменения. Наряду с этими изменениями наблюдается появление трещин в уголках рта, желтизна ладоней, ногти становятся хрупкими, выпадают волосы и др. Это заболевание иногда проявляется «экзотическими» гастрономическими пристрастиями. В тяжелой форме развития дефицита железа может наблюдаться понижение или повышение артериального давления, отечность, сердцебиение, а также сердечная недостаточность. Повышается объем циркулирующей крови, возрастает потребность в кислороде, и, как следствие, дефицит железа осложняет ход беременности и родов, что в свою очередь крайне негативно влияет на развитие плода.
К основным факторам риска возникновения и развития у беременных ЖДА относят наличие до беременности хронических заболеваний или анемии, хронические заболевания внутренних органов или инфекционные болезни, многоплодие, ранний токсикоз, уровень гемоглобина меньше 120 г/л в I триместре, длительность менструаций в течение нескольких лет до беременности более 5 дней [9].
Ежесуточно женщина потребляет с пищей от 10 до 20 мг железа, из которых полностью усваивается менее 2 мг, а за время менструации до 75% здоровых женщин теряют от 20 до 30 мг железа [10, 11]. Данное количество железа не может усвоиться даже при его большом содержании в пище. Таким образом, возникает дисбаланс, приводящий к развитию анемии.
При беременности, родах и кормлении грудью совокупная потеря железа составляет приблизительно 1 г, и для того чтобы пополнить запас железа исключительно из пищевых источников, женскому организму требуется примерно 4 года. Следовательно, если женщина рожает ребенка повторно в этот срок, у нее неизбежно развивается дефицит железа [5].
Современные клинические рекомендации включают в себя необходимость приема железосодержащих препаратов всем беременным во II и III триместрах гестации. Для взрослых небеременных женщин суточная доза (18 мг железа) в наиболее редких случаях покрывается исключительно за счет питания [4, 9]. Именно поэтому к началу беременности практически у половины всех женщин резервы железа минимальны.
Согласно современным данным, в конце гестационного процесса дефицит железа развивается без исключения у всех беременных как в скрытой, так и в явной форме. Главным образом это связано с тем, что беременность всегда сопровождается дополнительными потерями железа: 320–500 мг железа расходуется на возросший клеточный метаболизм и прирост гемоглобина, 50 мг железа — на увеличение размеров матки, 100 мг железа — на построение плаценты, 400–500 мг железа — на потребности плода [6].
В итоге плод с учетом запасного фонда обеспечивается в достаточном количестве железом, но у беременных при этом часто развиваются ЖДС различной степени тяжести. Для оценки соответствия запаса железа норме определяется уровень ферритина сыворотки крови, который при своих значениях менее 30 мкг/л считается сниженным.
Сниженная дородовая концентрация гемоглобина (особенно дефицит железа) выступает фактором риска послеродовых кровотечений, коррелируя с тяжестью состояния женщины на ее фоне. Применяя в дородовый период препараты внутривенного железа для коррекции ЖДА, врачи стремятся минимизировать как риск развития кровотечений, так и потребность переливания препаратов крови в перинатальный период. В постнатальный период (от 0 до 6 месяцев) дефицит железа отмечается у 13% матерей, а у 10% женщин диагностируют анемию. Пероральные формы препаратов железа при этом достаточно медленно действуют и часто не дают необходимого эффекта [2, 11].
Внутривенное железо, бесспорно, выступает безопасной альтернативой, снижая как необходимость переливаний крови, так и их объем. Лечение с помощью внутривенных препаратов железа позволяет достичь существенного увеличения запасов железа и значительно повысить концентрацию гемоглобина в крови.
За исключением тяжелых случаев, ЖДА лечится во время беременности амбулаторно. Врачи для ее лечения назначают прием лекарственных средств с содержанием данного элемента. Как правило, их употребляют длительное время (от 15 недель до 6 месяцев). Уровень гемоглобина в крови поднимается плавно, не ранее третьей недели от начала лечения. Показатель приходит в норму примерно через 2 месяца от начала терапии [9, 11]. Одновременно улучшается состояние здоровья и самочувствие женщины. Однако важно не прерывать курс лечения, так как при увеличении срока беременности плод также растет и его потребности в железе, соответственно, тоже повышаются.
Не стоит забывать и о предстоящих женщине родах, которые, в свою очередь, влекут значительную растрату сил и кровопотерю. Далее наступает период грудного кормления ребенка, вызывающий также нехватку железа. Поэтому специалисты рекомендуют в послеродовой период продолжать поддерживающее лечение с помощью препаратов железа еще 6 месяцев [11, 12]. Для того чтобы определить недостаток железа в женском организме вовремя, симптомы следует рассматривать как в комплексе, так и по отдельности.
Современные исследования показали высокую потребность в переливании компонентов крови пациенткам с тяжелыми маточными кровотечениями, что повышает стоимость госпитализации и снижает в целом качество жизни. Пероральный прием железосодержащих препаратов в целях устранения ЖДС у женщин с меноррагиями позволяет избежать трансфузий эритромассы во всех известных случаях, кроме выраженного падения уровня гемоглобина, когда пероральные формы не могут полностью компенсировать потери железа [12].
На сегодняшний день в России, к сожалению, широкое распространение получили лекарства, содержащие большое количество железа при расчете на одну таблетку. Токсические эффекты терапии, проявляющиеся при этом, считались неизбежными, и с целью их предотвращения, как правило, рекомендовался прием лекарственного средства во время еды для связки свободных ионов железа и предотвращения тем самым их отрицательного влияния на ЖКТ. Парадокс очевиден: рекомендовались значительные дозы железа, связывание железа белками пищи одновременно с этим снижало во много раз его поступление. Терапевтический эффект в результате не зависел никаким образом от высокой дозы железа в лекарстве [5, 6].
При выборе содержащего железо препарата необходимо учитывать ряд факторов. Так как ионизированное железо из ЖКТ всасывается исключительно в двухвалентной форме и огромную роль в данном процессе играет аскорбиновая кислота, то крайне важно наличие ее в препарате. В гемопоэзе большое значение принадлежит фолиевой кислоте, которая усиливает нуклеиновый обмен. Также для нормального обмена фолиевой кислоты важен цианокобаламин, выступающий ключевым фактором при формировании из нее активной формы.
Дефицит данных веществ, возникающий достаточно часто при связанных с кровопотерями анемиях, приводит к нарушениям синтеза ДНК в кроветворных клетках, в то время как включение данных компонентов в лекарственное средство повышает активную абсорбцию в кишечнике железа и его дальнейшую утилизацию, освобождает дополнительное число ферритина и трансферрина [13]. Как следствие, скорость синтеза гемоглобина увеличивается, а эффективность терапии как ЖДА, так и других ЖДС повышается.
Единственным препаратом железа для внутривенного введения в СССР был Феррум Лек. В России для внутривенного восполнения дефицита железа разрешены следующие препараты: Венофер, КосмоФер и Ликферр (из них отечественный Венофер). Во многих странах используются препараты нового поколения с усовершенствованными характеристиками — Феринжект (железа карбоксимальтозат), Ферумокситол (наночастицы оксида супермагнитного железа) и Монофер (железа (III) гидроксид олигоизомальтозат 1000) [5, 13, 14].
Датская фармацевтическая компания, являющаяся мировым экспертом в разработке железосодержащих препаратов, создала новый высокоэффективный препарат железа для внутривенного использования, с минимальными ограничениями при назначении. Организация работает над клиническими программами с целью дальнейшего подтверждения безопасности, эффективности и удобства применения Монофера как современного средства лечения ЖДА.
Препарат Монофер (железа (III) гидроксид олигоизомальтозат 1000) был создан на базе технологии матричной структуры с чередующимися фрагментами олигоизомальтозата 1000 и железа (III) гидроксида, за счет чего обеспечивается низкая токсичность препарата [14, 15]. Благодаря низкой токсичности Монофер может быть назначен в высокой дозе, создавая возможность коррекции ЖДС всего за один визит.
К основным факторам безопасности Монофера можно отнести: отсутствие тест-дозы, низкий риск анафилактических реакций, минимальный риск токсичности, обусловленный наличием в составе препарата свободного железа. Удобство применения Монофера основано на возможности высокой (до 20 мг/кг) и быстрой (до 60 мин) скорости инфузии за счет низкой токсичности препарата [15].
Матричная структура препарата включает прочно связанное и стабильное железо, способствуя медленному и контролируемому высвобождению железосодержащих белков биоактивного железа с минимальным риском токсичности из-за присутствия свободного железа (рис.) [10].
Препараты железа нового поколения имеют в своем составе меньшее содержание свободного железа, в отличие от старых препаратов железа. Монофер предоставляет для каждого пациента с ЖДА удобную дозировочную линейку в виде:
- внутривенной капельной инфузии: 200–1000 мг (назначается 1 раз в неделю до полного достижения восстановления дефицита железа):
а) 11–20 мг/кг — 60 минут (необходимо добавить от 100 до 500 мл стерильного раствора NaCl 0,9%); б) 6–10 мг/кг — 30 минут; в) 0–5 мг/кг — 15 минут;
- внутривенной болюсной инъекции: 100–200 мг в неделю до 3 раз (скорость — 50 мг/мин). Может быть также растворен в 10–20 мл стерильного раствора 0,9% NaCl [12].
Если необходимость пациента в восполнении железа превышает показатель 20 мг/кг, доза Монофера должна быть обязательно разделена и назначена с временным интервалом, как минимум, в одну неделю. Инфузии препарата более 1000 мг назначаются исключительно в госпитальных условиях. Препарат должен назначаться больным с диагнозом ЖДА, подтвержденным соответствующими лабораторными данными (результаты определения концентрации гематокрита и гемоглобина, ферритина сыворотки, количества эритроцитов и их параметров — среднего содержания в эритроците гемоглобина, среднего объема эритроцита или средней концентрации в эритроците гемоглобина).
Следует отметить, что в одном шприце Монофер можно смешивать исключительно со стерильным физиологическим раствором. Другие терапевтические препараты и растворы для введения добавлять запрещено, так как существует риск не только преципитации, но и другого фармацевтического взаимодействия.
Важно избегать проникновения препарата в околовенозное пространство, поскольку его попадание за границы сосуда приводит к коричневому окрашиванию кожи и некрозу тканей. В случае развития подобных осложнений для ускорения вывода железа и предотвращения его более глубокого проникновения в близлежащие ткани рекомендуется нанести гепаринсодержащий препарат на место инъекции (мазь или гель наносят не втирая, легкими движениями) [16].
Противопоказания к применению препарата:
- не связанная с дефицитом железа анемия (например, гемолитическая анемия);
- высокая чувствительность к активному веществу и входящим в состав препарата вспомогательным веществам;
- наличие различных признаков перегрузки железом (гемосидероз, гемохроматоз) или нарушение процессов утилизации железа;
- ревматоидный артрит в сочетании с симптомами активности воспалительных процессов;
- цирроз и гепатит печени (стадия декомпенсации);
- бактериемия;
- детский возраст менее 18 лет (по причине недостаточности доказанных данных о безопасности и эффективности) [3].
Препараты железа, вводимые парентерально, могут вызвать реакции повышенной чувствительности, в частности анафилактический шок, в связи с риском развития аллергических реакций у больных экземой, поливалентной аллергией, бронхиальной астмой, аллергическими реакциями на другие парентеральные препараты железа, с системной красной волчанкой, острыми и хроническими инфекционными заболеваниями, ревматоидным артритом и др. применение препарата ограничено. Также возможны эпизоды внезапного значительного снижения артериального давления при высокой скорости введения Монофера.
Таким образом, применение препарата рекомендовано в клинически оправданных случаях. Важно тщательно оценить отношение польза/риск для решения вопроса о использовании Монофера при беременности. Если для матери предполагаемая польза превышает риск для плода, то лечение можно проводить во II и III триместрах беременности. Не рекомендуется применение препарата в I триместре беременности [3, 17].
Выделение Монофера с грудным молоком на сегодняшний день не установлено. Следовательно, препарат в период лактации можно применять.
Монофер не должен одновременно назначаться с различными лекарственными формами железа для приема внутрь, так как их совместное употребление способствует сокращению всасывания железа из ЖКТ. Лечение пероральными препаратами железа начинают не ранее чем спустя 5 дней после последней инъекции. Препарат отличается хорошей переносимостью и обладает низкой токсичностью. В связи с этим риск передозировки минимален. Однако передозировка может развиваться из-за острой перегрузки железом или кумуляции железа и выражается симптоматикой гемосидероза. Контроль содержания в организме железа проводят, определяя степень концентрации ферритина.
Полученные результаты исследований показали, что профилактика анемии у женщин препаратом Монофер способствует сокращению частоты развития различных заболеваний, ассоциированных с дефицитом железа [18]. Кроме того, на фоне отсутствия ЖДА исчезает циркуляторная и гемическая гипоксия, что, в свою очередь, предупреждает развитие метаболических расстройств и приводит к уменьшению частоты осложнений, таких как фетоплацентарная недостаточность, гестоз, преждевременные роды и аномалии родовой деятельности. Отсутствие у препарата тяжелых побочных эффектов и удобный режим дозирования указывают на хорошую переносимость Монофера.
Таким образом, среди основных преимуществ Монофера в гинекологии можно выделить следующие: широкий спектр показаний для назначения, удобное дозирование и высокий профиль безопасности. Применение Монофера обеспечивает высокую эффективность как профилактики, так и лечения ЖДА.
На сегодняшний день существует большая доказательная база различных клинических исследований, подтверждающих эффективность и безопасность внутривенного введения железа при разнообразии клинических ситуаций, связанных с различными ЖДС. Анализ исследований, позволяющих сравнить результаты пероральной и внутривенной форм приема железа, свидетельствует о равной или более высокой эффективности последней формы. Также в современных исследованиях подчеркиваются такие недостатки пероральной формы введения железосодержащих препаратов, как побочные эффекты, несоблюдение предписаний врача, низкий уровень всасывания, а также и невозможность оперативного возмещения потери железа и поддержания его адекватной концентрации, характерных для пациенток с продолжающейся кровопотерей.
Внедрение в клиническую практику гидроксида изомальтозата 1000, не требующего тестовой дозы, с возможностью парентерального введения за короткое время высоких доз, несет в себе дополнительные преимущества в терапии препаратами, вводимыми внутривенно железа. Также, в отличие от пероральной формы, именно внутривенный путь введения препаратов железа позволяет преодолеть анемию, развивающуюся на фоне хронических заболеваний.
Литература
- Куликов А. Ю., Скрипник А. Р. Фармакоэкономический анализ лекарственного препарата «Монофер» в лечении железодефицитной анемии // Фармакоэкономика: теория и практика. 2021, 4: 183–186.
- Лебедев В. А., Пашков В. М. Принципы терапии железодефицитной анемии у гинекологических больных // Трудный пациент. 2013, 11: 3–7.
- Nordfjeld K., Andreasen H. Pharmacokinetics of iron isomaltoside 1000 in patients with inflammatory bowel disease // Drug. Des. Devel. Therapy. 2012, 6: 43–51.
- Малкоч А. В., Анастасевич Л. А., Филатова Н. Н. Железодефицитные состояния и железодефицитная анемия у женщин детородного возраста // Лечащий Врач. 2013; 4: 37–41.
- Мубаракшина О. А., Сомова М. Н., Любавская С. С. Фармакологическая коррекция дефицита железа и магния в период беременности. Воронежская государственная медицинская академия им. Н. Н. Бурденко. 2014; 4: 52–60.
- Подзолкова Н. М., Нестерова А. А. Железодефицитная анемия беременных // Русcкий медицинский журнал. 2003, 5: 326–331.
- Morrison J., Patel S. T., Watson W. Assessment of the prevalence and impact of anemia on women hospitalized for gynecologic conditions associated with heavy uterine bleeding // J. Reprod. Med. 2008, 5: 323–330.
- Протопопова Т. А. Железодефицитная анемия и беременность // Русский медицинский журнал. 2012; 17: 862–867.
- Чушков Ю. В. Современные возможности коррекции дефицита железа в акушерстве и гинекологии // Гинекология. 2011; 6: 44–47.
- Bhandari S. A hospital-based cost minimization study of the potential financial impact on the UK health care system of introduction of iron isomaltoside 1000 // Clin Risk Manag. 2011, 7: 103–113.
- Дворецкий Л. И. Алгоритмы диагностики и лечения анемий // Русcкий медицинский журнал. 2003, 8: 427–433.
- Coyne D. From anemia trials to clinical practice: understanding the risks and benefits when setting goals for therapy // Semin Dial. 2008, 21: 212–216.
- Лебедев В. А., Пашков В. М. Принципы терапии железодефицитной анемии у гинекологических больных // Трудный пациент. 2013, 11: 3–7.
- Gupta D. R., Larson D. S., Thomsen L. L. Pharmacokinetics of Iron Isomaltoside1000 in Patients with Stage 5 Chronic Kidney Disease on Dialysis Therapy. 2013, 03: 4172/2157–7609.
- Hildebrant P., Brunn N. et al. Effects of administration of iron isomaltoside 1000 in patients with chronic heart failure. A pilot study. Transfusion Alternatives in Transfusion Medicine // 2010, 11: 131–137.
- Locatelli F. Iron treatment and the TREAT trial // NDT +. 2011, 4: 13–15.
- Pasricha S. R., Flecknoe-Brown S. C. Diagnosis and management of iron deficiency anaemia: a clinical update. 2010, 9: 50–62.
- Philip A. Kalra, Sunil Bhandari, Sanjiv Saxena. A randomized trial of iron isomaltoside 1000 versus oral iron in non-dialysis-dependent chronic kidney disease patients with anaemia // Nephrol Dial Transplant. 2015, 3: 1–10.
А. З. Хашукоева*, 1, доктор медицинских наук, профессор М. И. Агаева* М. З. Дугиева*, доктор медицинских наук Т. Н. Сухова** Л. И. Абдурахманова*
* ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва ** ОСП РГНКЦ ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
1 Контактная информация
Современные подходы к лечению железодефицитной анемии у больных с гинекологической патологией/ А. З. Хашукоева, М. И. Агаева, М. З. Дугиева, Т. Н. Сухова, Л. И. Абдурахманова
Для цитирования: Лечащий врач №12/2017; Номера страниц в выпуске: 23-29
Теги: женщины, железо, внутривенные препараты
Профилактика анемии
Основными мерами профилактики заболевания являются:
- правильное питание – отказ от фастфуда и другой вредной пищи, введение в рацион продуктов, богатых железом, витаминами (особенно группы В);
- отказ от вредных привычек;
- своевременное лечение заболеваний, которые могут привести к возникновению анемии;
- нормализация режима труда и отдыха;
- регулярное проведение санации очагов хронической инфекции в организме;
- избегание переизбытка витамина С в организме;
- профилактика гельминтозов, а если они возникли, то своевременное лечение;
- отказ от малоподвижного образа жизни – занятия физкультурой, регулярные прогулки на свежем воздухе;
- избегание стрессов и других психоэмоциональных нарушений;
- использование средств индивидуальной защиты при работе на вредном производстве;
- дополнительный прием препаратов железа во время обильных месячных, при хронических или острых кровотечениях;
- отказ от бесконтрольного приема лекарственных средств, все препараты должен назначать только лечащий, врач, самолечение недопустимо;
- своевременное обращение к врачу при появлении первых подозрительных симптомов – это позволит диагностировать анемию на ранней стадии, что существенно облегчит последующее лечение и улучшит прогноз заболевания.
Как диагностировать АХЗ?
● Гемоглобин снижен.
● Размер эритроцитов (MCV) в норме, реже снижен (в отличие от железодефицитной анемии).
● Содержание гемоглобина в эритроцитах (MCH) в норме, реже ниже нормы. *Таким образом, чаще всего анемия хронических заболеваний — это нормоцитарная нормохромная анемия.
● Важным признаком, отличающим железодефицитную анемию от АХЗ, является снижение ферритина. При АХЗ уровень ферритина остается нормальным или повышается как острофазовый белок воспаления/инфекции или онкомаркер при онкозаболеваниях.
● При постановке диагноза АХЗ надо ответить на вопрос: «Дефицит железа является абсолютным (истинным) или функциональным (перераспределительным)?». Тактика лечения будет разной: в первом случае назначение препаратов железа приведет к быстрой компенсации дефицита и выздоровлению, во втором — их прием будет бесполезным.
Домашний рецепт от анемии
Рецепт домашнего смузи из сырой свеклы.
Для его приготовления потребуются следующие продукты:
- Свекла, как источник фолиевой кислоты, калия, натрия. Свекла прекрасно чистит кишечник, удаляя из него гнилостные бактерии. Особенно полезна свекла в сыром виде, так как содержит большое количество клетчатки.
- Чищеный апельсин.
- Четыре финика.
- Черная смородина – 70 г.
- Миндаль чищеный.
Свеклу мелко режут, складывают в блендер, туда же добавляют орехи и финики, ягоды и апельсин без косточек. Все заливают 0,5 стакана воды и перемалывают в блендере. Смузи для подъема гемоглобина готов.
Видео рецепт свекольно-ягодного смузи:
Свежевыжатые соки в лечении анемии
Данный народный метод лечения анемии был проверен многими людьми. Одна из читательниц, лежала в больнице, а после того как выписалась, долго не могла прийти в себя. Прочитала, что можно пить витаминный коктейль. Стала его делать и пить. В организме нормализуется уровень гемоглобина в крови, улучшается общее состояние организма. Потом она общалась с другими людьми, которые также подтвердили, что этот рецепт работает и, самое главное, не приносит абсолютно никакого вреда больному человеку. Только пользу.
Свежевыжатые соки могут хорошо помочь в борьбе с анемией. С этой целью можно использовать витаминный коктейль, в состав которого входит сок граната, лимона, яблока и моркови. Обязательно в напиток нужно добавить мед.
Пропорции должны быть следующими:
- Гранатовый сок – 0,2 л.
- Яблочный сок – 0,1 л.
- Морковный сок – 0,1 л.
- Лимонный сок – 0,1 л.
- Мед – 70 г.
Употреблять сок лучше начать с 2 столовых ложек, чтобы проверить реакцию организма. Если организм отзывается хорошо, то увеличивайте дозировку вплоть до полного стакана 1-3 раза в день.
Использовать для приготовления коктейля фабричные соки нельзя. Они обязательно должны быть свежего отжима. Когда все компоненты напитка будут готовы, их потребуется просто смешать.
Полезная информация: если какой-либо ингредиент вам не подходит, то вы можете его исключить или заменить на любой другой овощ или фрукт. Только помните, что фруктовых соков много пить нельзя из-за высокого содержания сахара!
Видео рецепт:
Другие народные средства
Для лечения анемии можно воспользоваться следующими рецептами:
- Отварная или квашеная свекла. Ее едят в чистом виде и добавляют в разные блюда. Также можно выжать из овоща сок, настоять на протяжении 3-4 часов и пить по 1/4 или 1/3 стакана 3-4 раз в день. Курс лечения составляет 3-4 недели. Сок нельзя хранить, его готовят каждый день.
- 100 г сырой измельченной моркови с добавлением масла или сметаны также можно употреблять в пищу для лечения анемии.
- Можно залить столовую ложку измельченных цветков топинамбура тремя стаканами кипятка. Накрывают кастрюлю полотенцем и настаивают на протяжении 8 часов, после чего процеживают и употребляют по 1/2 стакана 3-4 раза в день за 15 минут до еды.
- Каждый день нужно есть чеснок, что позволяет избавиться от анемии.
- Каждый день полезно употреблять в пищу свежие огурцы, не очищая их от кожуры. Также хорошо выпивать по стакану огуречного сока в день.
- Тыква полезна для лечения анемии. Ее употребляют 4-5 раз в день по 150-200 г. Кушать мякоть тыквы можно в сыром и отварном виде.
- От анемии можно избавиться с помощью молока и укропа. Заливают зелень или семена растения стаканом молока и доводят до кипения. Затем огонь убавляют и кипятят еще 10 минут. Принимают по 1/3 стакана 3 раза в день.
- Полезно при анемии каждый день употреблять в пищу зелень и корень сельдерея. Также за 20 минут до еды хорошо принимать по 1-2 чайной ложки сельдереевого сока свежего отжима.
- От анемии отлично помогает шпинат, который добавляют в салаты. Хранить готовый салат с этим растением нельзя, так как в нем образуются ядовитые вещества. Однако цельные листья разрешается на протяжении 30 дней держать в холодильнике.
- Кабачки позволяют избежать развития анемии. Их едят в свежем виде, не очищая от кожуры.
Более 100 рецептов народной медицины вы можете узнать из видео ниже:
Как лечить анемию хронических заболеваний?
1. Лечение основного заболевания.
Выше разобран патогенез анемии — для понимания того, что при АХЗ в первую очередь надо лечить основное заболевание. Снижая активность воспалительного процесса в организме, мы даем возможность железу при его дефиците всасываться из ЖКТ. Бывают ситуации, когда это невозможно. Единственное утешение — АХЗ развивается медленно и чаще имеет легкую степень тяжести.
2. Переливание эритроцитарной массы и эритропоэзстимулирующие препараты, с или без сочетания с внутривенными препаратами железа — при тяжелом течении анемии.
В любом случае лечением АХЗ должны заниматься грамотные специалисты, самодиагностики и самолечения здесь быть не должно.