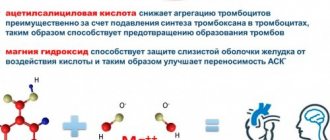
На сегодняшний день фармацевтические компании разработали множество гипотензивных средств, которые помогают значительно улучшить качество и продолжительность жизни гипертоника. Популярными медикаментами из группы ингибиторов АПФ являются препараты, в основу которых входит активное вещество эналаприл. Лекарства выпускаются под различными торговыми названиями, и имеют дорогие, так и более доступные аналоги. Среди них наибольшую популярность среди пациентов приобрели Энап и Эналаприл. Оба лекарства обладают схожими фармакологическими свойствами, и практически не отличаются по химическому составу. Однако, что лучше Энап или Эналаприл в борьбе с проявлениями артериальной гипертензии?
Сравнение эффективности Энапа и Эналаприла
Эффективность у Энапа достотаточно схожа с Эналаприлом – это означает, что способность лекарственного вещества оказывать максимально возможное действие схоже.
Например, если терапевтический эффект у Энапа более выраженный, то при применении Эналаприла даже в больших дозах не получится добиться данного эффекта.
Также скорость терапии – показатель быстроты терапевтического действия у Энапа и Эналаприла примерно одинаковы. А биодоступность, то есть количество лекарственного вещества, доходящее до места его действия в организме, схожа. Чем выше биодоступность, тем меньше его потерь будет при усвоении и использовании организмом.
Эффективность и переносимость эналаприла и индапамида при коррекции артериальной гипертензии
А
ртериальная гипиертензия (АГ) – неинфекционная пандемия, определяющая структуру инвалидизации и летальности при сердечно–сосудистых заболеваниях в социально–значимой группе населения. Развитие первичной АГ детерминировано множеством взаимодействующих факторов: от генетической предрасположенности до социальных условий окружающей среды. АГ, начинающаяся как функциональное расстройство, в большинстве случаев, последовательно, через различные патофизиологические механизмы приводит к специфическим поражениям органов – «мишеней» (ЦНС, сердце, почки), трансформируясь из фактора риска в заболевание.
По данным различных авторов, АГ в 80% и более случаев сочетается с различными видами метаболических нарушений, вошедших в мировую клиническую практику под термином «метаболический синдром», включающий дислипидемию, нарушение углеводного обмена и инсулинорезистентность (ИР), абдоминальное ожирение [1,3,5,15].
С позиций современного представления о механизмах формирования высоких цифр АД назначаемые антигипертензивные препараты должны обладать следующими свойствами:
1. Эффективно снижать АД (достижение целевого уровня АД);
2. Предупреждать (уменьшать) поражение органов «мишеней»;
3. Не вызывать метаболические нарушения;
4. Быть безопасными в применении и не оказывать побочных эффектов;
5. Обладать пролонгированным гипотензивным действием (уменьшение кратности приема) [9].
Согласно современным рекомендациям ВОЗ (1999) на первом этапе лечения АГ рекомендовано применение диуретиков, b-блокаторов и ингибиторов ангиотензин–превращающих ферментов
(иАПФ) с метаболически – нейтральными свойствами [4,9,10].
Тиазидные и тиазидоподобные диуретики можно условно разделить на два поколения: первое поколение – производные бензотиадиазина (гидрохлортиазид и др.) и бензолсульфонамида (хлорталидон и др.); второе поколение – производные хлорбензамида (индапамид, ксипамид и др.), содержащие метилиндолиновую группу.
Гемодинамический эффект индапамидоподобных диуретиков обусловлен их фармакологическим действием: ингибирование реабсорбции Na+, Cl–, H+ и в меньшей степени К+ и Mg2+ в проксимальных и дистальных канальцах короткого сегмента нефрона. Одновременно обсуждаемые диуретики устраняют избыточное содержание ионов Na+ в сосудистой стенке (вследствие их высокой липофильности), повышают синтез простагландинов Е2 и простациклина I2, угнетают приток ионов Са2+ в гладкомышечные клетки сосудистой стенки, что вызывает дилатацию сосудов и снижает их чувствительность к прессорным агентам (катехоламины, тромбоксаны). Суммарный гемодинамический эффект индапамидов проявляется в виде:
1. Вазодилатация;
2. Уменьшение общего периферического сосудистого сопротивления (ОПСС);
3. Снижение АД;
4. Изменение вязкостных свойств крови за счет ингибирования агрегационной активности тромбоцитов.
Применение индапамидов в суточной дозе 2,5 мг оказывает гипотензивный эффект без существенного влияния на диурез.
По своей гипотензивной активности индапамид превосходит в 30 раз действие спиронолактонов, в 100 раз – фуросемида и в 300 раз – хлорталидона при применении в сопоставимых дозах.
Терапевтическая эффективность индапамидовых диуретиков продемонстрирована в ряде крупных рандомизированных исследованиях [6,11,14]. Отмечена их способность профилактировать развитие ИБС за счет снижение массы миокарда при АГ. Это свойство, нетипичное для других классов диуретиков, делает индапамид уникальным препаратом с кардиопротективным действием
, выраженность которого не уступает b-блокаторам и ингибиторам АПФ.
Особое внимание привлекает тот факт, что индапамидоподобные диуретики не обладают синдромом «отмены», не вызывают побочных метаболических нарушений: не оказывают отрицательного влияния на обмен глюкозы и уровень атерогенных липидов крови. В исследованиях последних лет, показано, что индапамид способствует нормализации уровня глюкозы у диабетиков II типа, профилактируя дабетическую нефропатию [10,15]. Индапамид, улучшая микроциркуляцию в почке, устраняет микроальбуминурию, являющуюся маркером генерализованного поражения сосудов и предиктором сердечно–сосудистых осложнений. Аналогичная закономерность отмечена при исследовании обмена холестерина (Х) и триглицеридов (ТГ) у пациентов с дислипопротеинемией. Индапамид снижает уровень атерогенного холестерина низкой плотности (ХЛПНП) и ТГ, одновременно увеличивая концентрацию липопротеидов высокой плотности (ХЛПВП).
Таким образом, индапамид
, сочетая в себе все положительные фармакодинамические, фармакокинетические и экономические достоинства, при отсутствии побочных эффектов других диуретиков,
является препаратом первой линии в плане лечения больных АГ и хронической сердечной недостаточности
.
В настоящее время иАПФ, несмотря на их большое количество, согласно химической структуре ответственной за связывание системного и тканевого АПФ, составляют три группы:
1. Содержащие сульфгидрильную группу (каптоприл);
2. Содержащие карбоксильную группу – карбоксиалкилдипептиды (Эналаприл
, квинаприл, лизиноприл , рамиприл, периндоприл, целазаприл, беназаприл);
3. Содержащие фосфильную группу (фозиноприл).
Каптоприл действует как активный препарат, выделяется почками, что ограничивает его применение при нарушении функции почек, требует минимум двукратного применения в сутки.
Эналаприл
метаболизируется в организме и действует за счет своих активных метаболитов, превосходит по длительности и силе действия каптоприл, что позволяет его однократное суточное применение и в меньших дозах по сравнению с каптоприлом, выделяется через почки.
Фозиноприл действует через метаболиты, применяется однократно в сутки и имеет два пути выведения – почки и желудочно–кишечный тракт.
Все иАПФ обладают кардио–, вазо–, нефро–протекторными и метаболическими эффектами:
1. Кардиопртективные эффекты:
восстановление баланса между потребностью и обеспечением миокарда О2, снижение пред– и постнагрузки на ЛЖ, уменьшение объема и массы ЛЖ, замедление ремоделирования ЛЖ, уменьшение симпатической стимуляции, антиаритмический эффект;
2. Вазопротекторные эффекты:
прямой антиатерогенный эффект, антипрофилиративный и антимиграционный эффект на гладкомышечные клетки, нейтрофилы и моноциты; улучшение и восстановление функции эндотелия; антитромбоцитарный эффект, усиление эндогенного фибринолиза, улучшение податливости артерий и снижение их тонуса;
3. Нефропротекторные эффекты:
снижение внутриклубочковой гипертензии, увеличение скорости клубочковой фильтрации, увеличение Na+ –уреза и уменьшение К+–уреза, уменьшение протеинурии, увеличение диуреза;
4. Метаболические эффекты:
усиление распада липопротеидов очень низкой плотности и снижение синтеза ТГ, усиление синтеза ХЛПВП, повышение чувствительности клеточных рецепторов к инсулину и усиление потребления глюкозы.
Резюмируя выше изложенное, можно утверждать, что на сегодняшний день иАПФ являются перспективной группой препаратов в лечение АГ, многопрофильность действия позволили назвать их «золотым стандартом в терапии сердечно–сосудистых заболеваний»
.
Целью данной работы является изучение эффективности и переносимости тиазидного диуретика – индапамида и ингибитора АПФ – эналаприла у больных АГ.
Материалы и методы исследования
Нами был обследован 51 пациент с АГ 1–2 ст. по классификации ВОЗ [4]: 10 мужчин и 41 женщина в возрасте 60–78 лет (средний возраст 66,1±3,7 года). Критерии включения в исследование больных АГ: систолическое АД от 140 до 180 мм рт.ст., диастолическое АД – от 90 до 110 мм рт.ст. Средняя длительность АГ по всей группе больных составила 12,3±4,5 лет.
Всем больным до лечения и через 24 недели после лечения проводилось суточное мониторирование АД (СМАД) на комплексе АВРМ – 04 (Венгрия), регистрация стандартной ЭКГ на шестиканальном электрокардиографе «Kenz» (Япония), ЭхоКГ исследование в М и В режимах на аппарате «Тоshiba – 104A» (Япония) с расчетом массы миокарда ЛЖ (ММЛЖ) по формуле предложенной Devereux R. и Reichek N. [8] и индекса ММЛЖ: ИММЛЖ = ММЛЖ/площадь поверхности тела. Одновременно проводилось исследование электролитов в сыворотке (Na, K, Ca) и биохимических показателей крови: содержание глюкозы и толерантность к глюкозе по стандартной методике путем забора крови через 120 мин после 75 г нагрузкой глюкозой; уровень липидов (общий холестерин – ОХ, ТГ, ЛПВП).
В зависимости от программы лечения больные АГ случайной выборкой были распределены на две группы: А – 26 пациентов получали индапамид в дозировке от 1,5 до 3 мг/сутки; группа Б – 25 пациентов, у которых базовой гипотензивной терапией был Эналаприл
от 10 до 40 мг/сутки.
В начале исследования больным АГ в качестве монотерапии назначали один из 2 изучаемых препаратов в минимальной дозе один раз в сутки утром. После первого приема препаратов больные находились под наблюдением врача в течение 2–4 часов для своевременного распознавания «гипотонии первой дозы». Контрольное исследование проводили через 4 недели. Если по данным СМАД АД достигало нормальных величин (среднедневное АД 140/90 мм рт.ст. и менее, и средненочное АД 125/80 мм рт.ст. и менее), доза препарата оставалась неизменной до конца исследования, т.е. до 24 недель. В том случае, если через 4 недели по результатам СМАД АД оставалось повышенным (среднедневное АД > 140/90 мм рт.ст. и/или средненочное АД > 125/80 мм рт.ст.) дозу препатата увеличивали. При этом при среднедневном АД, равном или более 140/90 мм рт.ст., а средненочном 125/80 мм рт.ст. и менее увеличивали утреннюю дозу. При средненочном АД 125/80 и более, независимо от уровня среднедневного АД, добавляли второй (вечерний) прием препарата. В том случае, если при СМАД не было отмечено нормализации АД как в дневное, так и в ночное время, дозу препарата вновь увеличивали. Окончательной считали ту максимальную дозу препарата, при приеме которой у больного не возникали побочные эффекты, либо дозу препарата, на которой была достигнута норма АД (среднедневное АД 140/90 мм рт.ст. и менее, и средненочное АД 125/80 мм рт.ст. и менее). После достижения окончательной дозы препарата она оставалась неизменной до конца исследования, т.е. до 24–й недели лечения. На 24–й неделе исследования во время последнего визита пациента повторно проводили СМАД, лабораторные исследования.
Статистическую обработку полученных данных выполняли с применением программного пакета электронных таблиц Microsoft Excel. Для установления взаимосвязи признаков применяли многофакторный корреляционный анализ с использованием критериев Пирсона и Спирмана. При обработке результатов и выявления корреляционных связей применялась значимость (вероятность) отклонений р<0,05 и менее.
Результаты лечения
Критерии оценки гипотензивной эффективности
расценивали по следующим параметрам:
хорошая
– при нормализации среднего уровня АД: снижение САД ниже 140 мм рт.ст. днем и 125 мм рт.ст. ночью, ДАД ниже 90 мм.рт.ст. днем и 75 мм рт.ст. ночью;
удовлетворительная
– при снижении среднего АД больше чем на 10 мм рт.ст. от исходного уровня без его нормализации;
неудовлетворительная
– при снижении среднего АД менее чем на 10 мм.рт.ст. без его нормализации. Регистрацию побочных эффектов производили на всех этапах исследования.
Переносимость лечения
оценивали по следующим критериям: отсутствие побочных эффектов – «
отличная
», слабо выраженные побочные эффекты, не требующие коррекции дозы – «
хорошая
», побочные эффекты, проходящие после коррекции дозы – «
удовлетворительная
» и тяжелые побочные эффекты, требующие отмены препарата – «
неудовлетворительная
» .
На рисунке 1 представлены результаты гипотензивной эффективности к концу программы исследования у больных АГ в зависимости от программы лечения.
Рис. 1. Диаграммы эффективности лечения больных АГ
В группе А хорошая эффективность назначенной терапии была у 16 пациентов (61,5%), удовлетворительная – у 6 пациентов (23%), неудовлетворительная – у 4 пациентов (15%); в группе Б хорошая эффективность лечения зарегистрирована у 14 пациентов (56%), удовлетворительная – у 9 пациентов (36%), неудовлетворительная – у 3 пациентов (12%).
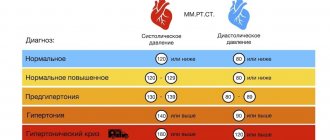
В таблице 1 представлена динамика профиля АД, характеризющий циркадный ритм, нарушения которого чаще всего встречаются у больных с сахарным диабетом II типа, с толерантностью к углеводам, с симптоматической АГ (феохромацитома, гипертония почечного генеза, ХПН), у лиц пожилого возраста.
Как видно из таблицы, в группе А, где в программу лечения был включен индапамид, до начала лечения
non–dippers
и
night–peakers
суммарно составили 53,8%, а в группе Б (лечение эналаприлом) – 61%, соответственно. Наличие патологического
non–dipper
и
night–peaker
– типов суточного профиля АД у больных, страдающих АГ, можно считать неблагоприятным прогностическим признаком. Общеизвестно, что «монотонный» суточный ритм АД часто встречается у пациентов с нарушением углеводного обмена и рассматривается, как одно из проявлений синдрома инсулинорезистентности (ИР) [2]. Сходный характер нарушений двухфазного ритма АД у больных двух групп позволяет предполагать, что эти изменения являются маркерами нарушений углеводного обмена. В результате лечения индапамидом и эналаприлом через 24 недели в обеих группах число больных с ночной гипертензией (
night–peakers
) и недостаточным ночным снижением АД (
non–dippers
) уменьшилось и в группе А составило 34,6% (практически вдвое), в группе Б – 44%, соответственно (p<0,01).
При анализе результатов ЭхоКГ (табл. 2) через 24 недели лечения эналаприлом установлено достоверное снижение индекса ММЛЖ (в среднем на 19%), уменьшение толщины стенок левого желудочка (в среднем на 12,3%). Изучая показатели Эхо–КГ через 24 недели лечения индапамидом, установлено достоверное снижение индекса ММЛЖ (в среднем на 29%), уменьшение толщины стенок левого желудочка (в среднем на 15%). Различия по сравнению с исходными данными достоверны по второму порогу вероятности безошибочных прогнозов (р<0,01).
Таким образом, у больных, получавших индапамид и эналаприл, степень снижения толщины стенок ЛЖ была сопоставима. Однако, на фоне терапии индапамидом уменьшение индекса ММЛЖ было более выраженным (почти 30%), что превышало соответствующие значения (около 19,1%%) для эналаприла. Полученные данные о регрессе гипертрофии миокарда ЛЖ совпадают с выводами других авторов [14,16,17]. Одним из возможных объяснений этого факта может быть – прогрессирующее с возрастом уменьшение количества функционирующих нефронов, вследствие гломерулосклероза, с уменьшением количества клеток юкстагломерулярного аппарата, вырабатывающего циркулирующий ренин, являющегося субстратом для синтеза ангиотензина, т.е. снижение вклада ренин–ангиотензин–альдостероновой системы (точка приложения для иАПФ) в формирование высоких цифр АД и в развитие ГМЛЖ [7].
При анализе ЭКГ достоверных изменений интервала PQ, QRS через 24 недели лечения на фоне индапамида и эналаприла не выявлено.
По данным биохимических показателей крови (табл. 3) на фоне лечения индапамидом и эналаприлом отмечено статистически недостоверное умеренное повышение глюкозы в плазме крови в среднем на 2,3% (р>0,05). По данным различных авторов, нетиазидные диуретики и ингибиторы АПФ не повышают вероятность развития сахарного диабета (СД) II типа [2,12,15].
В ходе лечения индапамидом и эналаприлом также не отмечено статистически достоверной динамики (различной направленности) в липидном спектре крови (р>0,05 по всем показателям). Уровень ХС при терапии индапамидом недостоверно увеличился на 0,75% (с 5,35±0,39 ммоль/л до 5,39±0,49 ммоль/л). В результате лечения эналаприлом имелась недостоверная, но отчетливая тенденция к снижению общего ХС на 5,51% (с 5,26±0,75 ммоль/л до 4,97±0,52 ммоль/л), Схожие данные были получены при оценке влияния препаратов на ТГ плазмы крови. Так, индапамид уменьшал уровень ТГ на 2,4% (с 1,499±0,41 ммоль/л до 1,463±0,35 ммоль/л), тогда как эналаприл на 2,86% (с 1,40±0,33 ммоль/л до 1,36±0,32 ммоль/л), однако эти изменения были недостоверными (р>0,05). Отсутствие отрицательного влияния индапамида и эналаприла на метаболизм липидов отмечено в целом ряде исследований [2,13,14,15,17,18].
Уровень мочевой кислоты (МК) повысился на фоне лечения индапамидом на 2,51% (с 234,00±29,09 мкмоль/л до 239,88±35,95 мкмоль/л) и уменьшился на 0,89% (с 224,30±35,93 мкмоль/л до 222,30±25,07 мкмоль/л) при лечении эналаприлом. Однако, эти изменения были недостоверными. В некоторых исследованиях [6] уровень МК повышался достоверно при приеме индапамида, однако, P. Weidmann [18] выявил увеличение МК при коротко длящейся терапии, а при пролонгированном приеме количество МК в крови уменьшается до исходных значений. По данным ряда авторов [7] эналаприл может увеличивать содержание МК в крови, однако имеются сообщения о нейтральном действии препарата [12,13]. Кроме того, индапамид уменьшал уровень мочевины на 3,83%, тогда как эналаприл увеличивал на 3,04%, однако эти изменения были недостоверны (р>0,05).
На фоне 24–х недельного цикла терапии обоими препаратами (индапамид и эналаприл) наряду со снижением АД все пациенты отмечали заметное улучшение общего состояния, проявляющееся уменьшением или исчезновением головной боли, шума в ушах, головокружения. У большинства пациентов повысилась трудоспособность и переносимость повседневных физических нагрузок. Из 26 пациентов группы индапамид полный курс лечения завершили все пациенты. Среди больных этой группы у 22% пациентов побочных эффектов не зарегистрировано – отличная переносимость. Хорошая переносимость выявлена более чем у половины пациентов (59%). Тяжелые побочные эффекты, требующие отмены препарата (неудовлетворительная переносимость), не выявлены. Самыми распространенными были сухость в полости рта – у 8 человек (30,8%), ортостатическая гипотония и головокружение – у 4 человек (15,4%), головные боли и запоры – у 2 пациентов (7,7%), зуд и парастезии – у 2 человек (7,7%), тошнота, кожная сыпь, нарушение координации отмечены в единичных случаях (3,8%).
В группе эналаприла примерно у четверти больных (21%) побочных эффектов не зарегистрировано – отличная переносимость. Хорошая переносимость установлена более чем у половины пациентов (52%). Тяжелые побочные эффекты (выраженный сухой кашель), требующие отмены препарата (неудовлетворительная переносимость), зарегистрированы у 4 человек (16%), миалгии, головокружение, кожная сыпь отмечены в единичных случаях (4%).
Обсуждение результатов
Как известно, уровень АД в организме определяется двумя физиологическими параметрами: МО (минутный объем) и общим периферическим сосудистым сопротивлением (ОПСС). Данную зависимость можно представить в виде следующей формулы:
АД = МО x ОПСС
При внезапном повышении МО (повышение активности симпатичеческой нервной системы), организм через функционирование барорефлекторного компенсаторного механизма уменьшает ОПСС, «гасит» эффект возросшего МО и способствует удержанию величины АД в пределах нормы.
Однако у некоторых индивидуумов отмечается неадекватность барорефлекторного контроля, что будет затруднять адекватную реакцию организма на колебания АД и способствовать «стабилизации» высоких цифр АД.
Таким образом, основная патофизиологическая сущность АГ определяется дисбалансом вазодилатирующих и вазоконстрикторных систем
, которая усугубляется нарушением метаболизма глюкозы и липопротеидов, ответственных за атерогенез.
На рисунке 2 представлена схема основных вазоконстрикторных систем и их взаимосвязь с поверхностью гладкомышечной клетки сосудистого русла и нервного симпатического окончания.
Рис. 2. Схема основных вазоконстрикторных систем и место действия иАПФ
Высвобождаемый из терминальных окончаний нейрона норадреналин (НА) через постсинаптические a2–адренорецепторы, расположенные на поверхности мышечной клетки, вызывает вазоконстрикцию, путем воздействия на кальциевые каналы и увеличения концентрации ионизированного Са2+ на сократительных внутриклеточных структурах (актин–миозин) гладкой мышцы. Одновременно высвобождаемый НА ограничивает свое выделение через стимуляцию пресинаптического a2–адренорецептора, лимитируя пролонгирование вазоконстрикторного эффекта.
Ангиотензин–II (АТ II), который образуется в результате деятельности циркулирующей и локальной (тканевой) РААС, свое вазоконстрикторное влияние осуществляет через несколько механизмов:
– прямое воздействие на АТ1–рецепторы, расположенные на поверхности мышечной клетки (постсинаптические рецепторы);
– усиление выделения НА из нейрона через стимуляцию АТ1–рецепторов (пресинаптических), расположенных на нервных окончаниях;
– усиление выделения эндотелиальными клетками еще одного мощного вазоконстриктора – эндотелина–1;
– увеличение входа в клетку ионизированного Са2+ (раскрытие медленных кальциевых каналов).
иАПФ, блокируя активность РААС, уменьшают многогранность констрикторного действия АГ II , что лежит в основе протекторного эффекта иАПФ для сердца, сосудов и почек. Опосредованно снижая выработку НА и поступление в клетку Са2+ (главного внутриклеточного компонента сокращения), иАПФ повторяют механизм действия таких гипотензивных препаратов, как антагонисты Са и a2–адреноблокаторы.
Индапамидоподобные диуретики (в частности индапамид
) гипотензивный эффект реализуют через удаление Na+ из сосудистой стенки (снижение чувствительности гладкой мышцы к симпатическому импульсу), уменьшение концентрации Ca2+ в миоплазме исполнительной клетки, снижение агрегационной активности тромбоцитов и выработки тромбоксана (мощного вазоконстриктора) через кальциевый механизм, сохранение нормального уровня концентрации Mg2+ внутри клетки – природного, физиологичного антагониста Ca.
Гипотензивный эффект индапамида и эналаприла в сочетании с метаболической нейтральностью (не оказывает отрицательного влияния на обмен глюкозы и липодов), подтвержденный данными наших исследований и других авторов [6,11,14,16,17], выгодно отличают их от других гипотензивных препаратов (тиазидные диуретики, b-блокаторы I–II поколения) и ставят в первый ряд программы лечения АГ.
Таким образом, препараты индапамид и эналаприл (иАПФ), обладая хорошей гипотензивной эффективностью в сочетании с метаболической нетральностью глюкозного и липидного обмена, имеют низкий процент побочных эффектов по сравнению с другими гипотензивными препаратами, их можно рекомендовать, как препараты первой линии в лечении АГ.
Литература:
1. Бутрова С. А. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению. Русский медицинский журнал 2001; 2: 56 – 60.
2. Кобалава Ж. Д., Котовская Ю. В, Школьникова Е. Э. Динамика показателей суточного мониторирования артериального давления и качества жизни у больных с систолической гипертонией при монотерапии арифоном. Терапевтический архив 1998; 9: 67 – 69.
3. Оганов Р. Г., Александров А. А. Гиперинсулинемия и артериальная гипертония: возвращаясь к выводам United Kingdom Prospective Diabetes Study. Русский медицинский журнал 2002; 10; 11: 486 – 491.
4. Рекомендации всемирной организации здравоохранения и международного общества гипертонии. 1999.
5. Шестакова М. В., Чугунова Л. А., Шамхалова М. Ш. Сердечно – сосудистые факторы риска у пожилых больных сахарным диабетом 2 типа и методы их коррекции. Русский медицинский журнал 2002; 10; 11: 480 – 485.
6. Achimastos A., Liberopoulos E., Nikas S. et al. The effects of the addition of micronised fenofibrate on uric acid metabolism in patients receiving indapamide. Curr Med Res Opin 2002; 18(2): 59–63.
7. De Rosa M. L., Cardace P., Rossi M. et al. Comparative effects of chronic ACE inhibition and AT1 receptor blocked losartan on cardiac hypertrophy and renal function in hypertensive patients. J Hum Hypertens 2002; 16(2): 133–140
8. Devereux R., Reicher N. Echocardiographic assessment of left ventricular mass in man. Circulation 1977; 55: 613–618
9. Guidelines Subcommittee. 1999 World Health Organization: International Sosiety of Hypertension guidelines for the management of hypertension. J Hypertens 1999; 17; 2: 151–183.
10. Kuo S. W., Pei–Dee, Hung Y. J. et al. Effect of indapamide SR in the treatment of hypertensive patients with type 2 diabetes. Am J Hypertens 2003 Aug;16(8):623–8
11. Lacourciere Y., Belanger A., Godin C. Long–term comparison of losartan and enalapril on kidney function in hypertensive type 2 diabetics with early nephropathy. Kidney Int 2000; 58(2): 762–769.
12. Mancia G., Omboni S., Agabiti–Rosei E. et al. Antihypertensive efficacy of manidipine and enalapril in hypertensive diabetic patients. J Cardiovasc Pharmacol 2000; 35 (6): 926 –931.
13. . Nikas S., Rizos E., Milionis H. The effects of the addition of losartan on uric acid metabolism in patients receiving indapamide. J Renin Angiotensin Aldosterone Syst 2000;1(3):289–291.
14. Ocon J, Mora J. Twenty–four–hour blood pressure monitoring and effects of indapamide. Am J Cardiol. 1990 May 2;65(17):58H–61H
15. Resnick L. M. Ionic basis of hypertension, insulin resistance, vascular disease and related disorders. The mechanism of «sindrom X». Am J Hypertens 1993; 6:123S–134S.
16. Tan K. W., Frise S. A. Efficacy and tolerability of doxazosin versus enalapril in the treatment of patients with mild–to–moderate hypertension. Clin Ther 1997; 19(3): 459–470.
17. Verdecchia P., Schillaci G., Reboldi G. P. Long–term effects of losartan and enalapril, alone or with a diuretic, on ambulatory blood pressure and cardiac performance in hypertension: a case–control study. Blood Press Monit. 2000; 5(3): 187–193.
18. Weidmann P. Metabolic profile of indapamide sustained–release in patients with hypertension: data from three randomised double–blind studies. Drug Saf 2001; 24(15): 1155–1165.
Сравнение безопасности Энапа и Эналаприла
Безопасность препарата включает множество факторов.
При этом у Энапа она достаточно схожа с Эналаприлом. Важно, где метаболизируется препарат: лекарственные вещества выделяются из организма либо в неизмененном виде, либо в виде продуктов их биохимических превращений. Метаболизм протекает спонтанно, но чаще всего задействует основные органы, такие как печень, почки, лёгкие, кожу, мозг и другие. При оценивании метаболизма у Энапа, также как и у Эналаприла мы смотрим, какой орган является метаболизирующим и наколько критично действие на него.
Соотношение риска к пользе – это когда назначение лекарственного препарата нежелательно, но оправдано при определенных условиях и обстоятельствах, с обязательным соблюдением осторожности применения. При этом у Энапа нет никаих рисков при применении, также как и у Эналаприла.
Также при рассчете безопасности учитывается проявляются ли только аллергические реакции или же возможная дисфункция основных органов. В прочем как и обратимость последствий от использования Энапа и Эналаприла.
Есть ли отличия между лекарствами?
Как правило, основное отличие между лекарствами заключается в ценовой политике, и особенностей дозировки активного вещества. Так, Энап лидирует среди пациентов, которым назначают минимальные дозы средства в концентрации 2,5 мг. К данной категории относятся больные с почечной и сердечной недостаточностью, а также пожилые, которым рекомендовано принимать дозу меньше 5 мг в сутки.
Энам можно использовать при диабетической нефропатии
Основным преимуществом применения Энапа является его комбинированное действие на организм, так как комбинация диуретика и ингибитора АПФ, позволяет использовать средство в минимальных дозах. Наличие инъекционной формы Энапа позволяет купировать острое повышение АД, ампулу средства, необходимо вводить каждые 6 часов. Продолжительность терапии составляет 48 часов, однако применение данного способа введения возможно лишь в условиях стационара под наблюдением специалистов, что делает аналог менее популярным среди пациентов.
Монотерапия Эналаприлом требует приема более высокой дозировки, что вызывает негативные явления в виде непродуктивного кашля. Целесообразным является назначение таблеток для дальнейшей стабилизации больного после перенесенного гипертонического криза.
Таким образом, оба медикамента обладают высокой эффективностью, поэтому способны качественно стабилизировать уровень кровяного давления, восстановить поврежденные ткани миокарда, и снизить риск развития патологических изменений со стороны сердца, и сосудов. При подборе лучшего лекарства, основное внимание следует обращать на производителя, от которого и зависит качество таблеток, и их лечебное действие на организм.
Сравнение привыкания у Энапа и Эналаприла
Как и безопасность, привыкание тоже включает множество факторов, которые необходимо учитывать при оценивании препарат.
Так совокупность значения таких параметров, как «cиндром о, у Энапа достаточно схоже со аналогичными значения у Эналаприла. Синдром отмены – это патологическое состояние, возникающее после прекращения поступления в организм веществ, вызывающих привыкание или зависимость. А под резистентностью понимают изначальную невосприимчивость к препарату, этим она отличается от привыкания, когда невосприимчивость к препарату развивается в течение определенного периода времени. Наличие резистентности можно констатировать лишь в том случае, если была сделана попытка увеличить дозу препарата до максимально возможной. При этом у Энапа значения «синдрома о достотачно малое, впрочем также как и у Эналаприла.
Видео по теме
Что лучше пить от давления? Обзор наиболее эффективных медикаментов в видео:
Подводя итоги, можно с уверенностью заявить, что Эналаприл и Энап являются яркими представителями эффективных гипотензивных средств, мягко снижающих артериальное давление, нормализующих кардиальную активность и предупреждающих развитие сердечной недостаточности.
Важно помнить, что данные препараты не следуют принимать без консультации специалиста, который назначит пациенту адекватные дозировки медикамента, учитывая степень сложности его недуга, наличие противопоказаний к приему и осложнений со стороны других органов.
Сравнение побочек Энапа и Эналаприла
Побочки или нежелательные явления – это любое неблагоприятное с медицинской точки зрения событие, возникшее у субъекта, после введения препарата.
У Энапа состояния нежелательных явлений почти такое же, как и у Эналаприла. У них у обоих количество побочных эффектов малое. Это подразумевает, что частота их проявления низкая, то есть показатель сколько случаев проявления нежелательного эффекта от лечения возможно и зарегистрировано – низкий. Нежелательное влияние на организм, сила влияния и токсическое действие у Энапа схоже с Эналаприлом: как быстро организм восстановиться после приема и восстановиться ли вообще.
Противопоказания и побочные действия
Перед назначением лекарственных средств из группы ингибиторов АПФ следует тщательно изучить противопоказания, позволяющие исключить риск развития побочных эффектов от терапии в каждом конкретном случае.
Препараты не стоит применять пациентам, у которых диагностированы:
- индивидуальная непереносимость к компонентам медикаментов;
- склонность к развитию ангионевротического отека и других форм аллергических реакций немедленного типа;
- порфирия;
- двухсторонний стеноз ренальных артерий;
- период беременности и кормления ребенка грудью.
Нередко ингибиторы АПФ вызывают побочные реакции, среди которых мигренозные боли, стойкое понижение кровяного давления, общая слабость и тошнота, головокружение, тревожность.
Принимать Энап или Эналаприл без назначения врача не следует, так как подобные действия могут усугубить состояние больного человека и спровоцировать развитие у него острых вариантов ишемической болезни сердца или срывов ритма.
Сравнение удобства применения Энапа и Эналаприла
Это и подбор дозы с учетом различных условий, и кратность приемов. При этом важно не забывать и про форму выпуска препарата, ее тоже важно учитывать при составлении оценки.
Удобство применения у Энапа примерно одинаковое с Эналаприлом. При этом они не являются достаточно удобными для применения.
Рейтинг препаратов составлен опытными фармацевтами, изучающий международные исследования. Отчет сгенерирован автоматически.
Дата последнего обновления: 2020-12-04 13:42:31
Отзывы врачей
Екатерина Громова, врач-терапевт, Нижний Новогород: «Энап назначаю при гипертонии и ишемии в качестве профилактики инфаркта. Эналаприл рекомендую при нестабильной стенокардии в комплексном лечении. Пациенты не всегда следуют инструкциям врача. Придя в аптеку, покупают более дешевый препарат Эналаприл. Жалоб на побочные эффекты почти не бывает. Оба препарата переносятся хорошо, если не нарушается дозировка».
Рекомендуем почитать: Мелоксикам и Диклофенак: что лучше?
Светлана Карташова, врач-терапевт, Ростов-на Дону: «Энап считаю более эффективным средством, чем Эналаприл, но многие пациенты предпочитают недорогие препараты. Назначаю лекарство при гипертонии 1-2 степени. Если заболевание протекает в тяжелой форме, то выписываю несколько препаратов. Из побочных эффектов могу отметить сухой кашель. В таком случае снижаю дозировку или подбираю другой препарат».
Отзывы пациентов
Валерий Кравцов, 53 года, Краснодар: «Как только исполнилось 50 лет, появилось много болячек, в т.ч. стало повышаться давление. Пришлось пройти обследование, после чего врач диагностировал артериальную гипертензию и назначил Энап. Лекарство не из дешевых, но купил и начал принимать его. Состояние улучшилось примерно через месяц.
Решил поискать аналоги и наткнулся на Эналаприл, который намного дешевле. Купил его и начал принимать в той же дозировке, которую назначил врач. Побочных действий не было, по эффективности оба препарата одинаковы, поэтому остановился на более дешевом средстве».
Ирина Романова, 47 лет, Сочи: «Эналаприл назначил терапевт после того, как диагностировал гипертонию 2 степени. Из-за проблем с щитовидной железой врач посоветовал минимальную дозировку. Никаких побочных эффектов не было, поэтому постепенно дозировку увеличили до 10 мг. Стала чувствовать себя намного лучше, но через несколько месяцев препарат перестал действовать.
Обратилась к врачу, рассказала о своих проблемах. Он выписал другой препарат — Энап, предупредив, что это лекарство подороже. Начала принимать его. Это лекарство действует мягче и эффективнее. Пока помогает, но, что будет через год, — не знаю».
Нина Круглицкая, 54 года, Хабаровск: «Эналаприл принимаю около года. Давление держится в норме. Когда начала пить лекарство, мучил сухой кашель. Думала, что начался бронхит, пошла к врачу. Но доктор сказал, что это побочное явление, которое часто бывает при приеме этого медикамента. Он предложил заменить его на другое, но кашель прошел, поэтому продолжила пить Эналаприл. Пока чувствую себя хорошо».
Рекомендуем почитать: В чем разница между препаратами Бетасерк и Бетагистин?