Бытует мнение, что осознание проблемы — это уже 50% ее решения. Однако осознать и принять болезнь подчас совсем непросто, и не только психологически: больные с синдромом Антона-Бабинского имеют существенные проблемы со слухом и зрением, но не осознают их в силу определенного поражения головного мозга.
Впервые наблюдения о том, как пациенты с корковой слепотой или глухотой воспринимают свои собственные заболевания, были опубликованы Габриэлем Антоном 1899 году [1]. В 1914 году описание было дополнено французским неврологом Жозефом Бабинским, отметившим аналогичные нарушения у больных с корковым параличом и предложившим термин «гемисоматоагнозия».
Суть синдрома Антона-Бабинского (анозогнозии) состоит в том, что больные не осознают свой недуг или же относятся к нему беззаботно и благодушно, при том, что у них отсутствуют признаки деменции или нарушенного сознания. Степень анозогнозии может быть различной — от недооценки нарушений и отсутствия тревоги в связи с дефектом до неосознания и даже отрицания болезни.
Агнози́я (греч. отрицательная приставка a + gnōsis — познание), МКБ 10 R48.1 — нарушение процессов узнавания и понимания значения предметов, явлений и раздражений, поступающих как извне, так и из собственного тела при сохранности сознания и функций органов чувств. Страдают высшие гностические механизмы воспроизведения целостных образов. Различают вкусовую, зрительную, обонятельную, сенситивную и слуховую формы. Малая медицинская энциклопедия. — М.: Медицинская энциклопедия. 1991-96 гг.
Анозогнози́я (а + греч. nosos — болезнь, gnosis — знание, познание), МКБ 10 R41.8 — разновидность агнозии, при которой у пациентов с психическим расстройством или неврологической патологией отсутствует осознание собственной болезни. В. Жмуров. Словарь терминов психиатрии — 2009.
Гемисоматоагнози́я — разновидность агнозии, при которой больной игнорирует половину тела при частичной сохранности ее функций. Так называемый синдром Бабинского слева или справа, а также с двух сторон. При полной или неполной сохранности движений в руке и ноге, больной не пользуется ими для осуществления разнообразных действий. Он «забывает» о них, игнорирует их существование, не включает в работу. А. Парняков, А. Власова. Нейропсихологические синдромы. — 2004.
Этиология и патогенез синдрома Бабинского
Симптомы синдрома Антона-Бабинского наблюдается при обширном поражении теменной доли субдоминантного (обычно правого) полушария головного мозга. Как и при других корковых синдромах, восприятие дефекта нарушено на стороне, противоположной патологическому очагу.
Современные датские неврологи Дэниэл Кондзиелла и Сиска Фрам-Фалкенберг в своей статье [2] высказывают предположение, что основная причина отсутствия осознания больными своего заболевания — повреждение не столько коры, сколько белого вещества (ассоциативных связей между первичными центрами и вторичной и третичной корой). То есть при повреждении коры «страдает» сама функция, а при повреждении белого вещества нарушается ее корковый «контроль».
Примечательно, что даже если больному «докажут», что с ним не всё в порядке, его беззаботность сохраняется. Вероятно, это объясняется тем, что пострадавшее субдоминантное полушарие является высшим центром, отвечающим за формирование эмоциональной оценки и осознание эмоций.
Чаще всего синдром Антона-Бабинского развивается в результате инсульта. Реже причиной служат новообразования головного мозга.
Синдром Антона-Бабинского — явление достаточно редкое. Поскольку речь идет о неврологическом синдроме, возникающем при ряде заболеваний, достоверной информации о его распространенности в литературе нет.
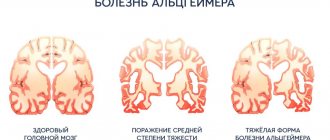
Болезнь Альцгеймера: причины, диагностика, лечение
Болезнь Альцгеймера является формой деменции или слабоумия, которую невозможно обратить вспять. Заболевание сопровождается прогрессирующей потерей памяти, снижением интеллектуальных способностей, ухудшением языковых и речевых навыков. Все эти симптомы в совокупности ведут к изменению поведения человека и снижению качества его жизни, итогом становится полная социальная дезадаптация. При болезни Альцгеймера поражение тканей мозга первично. Патологический процесс связан с накоплением амилоидного белка в межуточном веществе головного мозга и формированием сенильных бляшек, тау-протеина в клетках нервной ткани и формированием типичных структур, именуемых нейрофибриллярными клубочками. Образование патологических структур приводит к повреждению и гибели нервных клеток, снижению уровня нейротрансмиттеров, ухудшению взаимодействия между отделами головного мозга.
Болезнь Альцгеймера начинается с незначительных проблем с памятью, поскольку первыми поражаются височные доли коры головного мозга. Человек забывает куда положил вещь, для чего нужен этот столовый прибор, за чем ходил в магазин, в котором часу должен прийти на работу и т.д. Человек может не вспомнить дату рождения, свой адрес проживания, имена собственных детей, может теряться в простых вопросах, например, какой сегодня день, сколько времени, где и кем он работает. Позже присоединяются нарушения речи, больной не может вспомнить нужное слово, наблюдается расстройства ориентации, человек не может найти дорогу домой.
Стадии заболевания
В течении болезни Альцгеймера выделяют три стадии. На первой стадии больной может обслуживать себя самостоятельно, на второй стадии ему не обойтись без помощи близких. Человек не может самостоятельно одеться, принять душ, помыть посуду и т.д. Во время третьей стадии зависимость от присутствия родного человека становится тотальной: больной не может выполнить ни одно повседневное действие без посторонней помощи.
Заболевание и возраст
Риск возникновения болезни Альцгеймера и других форм деменции значительно возрастает с возрастом. Единичные случаи заболевания отмечаются после 40 лет, у людей 65 лет заболевание выявляется в 10–12%, в возрасте старше 85 лет в 30–40 % случаев.
Выделяют болезнь Альцгеймера с ранним и поздним началом. Ранее начало проявляется манифестацией заболевания до 65 лет и характеризуется быстрым прогрессированием. Высказан ряд предположений о генетической составляющей заболевания. «Позднее начало» болезни Альцгеймера проявляется после 65 лет, не считается унаследованным, его течение более плавное.
Генетическая предрасположенность
Болезнь Альцгеймера вызвана множеством еще недостаточно изученных факторов. Определены три гена, мутации в которых связаны с редкими ранними семейными формами заболевания. На их долю приходится 5% всех случаев. Гены PSEN1, PSEN2 и AP, расположенные на 14, 1 и 21 хромосомах, ответственны за синтез аномальных белковых структур, являющихся патоморфологическим субстратом болезни Альцгеймера. Существует 50% вероятность того, что мутация гена будет передана каждому из детей носителя патологического гена.
С поздним началом болезни Альцгеймера связаны другие гены. Они не считаются непосредственной причиной патологического процесса, хотя могут объяснить, почему существует повышенный риск развития позднего начала у лиц, в чьих семьях отмечались случаи заболевания. Ген APOE один из них. Ген APOE отвечает за продукцию аполипопротеина Е, белка-переносчика липидов (жиры и холестерин) в крови. Ген APOE существует в трех различных формах (аллелях): Е2, Е3 и Е4. Каждый человек наследует два аллеля APOE, которые представляют комбинацию этих трех. E3 является наиболее распространенным аллелем в популяции, обнаруживается у 60% населения в целом. Наличие аллеля Е4 APOE ассоциировано с большинством семейных случаев и повышенным риском развития болезни Альцгеймера, поэтому прогностически считается неблагоприятной комбинацией.
Факторы риска
Наряду с генетическими факторами, существуют и другие факторы риска болезни Альцгеймера. К ним относятся сахарный диабет 2 типа и более мягкие формы резистентности к инсулину, ожирение, высокое кровяное давление, дислипидемия и высокий уровень воспалительных маркеров, таких как С-реактивный белок (СРБ).
Диагностика
Точный клинический диагноз болезни Альцгеймера выставляется на основании клинической картины, благодаря использованию различных тестов и процедур, позволяющих исключить другие причины деменции. Врач оценивает личную и семейную истории болезни человека, проводит нейропсихологические тесты для измерения памяти, языковых навыков и других когнитивных функций.
Зачастую используются инструменты визуализации, такие как компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), для поиска признаков травм, опухолей и инсульта, а также атрофических изменений головного мозга, наблюдаемых при прогрессировании болезни.
Лабораторные тесты, позволяющие диагностировать болезнь Альцгеймера при жизни, к сожалению, отсутствуют. Единственным точным инструментом, подтверждающим наличие заболевания, является гистологическое исследование участка головного мозга после смерти. Патологоанатомы описывают сенильные бляшки и нейрофибриллярные клубочки, характерные для болезни Альцгеймера. Поскольку образование бляшек и клубочков также наблюдается при нормальном старении, то образец сравнивают с контрольным образцом нормальной ткани головного мозга человека того же возраста, но не страдающего заболеванием.
В 2011 г были разработаны новые критерии и рекомендации по диагностике болезни Альцгеймера. Выделены доклиническая, субклиническая и клиническая стадии заболевания, разработаны новые критерии синдрома деменции при болезни Альцгеймера.
Доклиническая стадия болезни Альцгеймера характеризуется отсутствием когнитивных нарушений, однако в головном мозге могут определяться амилоидные тельца. Появление биомаркеров при нейровизуализации является предвестником деменции за 10–15 лет до ее манифестации. Эта стадия выделена для того, чтобы помочь направить исследования в сторону ранней диагностики состояния.
Умеренные когнитивные нарушения из-за болезни Альцгеймера — наличие слабых изменений в памяти и способности мышления, которые не нарушают повседневную деятельность.
Деменция при болезни Альцгеймера. Память, мышление и поведенческие симптомы, которые нарушают способность человека функционировать в повседневной жизни.
Рекомендации призваны предоставить больше информации о нынешнем понимании болезни Альцгеймера и обеспечить основу для будущих исследований.
Лечение
Медикаментозная терапия включает группу препаратов ингибиторов холинэстеразы и антиглутаматэргические средства. Немедикаментозная терапия направлена на улучшение когнитивных функций и формирование нейронных связей: аэробные физические нагрузки, ведение активной социальной жизни, выполнение когнитивного тренинга.
Классификация типов синдрома Антона Бабинского
На настоящий момент описаны следующие типы анозогнозий (А. Парняков, А. Власова. Нейропсихологические синдромы. — 2004):
1. Анозогнозия слепоты. Возникает, если очаг поражения захватывает задние теменные и передние затылочные отделы коры. При этом больной отрицает полную потерю зрения центрального происхождения (например, при атрофии зрительного нерва или корковой слепоте), а отсутствие реальных зрительных впечатлений пытается компенсировать конфабуляторными, вымышленными образами, совершенно этого не осознавая. Так, на вопрос врача, какого цвета тот или иной предмет, больные уверенно отвечают, используя свой прошлый опыт, но затягивают с ответом, когда их спрашивают о количестве людей, находящихся в комнате. Страдающий корковой слепотой, будет утверждать, что у него всё в порядке со зрением и придумывать отговорки на возражения. Например, «в комнате темно» или же он «забыл надеть очки».
2. Анозогнозия глухоты (очаг поражения захватывает височные доли). Самый редкий вариант.
3. Анозогнозия афазии (очаг захватывает речевые центры). Встречается у больных с преимущественно грубой акустико-гностической сенсорной афазией, речь которых представляет собой поток сплошных литеральных и вербальных парафазий («словесная окрошка»). Больные не замечают ошибок в своей речи, думают, что речь их не изменена и хорошо понятна окружающим. Обнаружив, что их не понимают, начинают сердиться, проявляя аффективную неустойчивость. В более легких случаях сенсорной афазии, когда речь изменена умеренно, больные также не замечают собственных ошибок в речи (парафазии), не делают попыток их исправить, но при постоянных контактах с нейропсихологом способны согласиться с тем, что понимание речи окружающими у них неполноценно.
4. Анозогнозия паралича или гемиплегии (очаг захватывает прецентральную область коры). Типичным для данного расстройства является возникновение анозогнозий при параличе или парезе левых конечностей у правшей при инсульте. Больные утверждают, что движения в левых конечностях у них сохранены, что они могут, если захотят, встать и пойти, но в данный момент им просто не хочется этого делать. Такое отрицание двигательного дефекта часто сопровождается конфабуляциями: больные утверждают, что они не так давно гуляли, посещали своих родных и пр. Если обратить внимание больных на неподвижно лежащие левые конечности, они согласятся, что не могут ими двигать, но вскоре опять начинают настаивать на сохранности движений в левой руке и ноге.
5. Анозогнозия боли (очаг захватывает постцентральную область коры). Больные могут указать наличие и интенсивность раздражения, но неприятные ощущения, связанные с ним, у них отсутствуют или выражены слабо. В наиболее тяжелых случаях больные вовсе отрицают боль.
Системная красная волчанка
Начало болезни нередко характеризуется слабостью, похуданием, нарушением трофики, повышением температуры тела. В последующем развивается полисиндромная картина с типичными признаками для каждого синдрома.
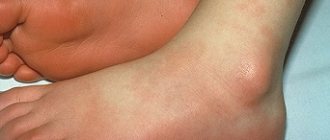
Поражение кожи при СКВ весьма разнообразно и нередко имеет первостепенное диагностическое значение. Лишь у 10- 15% больных кожные изменения могут отсутствовать. У 20- 25% кожный синдром бывает начальным признаком болезни, у 60-70% больных он появляется на разных этапах заболевания.
Е. Dubois выделяет до 28 вариантов кожных изменений при СКВ: от эритематозного пятна до тяжелых буллезных высыпаний. Поражения кожи при СКВ можно разделить на специфические и неспецифические.
Типичные для кожной формы красной волчанки очаги дискоидного характера с гиперемией, инфильтрацией, фолликулярным гиперкератозом и рубцовой атрофией встречаются в 25% случаев, как правило, при СКВ хронического течения.
Для дискоидной красной волчанки характерны три кардинальных клинических симптома: эритема, гиперкератоз и атрофия. Начало характеризуется появлением небольшого розового или красного пятна с четкими границами, которое постепенно покрывается в центре плотными серовато-белыми сухими чешуйками. Чешуйки крепко держатся в связи с наличием на их нижней поверхности шипообразных выступов, погруженных в расширенные фолликулярные устья (фолликулярный гиперкератоз). Характерно появление боли при снятии чешуек (симптом Бенье-Мещерского). Постепенно в центре очага начинает выявляться рубцовая атрофия и очаг принимает патогномоничный для дискоидной волчанки вид: в центре — гладкий нежный белый атрофический рубец, далее к периферии зона гиперкератоза и инфильтрации, а снаружи — венчик гиперемии. Типична локализация на открытых участках кожи: лице (особенно на носу и щеках с образованием фигуры бабочки), ушных раковинах, шее. Нередко поражается волосистая часть головы и красная кайма губ. Возможно расположение очагов на слизистой оболочке полости рта, где они могут изъязвляться.
При центральной эритеме Биетта (поверхностной форме красной волчанки) из трех основных кожных симптомов отчетливо выражена только гиперемия, в то время как чешуйки и рубцовая атрофия отсутствуют. Очаги обычно располагаются на лице и часто имитируют фигуру бабочки.
Множественные, рассеянные по различным участкам кожного покрова очаги дискоидной волчанки или центробежной эритемы Биетта характеризуют диссеминированную красную волчанку.
Высыпания на коже обычно не сопровождаются какими-либо субъективными ощущениями, однако эрозивные очаги на слизистой оболочке рта болезненны во время еды. Для кожной формы красной волчанки характерно многолетнее непрерывное течение с ухудшением весной и летом вследствие фотосенсибилизации. Среди редких кожных форм выделяют глубокую красную волчанку Капози-Ирганга, где наряду с обычными очагами имеется один или несколько резко отграниченных плотных подвижных узлов, покрытых нормальной кожей. Иногда эти узлы переходят в типичные очаги красной волчанки.
Наиболее частые кожные поражения при СКВ — изолированные или сливные эритематозные пятна различных очертаний и величины, отечные, резко отграниченные от окружающей здоровой кожи. Они идентичны поверхностной кожной форме красной волчанки и наблюдаются обычно на лице, шее, груди, в области локтевых, коленных и голеностопных суставов. Считается патогномоничным расположение подобных очагов на носу и щеках с образованием фигуры «бабочки» («волчаночная бабочка»). Реже наблюдается васкулярная «бабочка» в виде нестойкого, пульсирующего разлитого покраснения с цианотичным оттенком в средней зоне лица, усиливающегося при воздействии инсоляции, ветра, мороза или от волнения. Она почти неотличима от лихорадочной эритемы лица. Иногда «бабочка» имеет вид стойкого рожистого воспаления с резким отеком лица, особенно век. Поражение кожи с обилием эритематозных, резко отечных кольцевидных высыпаний может симулировать многоформную экссудативную эритему. Эта патология известна под названием синдрома Роуэлла.
Среди других кожных проявлений СКВ следует отметить люпус-хейлит (застойная гиперемия с плотными сухими сероватыми чешуйками, иногда корочками и эрозиями, с исходом в атрофию на красной кайме губ), так называемые капилляриты (отечная эритема с телеангиэктазиями и атрофией на подушечках пальцев, ладонях и подошвенной поверхности стоп и энантему — эритематозные участки с геморрагическими вкраплениями и эрозированием на слизистой оболочке рта.
К более редким поражениям относятся перниоподобные очаги (волчанка-ознобыш), буллезные, узловатые, уртикарные, геморрагические и папулонекротические высыпания, сетчатое и ветвистое ливедо с изъязвлениями и другие формы васкулитов.
Кроме того, у больных СКВ часты трофические нарушения: общая сухость кожи, диффузное выпадение волос, деформация и ломкость ногтей.
Целесообразно несколько подробнее остановиться на кожных проявлениях, входящих в диагностические критерии АРА. Алопеция относится к неспецифическим кожным признакам СКВ, но является самым частым среди них, встречается у 50% больных СКВ, причем поражаются волосы не только головы, но и бровей, ресниц и др. Различают рубцовую и нерубцовую алопецию. Рубцовая алопеция характерна для хронической СКВ и развивается обычно на месте дискоидных очагов. Нерубцовая алопеция проявляется диффузным истончением волос и наблюдается обычно в период тяжелого обострения СКВ. Диффузные формы алопеции обычно обратимы. Образовавшиеся из обломанных волос «столбики» по краю ростовой зоны являются патогномоничными признаками острой или подострой СКВ. При адекватной терапии восстанавливаются нормальные волосы.
Уртикароподобные поражения при СКВ никогда не бывают при чисто кожной красной волчанке и представляют собой уртикарный васкулит. В отличие от обычной крапивницы волдыри существуют более 24 ч. Тяжелых висцеральных изменений у этой группы больных обычно не наблюдается.
Фотосенсибилизация — частый и важный признак красной волчанки, наблюдается у 30-60% больных кожной формой и СКВ, является одним из диагностических критериев РА. Характерна локализация преимущественно на открытых участках кожи. Специальными исследованиями в эксперименте показано, что больные чувствительны как к А, так и к Взоне ультрафиолетовых лучей, подтвержден также факт обнаружения антител к ДНК, денатурированной ультрафиолетом, у больных СКВ, и отсутствие подобных антител при кожной форме волчанки и других фотодерматозах.
Поражение слизистых оболочек также входит в критерии АРА. На слизистой оболочке носа и рта могут быть белесоватые бляшки неправильных очертаний или серебристобелые рубцовые очаги. Нередко наблюдаются эрозивные и/или язвенные очаги с беловатым кератотическим ободком и интенсивной эритемой. Возможна перфорация носовой перегородки вследствие васкулита. При иммунофлюоресцентном исследовании биоптата из очага поражения обычно обнаруживают депозиты иммуноглобулинов и/или комплемента в дермоэпидермальном соединении, а иногда и в стенке сосудов. При гистологическом исследовании выявляют классический лейкоцитокластический ангиит.
Телеангиэктазии — частый признак при всех диффузных болезнях соединительной ткани. При СКВ описано три типа телеангиэктазий:
- небольшие линейные телеангиэктазии на заднем валике ногтевого ложа и на участках предлежащей кожи;
- неправильной формы, извитые на кончиках пальцев;
- в виде рассеянных пятен на ладонях и пальцах. Гистологически телеангиэктазии представляют собой только расширение сосудов без признаков воспаления.
В последние годы появилось значительное число работ, посвященных подострой кожной красной волчанке, которую описал R. Sontheimer дав ей название Subacute Cutaneus Lupus Erythstrongatosus (SCLE). Клинические симптомы поражения кожи при SCLE характеризуются распространенными аннулярными очагами, образующими полициклические участки на лице, груди, шее, конечностях. В центре очага-телеангиэктазии, гипопигментация. Рубцов не остается. Иногда высыпания могут быть папулосквамозными, напоминающими очаги поражения при псориазе. Обычно системные проявления болезни не столь выражены и характеризуются су ставномышечным синдромом, примерно 50% больных отвечают критериям АРА. Однако описаны довольно тяжелые формы с вовлечением ЦНС (20%), почек (10%). С помощью иммунологического исследования у 70% больных выявлены особые антитела к Ro(SSA)антигену, позднее была установлена статистически достоверная ассоциация SCLE с HLA DR3 и В8.
Особенности этой клинической формы волчанки описали А. А. Ароян и соавт..
Следует упомянуть также о характерных высыпаниях при волчанке новорожденных (неонатальная красная волчанка). Это очень редкий синдром. Т. Zizic полагает, что описано в литературе не более 100 случаев, тем не менее знать об этой форме необходимо. У новорожденного могут быть классическая кольцевидная дискоидная эритема, телеангиэктазии, атрофия кожи, фолликулярные пробки и чешуйки. Изменения исчезают в течение первых б мес жизни, иногда оставляя рубцовую атрофию, стойкую гипер или гипопигментацию. Такое поражение кожи обычно сочетается с частичной или полной блокадой сердца за счет фиброза его проводящих путей, что нередко является причиной летального исхода новорожденного. Из системных признаков наблюдаются гепатоспленомегалия, Кумбс-положительная гемолитическая анемия, антитела к La (SSB) и/или Ro (SSA)антигенам и РНК. Антинуклеарный фактор и LE-клетки нередко отсутствуют. Иммунологические изменения обычно также исчезают в течение б мес, иногда они являются единственным признаком неонатальной красной волчанки. Приблизительно у 20% матерей, родивших таких детей, впоследствии развивается красная волчанка или так называемая неполная красная волчанка, однако большинство из них клинически остаются асимптомными в течение всей последующей жизни, при этом в сыворотке крови можно обнаружить указанные выше антитела.
Существуют противоположные точки зрения в отношении того, являются ли СКВ и дискоидная красная волчанка вариантом одного и того же заболевания. Сходство их определяется следующими положениями: 1) кожные проявления при СКВ и дискоидной красной волчанке могут быть клинически и патологически неотличимы; 2) определенные клинические симптомы обнаруживают при обоих заболеваниях; 3) сходные гематологические, биохимические и иммунологические нарушения могут быть при обоих заболеваниях; 4) дискоидная красная волчанка иногда переходит в СКВ (3-12%); 5) у больных СКВ появляются типичные дискоидные очаги при стихании острой фазы болезни.
В то же время некоторые факты требуют объяснения: 1) сравнительно небольшой процент трансформации дискоидной формы в системную; 2) наличие лабораторных изменений при дискоидной красной волчанке не является указанием на предрасположенность к переходу в СКВ (гематологические нарушения отмечали у 50% из 77 больных с дискоидной волчанкой, но и через 5 лет наблюдения у них не развилась СКВ); 3) депозиты комплемента выявляют в непораженной коже при СКВ и не обнаруживают при дискоидной волчанке; 4) большинство больных с дискоидной волчанкой без осложнений переносят физические травмы, УФО, стрессы, у них не развиваются системные проявления; 5) возрастное и половое соотношение при возникновении СКВ значительно отличается от такового при дискоидной красной волчанке.
N. Rowell приводит сравнительную частоту некоторых клинических и лабораторных признаков при дискоидной красной волчанке и СКВ.
Полагают, что дискоидная красная волчанка, как и СКВ, возникает в результате соматической мутации популяции лимфоцитов у предрасположенных индивидуумов, но имеется различие в их генетической обусловленности. Таким образом, это самостоятельные заболевания, а не варианты какойто одной болезни. В то же время обе эти нозологические формы имеют несколько субтипов, также генетически детерминированных. Остается не до конца выясненным вопрос о возможности и частоте трансформации дискоидной волчанки в СКВ. Полагают, что при наличии генотипа, характерного только для дискоидной волчанки, никогда не происходит перехода в СКВ, даже под воздействием разнообразных внешних и стрессовых факторов. Однако, если у больных дискоидной волчанкой выявляют HLA-B8, имеется большой риск развития СКВ, особенно в возрасте 15-40 лет.
Поражение суставов и периартикулярных тканей. Артралгии встречаются почти у 100% больных. Боль в одном или нескольких суставах может продолжаться от нескольких минут до нескольких дней. При высокой активности болезни боли могут быть более стойкими, с развитием воспалительных явлений чаще всего в проксимальных межфаланговых суставах кистей, пястно-фаланговых, запястно-пястных, коленных суставах, могут поражаться и другие суставы. Процесс обычно симметричный. Утренняя скованность и нарушение функции суставов в острую фазу болезни значительно выражены, но быстро уменьшаются при снижении активности процесса под влиянием адекватной терапии. Состав синовиальной жидкости при остром и подостром артрите у больных СКВ значительно отличается от такового при РА. Синовиальная жидкость обычно прозрачная, вязкая, с небольшим числом лейкоцитов и преобладанием мононуклеарных клеток.
В суставной синдром следует включить и поражение связочного аппарата — тендиниты, тендовагиниты, вызывающие нередко при СКВ преходящие сгибательные контрактуры пальцев рук. При хроническом течении СКВ с преимущественным поражением суставов и околосуставных тканей сгибательные контрактуры принимают необратимый характер и могут стать причиной нарушения функции кисти. У 5% наблюдаемых нами больных отмечался фиброзирующий тендинит с резко выраженными контрактурами. Наряду с фиброзированием некоторых сухожилий значительно уменьшается их прочность. Мы наблюдали несколько случаев разрыва пяточного сухожилия, отрыва надколенника. Значительное повреждение околосуставных мягких тканей приводит при длительном хроническом течении артрита к формированию ревматоидоподобной кисти. При рентгенологическом исследовании выявляют эрозии лишь в 1-5% случаев, причем они не столь выражены, как при РА. Наши наблюдения позволили выявить ревматоидоподобное поражение кисти у 20% больных СКВ с хроническим артритом.
При СКВ наблюдаются асептические некрозы костей. Особенно часто поражается головка бедренной кости, по нашим наблюдениям до 25%. Однако может вовлекаться головка плечевой кости, как это было в нашем наблюдении у мужчины, заболевшего СКВ в возрасте 40 лет с развитием асептического некроза уже через б мес от начала болезни. Возможны множественные асептические некрозы с поражением костей запястья, коленного сустава, стопы. Образование асептического некроза костей может быть обусловлено как высокой активностью болезни, так и массивной кортикостероидной терапией.
Миалгия наблюдается у 35-45% больных, но признаки очагового миозита довольно редки. У некоторых больных резко выраженная мышечная слабость требует дифференциации с дерматомиозитом. При миастеническом синдроме, связанном с СКВ, как правило, не повышена активность АлАТ, АсАТ, креатинфосфокиназы. С помощью биопсии выявляют периваскулярные инфильтраты, вакуолизацию мышечных волокон и/или мышечную атрофию. Поражение мышц при СКВ в ряде случаев практически не отличается от такового при классическом дерматомиозите.
Поражение легких. В 50-80% случаев при СКВ наблюдается сухой или выпотной плеврит. Больных беспокоят боль в грудной клетке, небольшой сухой кашель, одышка. При небольшом количестве выпота плеврит может протекать незаметно и лишь при рентгенологическом исследовании выявляют утолщение плевры или жидкость в плевральных полостях обычно с обеих сторон, приподнятость диафрагмы. Наблюдается и довольно массивный выпот, достигающий Г/a-2 л. Описаны случаи СКВ, когда выпот с обеих сторон достигал III ребра и по жизненным показаниям приходилось проводить повторные пункции. Неадекватное лечение обычно приводит к образованию массивных спаек и облитерации плевральных полостей, что в дальнейшем резко снижает жизненную способность легких. Из-за массивных спаек диафрагма деформируется, снижается ее тонус, она подтягивается вверх с образованием высокого стояния с обеих сторон, но чаще справа. Плеврит при волчанке — важный диагностический признак, так же как и подтянутая диафрагма. В выпоте можно обнаружить LE-клетки, низкий уровень комплемента и высокое содержание иммуноглобулинов. По составу выпот представляет собой экссудат, содержащий более 3% белка, 0,55% глюкозы. При патологоанатомическом исследовании практически у всех больных находят признаки спаечного плеврита, значительное утолщение плевры. Микроскопически в плевре выявляют скопления макрофагов и лимфоцитов. В отдельных случаях возможен периваскулярный фибриноидный некроз с нейтрофильной и мононуклеарной инфильтрацией.
Поражение легких при СКВ — проявление классического васкулита, хотя непосредственно легочный васкулит довольно редкая патология, встречается в небольшом проценте случаев. N. Rothfield наблюдала легочный васкулит у 2% больных и всегда в сочетании с артериитом почечных сосудов и сосудов желудочно-кишечного тракта.
Люпус-пневмонит развивается обычно в период обострения СКВ с вовлечением в процесс других органов и систем. Клиническая картина скудна, нередко ограничивается выраженной одышкой, болью в грудной клетке, сухим кашлем у 50% больных. Редко отмечается кровохарканье. Рентгенологически характерно диффузное усиление легочного рисунка. Образование инфильтратов в легких не столь часто. Высокое стояние диафрагмы, обусловленное наличием плевро-диафрагмальных сращений и собственно легочным процессом, составляет важный рентгенологический диагностический признак люпус-пневмонита. Жизненная емкость легких у таких больных значительно снижена, выявляются признаки гипоксемии.
При сканировании иногда определяются кистевидные образования в нижних отделах легких. При высокой лихорадке, кашле с мокротой необходимо проводить дифференциальную диагностику с разнообразной вторичной инфекцией (бактериальной, вирусной, грибковой). Наиболее затруднительна диагностика с туберкулезом, особенно у больных, длительно леченных кортикостероидами.
В ряде случаев приходится проводить чрезбронхиальную биопсию. В диагностике может помочь также проведение кожных тестов, исследование полученного плеврального экссудата.
Поражение сердца и сосудов. Наиболее часто при СКВ наблюдается перикардит. Перикард, по данным разных авторов, вовлекается в процесс в 25-51% случаев. Характерен сухой перикардит, в отдельных случаях может наблюдаться значительный выпот вплоть до тампонады сердца. Сухой перикардит диагностируют на основании жалоб (боль за грудиной, сердцебиения, затруднение глубокого вдоха), объективных данных (тахикардия, приглушенность тонов, иногда шум трения перикарда). Вспомогательное значение имеют показатели ЭКГ и ФКГ (снижение вольтажа, отрицательный зубец Т, высокочастотный шум). Выявление небольшого выпота облегчает эхокардиографию.
Значительный выпот определяется клинически и рентгенологически.
Мы наблюдали случай выпотного перикардита у 18-летней девушки с поражением кожи по типу «бабочки», алопецией, высокой лихорадкой, резчайшей одышкой, тахикардией более 200 в 1 мин. Состояние было близким к тампонаде сердца. При пункции перикарда было получено почти 1,5-2 л густой жидкости желтого цвета, напоминающей гной. Однако выпот оказался асептическим, а гноеподобный вид жидкости был обусловлен большим количеством содержащегося в ней фибрина. В перикардиальной жидкости выявлены LE-клетки, низкий уровень комплемента. Состояние больной улучшилось только после назначения 60 мг преднизолона в день.
При длительном течении СКВ у больных с рецидивирующим (даже сухим) перикардитом развиваются массивные спайки.. Для этой группы больных характерна даже вне обострения СКВ стойкая боль за грудиной, в боку, усиливающаяся при смехе, чиханье, длительно может выявляться шум трения перикарда. В редких случаях отмечаются массивные перикардиальные наложения с облитерацией перикарда столь выраженной, что требуется хирургическое вмешательство.
Миокардит обычно наблюдается у больных с высокой степенью активности. Клиническая картина диффузного миокардита, данные ЭКГ и ФКГ не имеют специфических черт и соответствуют критериям этой патологии. Важно то обстоятельство, что эффективны лишь кортикостероиды, сердечная недостаточность не купируется препаратами дигиталиса, которые могут быть лишь вспомогательным средством в адекватной кортикостероидной терапии.
Нерезко выраженное поражение миокарда иногда не диагностируется из-за других более тяжелых проявлений СКВ (цереброваскулит, нефрит) и купируется терапией, адекватной общей активности болезни.
При патологоанатомическом исследовании поражение миокарда выявляют довольно часто: находят очаговые инфильтраты из лимфоцитов и плазматических клеток; могут быть даже очаговые некрозы, рубцовые изменения. В сосудах миокарда обнаруживают отложения фибрина. Поражается проводящая система сердца. Наблюдается атриовентрикулярная блокада.
Эндокардит в последние годы диагностируется при жизни довольно часто. Клинически эндокард изолированно не поражается. Как правило, вовлекаются все оболочки сердца и обязательно перикард.
При эндокардите выслушивается грубый систолический шум на верхушке и других проекционных точках сердца (чаще в точке Боткина), выявляют и диастолический шум, ослабление I тона на верхушке. Классический эндокардит Либмана-Сакса в основном патоморфологический признак СКВ, реже клинически выявляют пороки сердца. Бородавчатые изменения обнаруживают чаще при микроскопическом исследовании, но они могут быть видны и макроскопически. Чаще поражается митральный клапан. Сотрудниками Института ревматологии АМН описано 4 случая митрального порока сердца у больных с достоверной СКВ. Имеются сообщения также о поражении аортального и трикуспидального клапана.
Из сосудов при СКВ поражаются в основном артерии среднего и мелкого калибра. Степень и выраженность поражения сосудов варьируют. Полагают, что антитела к ДНК, преципитирующие в контриммуноэлектрофорезе, ассоциируются с артериитом, а различия в клинической патологии сосудов обусловлены составом иммунных комплексов, в которые входят антитела с разной аффинностью.
Кожные васкулиты представлены эритематозными высыпаниями, дигитальными капилляритами, ишемическими некрозами кончиков пальцев кистей, а также сетчатым ливедо.
Поражается и венозное звено. Тромбофлебиты конечностей как проявление васкулита наблюдались нами у 25% больных, возникли, как правило, в период обострения СКВ и поддавались только лечению кортикостероидами.
Поражение крупных сосудов при СКВ требует дополнительного изучения.
К настоящему времени имеется небольшое число сообщений о вовлечении в процесс аорты и ее ветвей, подключичной артерии и коронарных сосудов, тромбозах магистральных сосудов конечностей с гангреной. В Институте ревматологии РАМН мы наблюдали двух больных с тромбозом глубоких вен плеча. В одном случае консервативное лечение было эффективным, в другом потребовалось извлечение тромба хирургическим путем. Нередко наблюдаются тромбофлебиты поверхностных вен плеча и передней поверхности груди.
Коронарные артерии вовлекаются в процесс не столь редко. В ранние сроки болезни коронарит связан с высокой активностью СКВ. Описаны случаи инфаркта миокарда у молодых женщин. В поздние сроки коронарит связан с возможностью развития атеросклероза при длительной терапии кортикостероидами. Имеются’сообщения, что коронароатеросклероз возникает уже через год терапии кортикостероидами. Существует четкая корреляция поражения коронарных артерий с высоким АД. Инфаркт миокарда при большой давности СКВ является наиболее частой причиной смерти в описаниях последних 10 лет. В связи с этим рекомендуется интенсивное лечение гипертензии с момента ее выявления.
Поражение желудочно-кишечного тракта при СКВ наблюдается почти в 50% случаев. В острый период болезни характерны жалобы на отсутствие аппетита, отвращение к пище, тошноту, рвоту, изжогу, боль в различных отделах живота. При рентгенологическом исследовании вовлечение пищевода в процесс отмечают у 10-15% больных, наблюдают дилатацию пищевода, нарушение его моторики. При морфологическом исследовании нередко выявляют изъязвление слизистой оболочки пищевода, желудка и двенадцатиперстной кишки, дегенерацию коллагеновых волокон, распространенный артериит. Описана ишемия стенки желудка или кишечника с перфорацией.
Поражение кишечника тесно связано с вовлечением серозных оболочек и непосредственным поражением сосудов брыжейки и кишечного эндотелия. Артериит, поражающий мезентериальные сосуды, является основной причиной абдоминального криза при СКВ. Как правило, абдоминальные кризы возникают в период высокой активности СКВ и совпадают с другими признаками васкулита — поражением ЦНС, обострением нефрита, тяжелым синдромом Рейно. До острого («хирургического») живота могут быть преходящие боли (иногда за несколько месяцев до криза), локализующиеся вокруг пупка, в нижнем квадранте живота. При пальпации имеется болезненность по всему животу и иногда определяются участки ригидности брюшной стенки. Причин абдоминального криза достаточно много, в том числе серозит (первичный перитонит), язвенное поражение желудка и кишечника, панкреатит, поэтому необходима дифференциальная диагностика, которой помогает иногда тщательный анализ характера боли. Так, боль в эпигастрии, в верхней части живота более характерна для панкреатита, язвы желудка. Боль в нижних отделах — для брыжеечного артериита, перфоративной язвы нисходящей толстой кишки, некротизирующего энтероколита с пневматозом в тонком кишечнике.
Рентгенологическое исследование не всегда помогает диагностике, но могут быть обнаружены растяжение толстого кишечника и «уровни жидкости», утолщение складок слизистой оболочки с «отпечатками больших пальцев» или сужением просвета кишки, псевдообструкция, атония желудка, дуоденостаз. Свободный воздух в полости живота — поздний признак, требующий срочного хирургического вмешательства. Для уточнения диагноза используют парацентез с определением состава полученной жидкости. Если она стерильна, нужно увеличить дозу кортикостероидов, так как в этом случае абдоминальный криз обусловлен васкулитом. Если жидкость инфицирована, это значит произошла перфорация и необходимо хирургическое вмешательство. Следует помнить о том, что кортикостероиды могут «смазывать» картину острого живота и особенно внимательно обследовать больных в случае появления боли в животе при СКВ. При появлении признаков острого живота необходим точный диагноз, так как при упущенных сроках даже умело проведенная операция, включающая иссечение некротизированной части кишечника и идеальный гемостаз, не спасает от неблагоприятного исхода. Поэтому, если боль не купируется в течение 1-2 дней парентеральным введением больших доз кортикостероидов, необходима лапаротомия.
Поражение поджелудочной железы и печени при СКВ требует дальнейшего изучения. Острый панкреатит диагностируют редко, однако в сравнительно недавних исследованиях признаки острого панкреатита были выявлены у 20 (8%) из 241 больного на фоне высокой активности болезни с вовлечением многих органов и систем и наличием васкулита, преимущественно артериита. Развитие панкреатита крайне неблагоприятно для прогноза.
Патология печени при СКВ проявляется от незначительного увеличения ее размеров до картины довольно тяжелого гепатита. Гепатомегалия выявлена в 23-50% случаев по данным разных авторов, при этом желтуха наблюдалась у 3-7%, в то же время нередко повышаются уровни АсАТ и АлАТ. При гистологическом исследовании биоптата печени отмечают полнокровие и застой в сосудах, жировую инфильтрацию и некрозы в портальной системе. Иногда выявляют артериит, приводящий к инфарктам печени, спонтанным разрывам, обусловливающим картину острого живота.
Собственно волчаночный гепатит следует дифференцировать от хронического активного гепатита (ХАГ). При сходных симптомах имеются, однако, и отличительные черты. Так, диарея в 30% случаев встречается при ХАГ и только в 5% — при СКВ, гапатомегалия при ХАГ выявляется в 75% и спленомегалия в 50%, при СКВ-в 20%. Более характерны для ХАГ такие признаки, как желтуха (80%), повышение уровня аминотрансфераз (90%) и щелочной фосфатазы (50%), гипергаммаглобулинемия (60%). В то же время наиболее часто встречающиеся при СКВ такие показатели, как LE-клетки (75%), высокий титр антинуклеарного фактора (90%), при ХАГ выявляют в 15 и 40% соответственно. В наблюдении Т. Zizic антитела к нативной ДНК при СКВ были выявлены у 45%, а при ХАГ отсутствовали, в то же время антитела к гладкой мускулатуре при ХАГ были у 70% больных, а при СКВ отсутствовали. Такие клинические признаки, как полисерозит и гломерулонефрит, поражение ЦНС, очень редки при ХАГ. В то же время эритематозные высыпания, вульгарные угри, пурпура, витилиго могут наблюдаться достаточно часто и при ХАГ. Лейкопения, тромбоцитопения, положительная проба Кумбса характерны для обоих заболеваний. Если клинические и лабораторные признаки не позволяют провести дифференциальный диагноз, следует прибегнуть к биопсии печени, позволяющей подтвердить диагноз ХАГ. Повышение уровня аминотрансфераз может быть обусловлено и лекарственными препаратами, в первую очередь ацетилсалициловой кислотой (гепатотоксична у 25% больных), а также циклофосфамидом. При дифференциальной диагностике следует помнить о возможности вирусного гепатита. Однако патология печени у больных СКВ на высоте активности болезни, как правило, связана с самим заболеванием.
Поражение почек. Механизм развития волчаночного нефрита отражает патогенез СКВ в целом. Это классическое иммунокомплексное заболевание, для которого характерна неконтролируемая продукция антител, образующих иммунные комплексы, обусловливающие поражение почек.
Изучение патогенеза нефрита в эксперименте наглядно показало патогенетическую обусловленность различных типов поражения почек в зависимости от характера иммунного ответа. Так, у гибрида новозеландских мышей B/W развивается прогрессирующий иммунокомплексный гломерулонефрит, как правило, со смертельным исходом. Подобный злокачественный нефрит, рано приводящий к смерти развивается у мышей линии MRL/MPlpr/lpr (близкой к MRL/I). В то же время у другой линии мышей — MRL/n, отличающейся по единственному генетическому локусу от указанных животных, развивается умеренное поражение почек, не влияющее на продолжительность жизни животных. У мышей линии BXSB развиваются тяжелый нефрит и аутоиммунная гемолитическая анемия. Гистопатологические изменения в почках при аутоиммунном нефрите у мышей аналогичны таковым при люпус-нефрите у людей, хотя имеются некоторые особенности. Так, у мышей линии NZB гистологические проявления в почках ограничиваются мембранозным типом нефрита, а у других линий мышей развивается в основном диффузный пролиферативный нефрит. Моделью, почти абсолютно близкой к человеческой, является нефрит у гибридов NZB/NZW f, что дало возможность детально изучить гистологические изменения и выделить морфологические типы нефрита, доказать его иммунокомплексную природу, выделив из гломерул иммунные комплексы, содержащие ДНК, антиДНК, IgG, C3 и другие компоненты иммунного ответа.
Морфологические изменения в почках при СКВ встречаются значительно чаще, чем клинические проявления нефрита. Иммунофлюоресцентное исследование биоптата или патологоанатомического материала почки практически у всех больных позволяет выявить депозиты иммуноглобулинов или фракций комплемента в базальной мембране гломерул. Гистологические изменения в биоптате находят более чем у половины больных СКВ без клинических признаков нефрита.
Морфология волчаночного нефрита отличается полиморфизмом. Помимо гистологических изменений, свойственных гломерулонефриту вообще (пролиферация мезангиальных и эпителиальных клеток, расширение мезангиума, изменения базальных мембран капилляров и др.), отмечают и изменения, достаточно специфичные именно для СКВ, — фибриноидный некроз капиллярных петель, кариопикноз и кариорексис, гематоксилиновые тельца, гиалиновые тромбы, «проволочные петли». В биоптатах почек эти признаки встречаются с различной частотой, при этом картина варьирует. Выраженность и распространенность изменений в интерстиции, канальцах, сосудах четко коррелируют с тяжестью поражения гломерул. Изолированные тубулоинтерстициальные изменения казуистически редки.
С 1982 г. за рубежом используется в основном классификация волчаночного нефрита, предложенная ВОЗ, с небольшими модификациями каждого из исследователей. Эта классификация включает б классов: I — отсутствие изменений в биоптате; II — мезангиальный нефрит; III — очаговый пролиферативный гломерулонефрит; IV — диффузный пролиферативный гломерулонефрит; V — мембранозный гломерулонефрит; VI — склерозирующий гломерулонефрит.
В основе отечественной классификации волчаночного нефрита лежат характер морфологических изменений и распространенность процесса. Выделяют следующие типы гломерулонефрита:
- очаговый волчаночный пролиферативный;
- диффузный волчаночный пролиферативный;
- мембранозный;
- езангиомембранозный;
- мезангиопролиферативный;
- мезангиокапиллярный;
- фибропластический.
Имеются определенные параллели между этими двумя классификациями: II класс ВОЗ близок мезангиомембранозному гломерулонефриту по классификации В. В. Серова и соавт., III класс включает в себя лишь часть случаев, описываемых В. В. Серовым и соавт. под названием «очаговый пролиферативный гломерулонефрит», так как «очаговость» и «диффузность» по классификации ВОЗ определяются степенью распространенности всех гистологических изменений, а по классификации В. В. Серова — степенью распространенности лишь специфических волчаночных признаков. Соответственно класс IV включает в себя не только «диффузный пролиферативный волчаночный нефрит» В. В. Серова и соавт., но и часть случаев «очагового пролиферативного волчаночного нефрита», а также случаи мезангиопролиферативного, мезангиокапиллярного и, очевидно, фибропластического нефрита. Наконец, V класс ВОЗ полностью соответствует мембранозному нефриту в классификации В. В. Серова и соавт.
При иммуногистохимическом исследовании в клубочках чаще выявляются IgG, C3, фибрин; несколько
Два случая из практики
В качестве примера можно привести историю болезни пациента с синдромом Антона-Бабинского, описанную датскими неврологами Дэниэлем Кондзиеллой и Сиской Фрам-Фалкенберг.
«Мужчина, 55 лет, после 3-недельной лихорадки и ночной потливости стал очень странно себя вести. Натыкался на столы и стулья, никак не мог найти чашку, стоящую прямо перед ним, друзей и родственников узнавал только тогда, когда они с ним заговаривали. Несмотря на то что он явно потерял зрение и не мог самостоятельно справляться с повседневными делами, сам этого не признавал. Отрицал свою слепоту и, натыкаясь на препятствия, придумывал этому безобидные оправдания. Если ему задавали вопросы о внешнем виде чего-либо, он без колебаний что-нибудь выдумывал.
У пациента диагностирован инфекционный эндокардит — при чреспищеводной ЭхоКГ выявлены вегетации на клапане аорты. Начат подбор антибиотиков. КТ головного мозга выявила обширный инфаркт обеих затылочных долей и белого вещества левой теменной доли. После установки протеза аортального клапана повторных эпизодов эмболии не наблюдалось. После хирургического вмешательства, пациент постепенно начал осознавать, что ослеп, однако по-прежнему относился к этому факту равнодушно. Несмотря на длительную программу реабилитации, так и не смог вернуться к самостоятельной жизни».
Из опроса пациента с синдромом Антона-Бабинского.
Врач:
Как Ваше самочувствие?
Пациент:
Нормально.
Врач:
С Вами всё в порядке?
Пациент:
Да, всё прекрасно.
Врач:
А как насчет Вашего зрения?
Пациент:
Всё хорошо.
Врач (показывая ручку):
Скажите, что это?
Пациент:
Доктор, тут слишком темно. Никто же ничего не видит.
Врач (включая электрический свет, несмотря на то что за окном светло):
Я включил свет. Теперь Вы можете сказать, что это?
Пациент:
Слушайте, не хочу я с Вами в эти игры играть.
Врач (высокий и худощавый):
Ладно. А внешность мою Вы можете описать?
Пациент:
Конечно. Вы маленький такой и толстый [2].
Известный британский невролог, нейропсихолог и публицист Оливер Сакс в своей книге «Человек, который принял жену за шляпу» (1971) на примерах своих пациентов описывает несколько видов анозогнозий. Вот, например, отрывок из рассказа «Направо, кругом!», в котором описана жизнь миссис С., шестидесятилетней женщины, перенесшей обширный инсульт:
«Миссис С. бесповоротно утратила идею «левой стороны‟- как в отношении мира, так и в отношении своего собственного тела. Иногда она ворчит, что ей дают слишком маленькие порции, но это происходит оттого, что она берет пищу только с правой стороны тарелки. Ей и в голову не приходит, что у тарелки имеется левая половина. Решив привести в порядок внешность, она красит губы и пудрится тоже только справа, а к левой стороне лица вообще не притрагивается. Помочь ей тут практически невозможно, поскольку никак не удается привлечь ее внимание к нужному месту. Умом она, конечно, понимает, что что-то не в порядке, и порой даже смеется над этим, но непосредственного знания у нее нет.
На помощь ей приходит интеллект и дедукция. Она выработала различные стратегии, позволяющие действовать в обход дефекта. Не имея возможности смотреть и поворачиваться влево, она разворачивается вправо. Для этого она заказала вращающееся кресло-каталку и теперь, не обнаружив чего-нибудь на положенном месте, крутится по часовой стрелке до тех пор, пока искомое не окажется в поле зрения. Если ей кажется, что на тарелке не хватает еды, она тоже начинает вертеться вправо. Доехав по кругу до недостающей половины, она съедает ее, точнее половину этого количества, и таким образом утоляет голод. […]
Казалось бы, чем вращаться самой, гораздо легче поворачивать тарелку. Она тоже так считает и говорит, что уже пробовала, но натолкнулась на странное внутреннее сопротивление. Выяснилось, что ей гораздо легче и естественнее крутиться на стуле, поскольку всё ее внимание, все ее движения и импульсы инстинктивно обращены теперь вправо и только вправо».