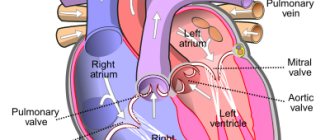
При нормальном строении сердца в левое предсердие впадают легочные вены, и именно по ним насыщенная кислородом кровь поступает в левый желудочек, а затем – в аорту. Далее она разносится артериями по большому кругу кровообращения.
Под воздействием ряда внешних негативных факторов во внутриутробном периоде могут создаваться условия для формирования такого врожденного порока развития сердца как аномальный дренаж легочных вен (АДЛВ), при котором эти сосуды впадают не в левое, а в правое предсердие, полые вены или венечный синус. Такое ненормальное расположение сосудов может быть частичным или тотальным, т. е. с правым предсердием может сообщаться часть отдельных легочных вен или все устья этих сосудов. Именно от этих факторов во многом зависит состояние больного.
По данным статистики, АДЛВ выявляется у 1,5-3% пациентов с врожденными пороками развития сердца. Чаще такая патология обнаруживается среди мужчин.
Нередко АДЛВ сочетается с такими аномалиями развития сердца как открытое овальное окно и дефект межпредсердной перегородки. А у 20% больных ему сопутствуют другие дефекты: общий артериальный ствол, тетрада Фалло, декстрокардия, дефект межжелудочковой перегородки, недоразвитие левых камер сердца и др. Кроме этого, у пациентов с этим диагнозом нередко выявляются внекардиальные аномалии развития: подковообразная почка, поликистоз почек, гидронефроз, пупочные грыжи, дивертикулы кишечника и пороки развития опорно-двигательного аппарата или эндокринной системы.
В этой статье мы ознакомим вас с предположительными причинами, разновидностями, проявлениями, способами выявления и лечения аномального дренажа легочных вен. Полученная информация поможет вам понять суть такого врожденного порока сердца, и вы сможете задать интересующие вас вопросы лечащему врачу.
Немного истории
Впервые этот редкий врожденный порок был описан Вилсоном еще в 1798 году, но его варианты более детально были рассмотрены только после накопления достаточного кардиохирургического опыта в 50-60 годах XX века. Первая удачная операция по коррекции этой патологии была выполнена Миллером в 1951 году. Впоследствии кардиохирургические методики совершенствовались, и в 1956 году была проведена радикальная коррекция АДЛВ при помощи поверхностной гипотермии. В этом же году подобное вмешательство было выполнено с использованием искусственного кровообращения.
На территории СССР впервые успешная операция по устранению такого порока сердца была проведена Николаем Михайловичем Амосовым в 1978 году, а о выполнении серии удачных коррекций у детей раннего возраста в 1984 году сообщил один из ведущих российских кардиохирургов Георгий Эдуардович Фальковский.
Причины
Вероятно, определенную роль в развитии АДЛВ играет наследственность.
Вероятными причинами развития АДЛВ могут становиться те же внешние факторы, которые провоцируют и другие врожденные аномалии строения сердца и сосудов:
- наследственность (мутации хромосом);
- прием некоторых тератогенных лекарств;
- воздействие токсических веществ на организм во время беременности;
- вредные привычки будущей матери;
- перенесенные беременной инфекционные заболевания;
- эндокринные нарушения;
- токсикоз;
- неблагоприятная экология.
Разобщенность легочных вен с левым предсердием может вызываться следующими факторами:
- отсутствие их соединения с левым предсердием – формируется из-за того, что под влиянием вышеописанных внешних причин левопредсердный вырост не может связаться с венозными сплетениями будущего легкого;
- ранняя атрезия легочной вены – происходит при первоначальном соединении легочного сосудистого ложа и общей легочной вены, просвет которых впоследствии облитерируется, и кровь из легких начинает поступать через иные коллатеральные пути.
Врожденная аневризма левого предсердия
Врожденный дефект, проявляющийся аневризматической дилатацией левого предсердия без заболеваний левого желудочка или митрального клапана (рис.90).
Рис.90.
Врожденная аневризма левого предсердия.
ЭхоКГ критерии
Одномерная ЭхоКГ:
- Выраженная дилатация переднезаднего размера левого предсердия.
- Нормальный ЭхоКГ-паттерн митрального клапана (может быть пролапс митрального клапана).
Двухмерная ЭхоКГ:
- Большое объемное образование, связанное с левым предсердием.
- Может быть сдавление стенки левого желудочка аневризматическим телом.
- Изменение позиции камер сердца из-за смещения их объемным образованием.
Допплер-ЭхоКГ:
- Оценка запирательной функции митрального клапана.
- Оценка легочной гемодинамики.
Дифференциальный диагноз:
- Врожденная недостаточность митрального клапана.
- Митральный стеноз.
- Рестриктивная кардиомиопатия.
- Гипертрофическая кардиомиопатия с маленькой полостью левого желудочка.
Разновидности
АДЛВ бывает двух типов:
- Тотальный (или полный). При таком пороке кровообращение между большим и малым кругом полностью прекращается, так как сообщение между легочными венами и левым предсердием отсутствует. Эта форма порока несовместима с жизнью, однако у ребенка могут присутствовать такие сопутствующие аномалии развития сердца как дефекты межпредсердной или межжелудочковой перегородки, немного компенсирующие подобное существенное нарушение гемодинамики. В таких случаях малыш может некоторое время жить. Однако в большинстве случаев без своевременной кардиохирургической коррекции тотального АДЛВ дети погибают до первого года жизни.
- Частичный. При такой аномалии одна из ветвей легочных вен сообщается с левым предсердием, и состояние гемодинамики у больного зависит от объема сброса крови.
В зависимости от уровня впадения легочных вен в левое предсердие выделяют четыре анатомических варианта АДЛВ:
- надсердечный (или супракардиальный) – наблюдается почти у 55% новорожденных и сопровождается впадением легочных вен в систему верхней полой вены;
- сердечный (или интракардиальный) – выявляется у 30% больных и сопровождается впадением легочных вен в правое предсердие или венечный синус;
- подсердечный (или субкардиальный, инфракардиальный) – наблюдается у 12% детей и сопровождается впадением легочных вен в нижнюю полую или воротную вену (иногда в лимфатический проток);
- смешанный – выявляется у 3% новорожденных и может сопровождаться различными вышеописанными вариациями впадения легочных вен.
Публикации в СМИ
Аномальный дренаж лёгочных вен (АДЛВ) — ВПС, характеризующийся впадением всех лёгочных вен в правое предсердие или магистральные вены большого круга кровообращения. Таким образом, выделяют тотальный АДЛВ либо частичный АДЛВ.
Статистические данные • Тотальный АДЛВ составляет 2,6% всех ВПС, частичный АДЛВ — 1,5% • Сочетание тотального АДЛВ с дефектом межпредсердной перегородки (ДМПП) встречают в 0,7–9% всех ВПС, частичного АДЛВ с ДМПП — в 5,7% • Чаще всего аномально дренируется правое лёгкое (97,2%) • Наиболее частый тип АДЛВ — супракардиальный (75% частичного и 45% тотального АДЛВ).
Этиология: факторы, формирующие ВПС (см. Тетрада Фалло).
Патогенез • Изменения гемодинамики при частичном АДЛВ аналогичны таковым при ДМПП (см. Дефект межпредсердной перегородки) и почти не зависят от анатомического типа порока (см. ниже) • При тотальном АДЛВ кровь из всех вен организма поступает в правое предсердие, и жизнь ребёнка невозможна без наличия сообщения между большим и малым кругами кровообращения • Чаще всего в качестве такого шунта выступает открытое овальное окно или истинный вторичный ДМПП, размер последнего определяет быстроту развития и тяжесть лёгочной гипертензии и, следовательно, прогноз при естественном течении.
Классификация анатомических типов частичного АДЛВ
• Супракардиальный тип — дренирование отдельных лёгочных вен или их общего коллектора в верхнюю полую вену или её притоки •• Правая верхняя лёгочная вена ® верхняя полая вена •• Добавочная правая верхняя лёгочная вена ® верхняя полая вена •• Левая верхняя лёгочная вена ® левая плечеголовная вена •• Левая верхняя лёгочная вена ® левая плечеголовная вена ® правое предсердие (отдельно от верхней полой вены) •• Правая верхняя лёгочная вена + правая нижняя лёгочная вена ® добавочная верхняя полая вена
• Кардиальный тип — дренирование отдельных лёгочных вен или их общего коллектора в правое предсердие или коронарный синус •• Правая верхняя лёгочная вена + правая нижняя лёгочная вена ® правое предсердие (изолированный или в сочетании с ДМПП) •• Левая верхняя лёгочная вена + левая нижняя лёгочная вена ® коронарный синус
• Субкардиальный тип — дренирование отдельных лёгочных вен или их общего коллектора в нижнюю полую вену •• Правая нижняя лёгочная вена ® нижняя полая вена •• Левая нижняя лёгочная вена ® нижняя полая вена
• Смешанный тип.
Клиническая картина и диагностика. Диагностика практически полностью основана на данных инструментальных методов, поскольку патогенез и клиника порока идентичны таковым при ДМПП, а также в связи с частым сочетанием ДМПП и АДЛВ.
Жалобы: см. Дефект межпредсердной перегородки.
Объективно: см. Дефект межпредсердной перегородки.
Инструментальная диагностика
• ЭКГ •• Признаки гипертрофии и перегрузки правых отделов •• Чаще всего ЭКГ соответствует норме.
• Рентгенография органов грудной клетки •• Усиление лёгочного рисунка •• Выбухание дуг лёгочной артерии и правых камер сердца •• При наиболее частом варианте АДЛВ (дренирование правой верхней лёгочной вены в верхнюю полую вену) определяют расширение тени нижнего сегмента верхней полой вены и корня правого лёгкого •• При супракардиальном типе тотального АДЛВ рентгенологические данные высокоспецифичны ••• При наиболее частом варианте тотального АДЛВ (дренирование общего коллектора в левую плечеголовную вену или добавочную верхнюю полую вену) тень сердца имеет конфигурацию, напоминающую цифру 8, или фигуру снежной бабы (симптом Снеллена–Альберса) ••• Тотальный АДЛВ в верхнюю полую вену приводит к аневризме центрального её участка, последняя видна в виде локального выпячивания по правому контуру тени сосудистого пучка •• Кардиальный и субкардиальный типы АДЛВ не имеют специфических признаков •• Иногда гомогенная пятнистость лёгочного рисунка напоминает картину милиарного туберкулеза лёгких •• При впадении правой нижней лёгочной вены в нижнюю полую вену в передне-задней проекции визуализируется тень аномально идущего сосуда, напоминающего формой «турецкую саблю» (симптом «турецкой сабли»).
• ЭхоКГ •• Отсутствие устьев лёгочных вен в левом предсердии •• Диагностика порока практически основана только на регистрации патологических потоков из лёгочных вен по данным исследования в режиме цветового допплеровского картирования •• ЭхоКГ — высокочувствительный метод диагностики АДЛВ, однако в большинстве случаев анатомический вариант АДЛВ диагностируют ошибочно или неполностью •• Всем взрослым и детям старшей возрастной группы проводят чреспищеводную ЭхоКГ •• В остальном — см. Дефект межпредсердной перегородки.
• Радионуклидная ангиокардиография (по методу первого прохождения или равновесная) •• Регистрация патологического потока из лёгочных вен и его количественная оценка •• Диагностика сопутствующего нарушения сократительной функции правого желудочка.
• Зондирование полостей сердца •• Давление в полостях сердца обычно в пределах нормы или незначительно повышено в правом предсердии •• При супракардиальном типе АДЛВ — повышенные pO2 и насыщение крови кислородом в верхней полой; при субкардиальном — в нижней полой вене •• Изменения насыщения кислородом крови в правых камерах сердца не специфичны для АДЛВ •• Наиболее специфичный признак — проведение зонда из нижней полой вены или правого предсердия в лёгочную вену •• Диагностика сопутствующего ДМПП — см. Дефект межпредсердной перегородки.
• Правые атриография и вентрикулография, флебография верхней полой вены, левая атриография, ангиопульмонография •• Поступление контраста, прошедшего через малый круг кровообращения, в полые вены или правое предсердие (практически единственный чувствительный метод диагностики тотального АДЛВ) •• Наиболее специфичный признак — контрастирование устья аномально дренируемой лёгочной вены при введении катетера в её просвет •• Диагностика сопутствующего ДМПП — см. Дефект межпредсердной перегородки.
Медикаментозная терапия: не разработана, в профилактике инфекционного эндокардита необходимости нет.
Хирургическое лечение
• Показания: см. Дефект межпредсердной перегородки.
• Противопоказания: см. Дефект межпредсердной перегородки.
• Методы оперативного лечения •• При частичном АДЛВ — полная анатомическая коррекция порока путём многочисленных вариантов реплантации устьев лёгочных вен, их общих коллекторов, дополнительной верхней полой вены или коронарного синуса, дренирующих лёгочные вены, в левое предсердие •• Устранение сопутствующего ДМПП — см. Дефект межпредсердной перегородки •• При кардиальном варианте частичного АДЛВ и при тотальном АДЛВ — создание искусственного или расширение естественного ДМПП с последующей изоляцией при помощи аутоперикардиальной или синтетической заплаты созданного дефекта и устьев аномально дренируемых вен в левое предсердие.
Специфические послеоперационные осложнения: синдром слабости синусового узла, усиление лёгочной венозной гипертензии при неадекватном обеспечении путей оттока из лёгочных вен.
Прогноз • При частичном АДЛВ аналогичен таковому при ДМПП (см. Дефект межпредсердной перегородки) • При тотальном АДЛВ менее 50% детей доживают до 3 мес и менее 20% — до 1 года • Пациенты, пережившие первые несколько недель, обычно имеют выраженную кардиомегалию, сердечную недостаточность и лёгочную гипертензию • Пациенты, дожившие без хирургического лечения до 1 года, обычно имеют ДМПП очень больших размеров и доживают до 10–20 лет, после чего у части из них развивается необратимая лёгочная гипертензия • Наличие обструкции на пути оттока из аномально дренируемых лёгочных вен уменьшает продолжительность жизни в 3,5–5 раз • Общая госпитальная смертность при хирургической коррекции тотального АДЛВ — 6–25% (в среднем 13%), частичного АДЛВ — 2–4% • Госпитальная летальность при радикальной коррекции субкардиального типа АДЛВ у новорождённых — 30–40%, кардиального и супракардиального — 5–10% • У 85% пациентов полная коррекция гемодинамики наступает в течение 1 года после оперативного лечения частичного АДЛВ • Отдалённая смертность после коррекции тотального АДЛВ практически полностью зависит от ближайшего (госпитального) периода, последующие летальные случаи обусловлены другими заболеваниями.
Синонимы: Аномальное впадение лёгочных вен; Аномалия соединения лёгочных вен; Полный аномальный дренаж лёгочных вен; Неполный аномальный дренаж лёгочных вен.
Сокращения. АДЛВ — аномальный дренаж лёгочных вен.
МКБ-10 • Q26 Врождённые аномалии [пороки развития] крупных вен
Как нарушается гемодинамика
Во время внутриутробного развития этот порок сердца никак себя не проявляет, так как внутрисердечное кровообращение у плода сопровождается сообщением левого и правого предсердия через открытое овальное окно. АДЛВ начинает давать о себе знать после рождения ребенка, и выраженность гемодинамических нарушений будет определяться типом и вариантом данной аномалии. Кроме этого, на выраженность симптомов порока может влиять наличие сопутствующих дефектов развития сердца и сосудов.
При тотальном АДЛВ поступающая в правое предсердие обогащенная кислородом кровь смешивается с венозной кровью. Далее некоторая ее часть попадает в правый желудочек, а другая поступает в левое предсердие через существующий дефект межпредсердной перегородки или открытое овальное окно. В таких случаях тотальный АДЛВ совместим с жизнью, так как сообщение между большим и малым кругом кровообращения не утрачивается. Подобные гемодинамические нарушения приводят к перегрузке правых камер сердца, повышению давления в легочных сосудах и понижению содержания кислорода в крови, которое приводит к кислородному голоданию органов и тканей.
При частичном АДЛВ нарушения гемодинамики происходят так же как и при межпредсердных дефектах. Тяжесть состояния больного при таком типе аномалии определяется объемом патологического артерио-венозного сброса.
«Верхом сидящий» трехстворчатый клапан
Обязательным компонентом порока является ДМЖП и смещение клапанного аппарата трехстворчатого клапана в полость левого желудочка.
ЭхоКГ критерии
Одномерная ЭхоКГ:
- Маленькие размеры правого желудочка.
- Передняя створка трикуспидального клапана пересекает МЖП во время диастолы.
- Визуализация эхосигналов от клапанного аппарата трикуспидального клапана в полости левого желудочка.
- Перерыв эхосигнала от межжелудочковой перегородки.
- Дилатация левого желудочка и левого предсердия.
Двухмерная эхоКГ:
- Гипоплазия полости правого желудочка.
- Смещение правого атриовентрикулярного кольца и подклапанного аппарата в левый желудочек.
- Непосредственная визуализация дефекта межжелудочковой перегородки.
- Выявление сопутствующих аномалий.
Допплер-эхоКГ:
- Оценка состояния легочного кровотока.
- Оценка величины систолического градиента между желудочками.
Дифференциальный диагноз:
Открытый общий атриовентрикулярный канал.
Симптомы
Признаки АДЛВ дают знать о себе сразу же после рождения ребенка. При тотальном пороке, который не сопровождается присутствием дефектов межпредсердных коммуникаций, кровообращение между малым и большим кругом становится полностью невозможным, и новорожденный быстро погибает. Спасти жизнь ребенка в таких случаях может только экстренное выполнение такой кардиохирургической операции по методу Рашкинда как баллонная эндоваскулярная атриосептостомия.
В остальных случаях выраженность клинических проявления АДЛВ обуславливается его анатомическим вариантом, размером дефектов межпредсердной перегородки и характером гемодинамических нарушений. Обычно родители детей с таким врожденным пороком замечают следующие проявления этой патологии:
- быстрая утомляемость;
- появление одышки после физической активности (кормления, плача и пр.);
- боли в области сердца (ребенок плохо спит, беспокойный, громко плачет и вытягивает ножки);
- бледность кожи;
- легкий цианоз;
- кашель;
- тошнота и рвота;
- медленная прибавка веса;
- частые ОРВИ и пневмонии.
При прощупывании пульса врач может выявить его учащенность и аритмичность. При осмотре определяется деформация грудной клетки и усиленный толчок сердца.
Легкий цианоз, возникающий на первых неделях жизни, может со временем исчезать или становится менее выраженным. Как правило, синюшность более выражена при физической нагрузке.
При выслушивании тонов сердца специфические признаки данного порока не выявляются. Могут выслушиваться:
- громкий I тон над сердцем;
- расщепление II тона с усилением легочного компонента;
- выслушиваемый III тон над верхушкой сердца (у многих больных);
- мягкий систолический шум над легочной артерией с вариабельной продолжительностью и интенсивностью.
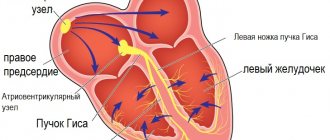
На ЭКГ определяется перегрузка правых отделов сердца – высокий вольтаж зубца Р в правых отведениях и отклонения электрической оси вправо в стандартных отведениях. На перегрузку правого предсердия указывает высокий Р зубец в правых грудных и стандартном отведениях. Нередко присутствуют признаки неполной блокады правой ножки пучка Гиса.
При наличии большого дефекта в межпредсердной перегородке ребенок может развиваться нормально и тогда в более старшем возрасте возникают жалобы на значительное снижение толерантности к физическим нагрузкам, одышку, бледность и плохое общее самочувствие. Позднее у таких детей возникают признаки правожелудочковой недостаточности.
Врожденный стеноз аорты
Рис.94.
Клапанный стеноз аорты. Постстенотическая дилатация восходящей аорты (схема). Стеноз аорты подразделяют на следующие формы:
- Клапанный врожденный стеноз (рис.94).
- Подклапанный аортальный стеноз
- А. дискретный мембранозный стеноз.
- Б. дискретный фибромышечный субаортальный стеноз.
- В. туннельный субаортальный стеноз.
- Надклапанный стеноз аорты.
- Двухстворчатый аортальный клапан со стенозированием.
В 20% случаев врожденному стенозу аорты сопутствуют ОАП, коарктация аорты, ДМЖП, стеноз легочной артерии.
Клапанный врожденный стеноз (см. аортальный клапанный стеноз)
Примечание:
если сращены все 3 полулунные створки, то определяется узкое центральное отверстие, при срастании 2-х створок (встречается чаще) отверстие в просвете аорты располагается асимметрично.
Подклапанный стеноз аорты дискретный мембранозный
Сразу под клапаном аорты расположена тонкая фиброзная мембрана (рис.95).
Рис.95.
ЭхоКГ критерии
Одномерная ЭхоКГ:
- Частичное раннесистолическое прикрытие аортального клапана.
- Систолическое трепетание аортального клапана.
- Наличие дополнительных сигналов в выходном тракте левого желудочка.
- Сужение выходного тракта левого желудочка.
- Переднесистолическое движение передней митральной створки.
- Гипертрофия левого желудочка.
- Задержка открытия митрального клапана.
Двухмерная ЭхоКГ:
- Фиброзная мембрана сразу под аортальным клапаном, пролабирующая в выходной тракт левого желудочка в диастолу (рис.96).
- Узкий выходной тракт левого желудочка.
Допплер-ЭхоКГ:
- Увеличение пикового систолического потока в восходящей аорте свыше 1,5м/с.
- Наличие систолического градиента (свыше 5 мм рт.ст.).
Рис.96.
Подклапанный перимембранозный стеноз аорты.
Дифференциальный диагноз:
- Асимметричная гипертрофическая кардиомиопатия с обструкцией выходного тракта левого желудочка (идиопатический гипертрофический субаортальный стеноз): при дискретном стенозе обычно наблюдается частичное раннесистолическое прикрытие аортального клапана (в среднем через 0,05 с), при ИГСС — среднесистолическое (в среднем через 0,14 с от момента открытия аортального клапана)
Подклапанный стеноз аорты дискретный фибромышечный
Образован фиброзномышечным кольцом, обычно локализуется более дистально от аортального клапана, чем при дискретном мембранозном стенозе, приблизительно 1 см и более.
Диагностика
Одним из методов, помогающих обнаружить и верифицировать АДЛВ, является УЗИ сердца.
Впервые АДЛВ может выявляться у плода при УЗ-обследовании в третьем триместре беременности.
Для уточнения всех данных о таком врожденном пороке сердца назначаются следующие инструментальные методики исследования:
- рентгенография;
- ЭКГ;
- Эхо-КГ (взрослым и детям старшего возраста назначается чреспищеводное Эхо-КГ);
- МРТ;
- зондирование камер сердца и ангиокардиография.
Лечение
Единственным способом устранения АДЛВ является его кардиохирургическая коррекция. До операции ребенку рекомендуется ограничение физической активности и назначаются лекарственные средства для профилактики острой сердечной недостаточности (мочегонные, сердечные гликозиды). Родители ребенка должны знать о том, что даже плач или температурный дискомфорт способны существенно ухудшать самочувствие при таком пороке сердца. Если ребенок уже взрослый, то они должны постоянно следить за его досугом – он не должен бегать, поднимать тяжести и переутомляться.
Методы хирургической коррекции
Способ выполнения кардиохирургической коррекции при АДЛВ определяется типом и вариантом порока.
При тотальном дренаже находящемуся в критическом состоянии ребенку до 3 месяцев может выполняться паллиативная операция, заключающаяся в увеличении межпредсердного сообщения при помощи проведения баллонной атриосептомии по методике Рашкинда. Такая коррекция способствует поступлению крови в левое предсердие и восстановлению кровообращения в большом круге.
Для радикального устранения АДЛВ проводятся вмешательства направленные на создание широкого анастомоза между левым предсердием и легочными венами, прекращение патологического дренажа легочных вен с другими венозными сосудами и устранение дефекта межпредсердной перегородки. Такие вмешательства предпочтительней выполнять в раннем возрасте. Методика радикальной коррекции выбирается в зависимости от анатомического варианта АДЛВ.
Корректирующие вмешательства являются достаточно эффективными, однако, несмотря на развитие современной кардиохирургии, процент летальных исходов, наступающих во время операции или в послеоперационном периоде, остается высоким. Результат радикальной коррекции во многом зависит от мастерства кардиохирурга, технического оснащения, типа и варианта порока. Кроме этого, наиболее высокий риск наступления смерти наблюдается среди новорожденных и детей раннего возраста, страдающих от выраженной легочной гипертензии. Чаще всего такое проявление порока наблюдается среди больных с субкардиальным вариантом аномалии.
Отдаленные результаты среди выживших после радикальной коррекции АДЛВ детей вполне удовлетворительные. Только у некоторых пациентов возможно развитие слабости синусового узла и легочной гипертензии, плохо поддающихся медикаментозной терапии.
Осложнения
- Обструкция анастомозов (5-10% случаев)
Полный аномальный дренаж легочных вен в правое предсердие (II тип, кардиальный), сочетающийся с дефектом межпредсердной перегородки. Рентгенография грудной клетки в прямой проекции. Увеличение правых отделов сердца и увеличение васкуляризации центральных отделов легкого. МРТ с контрастным усилением грудной клетки. Частичный аномальный дренаж легочных вен, левая легочная вена впадает через вертикальную вену (стрелка) в безымянную вену (*).
Прогноз
Удачно выполненная радикальная кардиохирургическая коррекция АДЛВ существенно улучшает прогнозы исхода этого порока сердца. Однако риск летального исхода во время или после операции пока остается высоким.
При тотальной форме АДЛВ и отсутствии экстренной кардиохирургической коррекции в возрасте до года погибает около 80% детей. Если аномальный дренаж легочных вен является частичным, то больные могут доживать до 20-30 лет. При отсутствии хирургического лечения такие пациенты умирают от сердечной недостаточности или легочных инфекций.
Аномальный дренаж легочных вен относится к редким врожденным порокам сердца и всегда нуждается в проведении кардиохирургической коррекции. В некоторых случаях состояние новорожденного ребенка из-за существенных гемодинамических нарушений становится критическим, и такие операции выполняются в экстренном порядке. После проведения удачной радикальной кардиохирургической коррекции состояние больного значительно улучшается, и прогноз исхода заболевания становятся благоприятным.
Клинические проявления
Типичные симптомы:
Обструкция легочных вен:
- острая ургентная ситуация в первые несколько часов или дней жизни
- Цианоз
- Одышка
- Легочная гипертензия.
Без обструкции легочных вен:
- Увеличение легочного кровотока
- Легочная гипертензия
- Тахипноэ
- Признаки сердечной недостаточности
- Дистрофия.
Незначительное увеличение давления в легочных артериях может вызывать только минимальное количество симптомов; цианоз может отсутствовать или быть нерезко выражен.