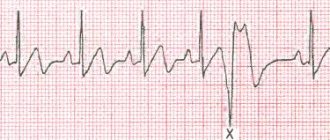
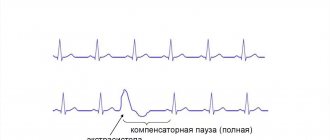
В латинском языке существует слово compensatum, что в переводе означает «уравновешивать». Компенсаторная пауза — это термин, который характеризует диастолическую паузу, наступающую после нарушения сердечного ритма. По времени такая пауза удлиненная. Ее длительность приравнивается к двум обычным для сердечного ритма паузам.
Наступает компенсаторная пауза после желудочковой экстрасистолы и длится до очередного самостоятельного сокращения.
Причины возникновения компенсаторной паузы
После экстрасистолы желудочка наблюдается рефрактерный период, характеризующийся тем, что желудочек не реагирует на следующий импульс, исходящий из синуса. Это приводит к тому, что желудочек сокращается не после первого, а после второго импульса синуса. Бывают случаи, когда сердцебиение очень редкое, конец рефрактерного периода наблюдается после экстрасистолы и до очередного импульса синуса. Такие изменения в ритме сердца могут привести к отсутствию компенсаторной паузы.
Сердечный ритм бывает номотопный и гетеротопный. Их одновременное наличие у человека называется парасистолией, которая нередко может быть причиной появления компенсаторных пауз.
Еще одной причиной их появления может стать экстрасистолическая аллоритмия, которая представляет собой серьезную патологию, связанную с нарушениями функции кровообращения и сердечного ритма.
Синдром удлиненного и укороченного интервала QT в клинической практике
Среди причин удлинения и укорочения интервала QT выделяют врожденные и приобретенные факторы. Основной причиной заболевания является наследственная каналопатия, обусловленная мутацией ряда генов, кодирующих белки трансмембранных калиевых и натриевых ионных каналов. Синдром удлиненного интервала (СУДИ) QT имеет достаточно долгую историю изучения, насчитывающую более 100 лет. Возможно, первым описанием наследственного СУДИ QT является работа T. Messner и соавт., опубликованная в 1856 г. [1]. Мощным толчком для изучения электрофизиологии сердца явилось внедрение в медицинскую практику методики регистрации ЭКГ, разработанной нидерландским физиологом В. Эйндховеном в 1903 г. Но только в 1957 г. A. Jervell и F. Lange-Nielsen диагностировали клинико-электрокардиографический «синдром длинного QT» у четырех членов одной семьи, страдавших врожденной невральной глухотой, частыми приступами потери сознания и имевших стойкое удлинение интервала QT на ЭКГ, положивший начало современному этапу изучения СУДИ QT. Вскоре P. Romano (1963) и D. Ward (1964) представили наблюдения аналогичного синдрома, но без врожденной глухоты. При этом у родственников больных также обнаруживалось удлинение интервала QT, но приступов потери сознания не отмечалось [1]. Аритмогенный потенциал укороченного интервала QT был впервые отмечен I. Gussak и соавт. в 2000 г. при описании клинического случая внезапной сердечной смерти одной молодой женщины и семьи, в которой наблюдалось несколько случаев раннего возникновения фибрилляции предсердий (ФП) у ее членов. Ни у кого из обследованных не имелось структурных изменений в сердце, но отмечалось отчетливое уменьшение продолжительности интервала QT на ЭКГ (QTC варьировал от 248 до 300 мс) [2].
Электрофизиология сердечной клетки и связь с продолжительностью интервала QT Интервал QT ЭКГ отражает суммарную продолжительность деполяризации и реполяризации кардиомиоцитов желудочков. На уровне отдельной клетки интервал QT соответствует продолжительности трансмембранного потенциала действия (ТМПД), обусловленного трансмембранным током ионов по натриевым, кальциевым и калиевым каналам. Известно пять последовательных фаз ТМПД: Фаза 0 (деполяризация) характеризуется массивным током ионов натрия внутрь клетки (INa). Фаза 1 (начальная быстрая реполяризация) характеризуется прекращением тока ионов натрия и преходящим быстрым током ионов калия из клетки (It0). Фаза 2 (плато) характеризуется медленным током ионов кальция внутрь клетки через кальциевые каналы L-типа (ICa-L) и продолжающимся истечением ионов калия наружу (IK). Фаза 3 (конечная быстрая реполяризация) характеризуется током ионов калия наружу клетки (IKr, IKs) c формированием трансмембранного потенциала покоя (ТМПП). Фаза 4 (деполяризация) характеризуется поддержанием ТМПП за счет активного поступления ионов калия внутрь клетки (IK1). На микроструктурном уровне трансмембранные ионные каналы представляют собой сложные структурные образования, состоящие из специфических белковых комплексов. Дисфункция этих белковых каналов может обусловливать ускорение или замедление трансмембранных ионных потоков в различные фазы ТМПД, что может приводить к удлинению или укорочению продолжительности ТМПД и интервала QT. Основной причиной дисфункции трансмембранных ионных каналов является мутация генов, кодирующих их белки. Мутации могут затрагивать все типы каналов, а также их сочетания, что обусловливает существование большого количества клинических форм синдрома удлиненного и укороченного интервала QT. В настоящее время структура и генетика трансмембранных ионных каналов изучены в полной мере, что делает доступной медикаментозную коррекцию их нарушений. Подробная литература по данному вопросу представлена в обзоре S. Nachimuthu и соавт. [3].
Методика измерения и оценки интервала QT Интервал QT измеряется на ЭКГ от начала зубца Q (в случае его отсутствия – от начала зубца R) до конца зубца Т. Несмотря на кажущуюся простоту, измерение и оценка интервала QT представляют собой достаточно трудную задачу и являются одним из наиболее сложных моментов при анализе ЭКГ. Наибольшие сложности составляет: 1) определение начала комплекса QRS и окончания зубца Т; 2) выбор отведений, в которых предпочтительно измерять интервал QT; 3) необходимость корректировки продолжительности интервала QT для ЧСС, пола и продолжительности комплекса QRS [4].
По данным ряда исследований, у здоровых людей в разных отведениях продолжительность интервала QT может варьировать в пределах 50–65 мс. Согласно Рекомендациям по стандартизации и интерпретации ЭКГ Американской сердечной ассоциации 2009 г. [4], при измерении интервала QT в отдельных отведениях для анализа следует выбирать отведение с наибольшим интервалом QT (обычно отведение V2 или V3). В большинстве случаев окончание зубца Т определяется в момент возврата конечной части зубца Т на изолинию. В случае «двугорбого» зубца Т с одинаковыми по амплитуде вершинами окончание зубца Т рекомендуют определять по окончанию второй вершины [5]. Если зубцы Т и U накладываются друг на друга, то интервал QT рекомендуется измерять в отведениях без зубца U (часто это отведения aVR или aVL) или определять окончание зубца Т в месте пересечения изолинии с линией, проведенной по касательной вдоль нисходящей части зубца Т (необходимо учитывать, что последний способ может занижать значения интервала QT) [4] (рис. 1). При ручном способе измерения продолжительность интервала QT рекомендуется определять как среднее значение нескольких измерений (как минимум 3–5 сердечных цикла) [5]. В последние годы во многих современных электрокардиографах появилась возможность автоматизированного анализа ЭКГ, включая определение продолжительности интервала QT. Используемые при автоматическом анализе суперпозиция и усреднение нескольких отведений позволяют более точно определять начало и конец интервала QT, вследствие чего автоматически измеренный интервал QT часто длиннее, чем интервал QT при ручном способе измерения. Поэтому в случае выявления удлинения интервала QT при автоматизированном анализе рекомендуется перепроверять результаты ручным способом [4]. Известно, что продолжительность интервала QT имеет отчетливую взаимосвязь с ЧСС (интервалом RR): при уменьшении ЧСС интервал QT увеличивается, а при увеличении ЧСС – уменьшается. Данная особенность свидетельствует о необходимости коррекции продолжительности интервала QT в зависимости от ЧСС. Для этой цели предложен ряд формул, использующих экспоненциальный, линейный или логарифмический методы [5]. Следует отметить, что в диапазоне ЧСС от 60 до 90 уд./мин. большинство формул обеспечивают сопоставимые результаты коррекции и являются взаимозаменяемыми.
Одна из первых формул для коррекции интервала QT в зависимости от ЧСС была предложена H.C. Bazett в 1920 г., и до настоящего времени она остается основной формулой для определения корригированного интервала QT (QTc) как в научных исследованиях, так и в клинической практике. Большинство электрокардиографов при автоматизированном анализе используют именно формулу Bazett. В формуле Bazett используется экспоненциальный метод определения QTc (QTc=QT/RR1/2). К недостаткам формулы Bazett можно отнести возможность ошибочной коррекции при слишком высокой или низкой ЧСС. Формулы, использующие линейный метод коррекции (Framingham, Hodges, Rautaharju), позволяют уменьшить ошибки экспоненциального метода и могут использоваться как при высокой, так и низкой ЧСС. Наиболее известной из них является формула Framingham (QTc=QT + 0,154 х (1 – RR)), а наиболее точной, но более сложной – формула Rautaharju. Подробно с различными методами коррекции интервала QT для ЧСС можно ознакомиться в обзоре I. Goldenberg и соавт. [5].
Следует отметить, что ручное определение QTc для каждого индивидуального пациента – достаточно трудоемкий процесс, отнимающий много времени. Поэтому в клинической практике для быстрого определения пациентов группы риска возникновения тахикардии torsades de pointes (TdP) можно использовать номограмму зависимости QT от ЧСС [3]. Поскольку интервал QT может увеличиваться при нарушениях внутрижелудочкового проведения, для оценки продолжительности реполяризации у больных с блокадами ножек пучка Гиса рекомендуется использовать либо продолжительность интервала JT (от начала сегмента ST до конца зубца Т), либо формулы коррекции, учитывающие одновременно ЧСС и продолжительность комплекса QRS [4]. К сожалению, эти методы анализа до настоящего времени не имеют общепризнанных нормативов и весьма ограниченно используются в клинической практике.
Интервал QT: удлиненный, нормальный, укороченный В 2009 г. S. Viskin [6], используя данные популяционных и генетических исследований, разработал «шкалу QT», ранжирующую весь непрерывный спектр интервалов QT от очень коротких до очень длинных, раздельно для мужчин и женщин. В соответствии с данной шкалой нормальной продолжительностью интервала QT считаются значения QTc 360–389 мс для мужчин и 370–399 мс – для женщин; при QTc, равном 390–449 мс для мужчин и 400–459 мс – для женщин, интервал QT расценивался как возможно удлиненный; при QTc, равном 450–469 мс для мужчин и 460–479 мс – для женщин, как удлиненный; при QTc, равном или больше 470 мс для мужчин и 480 мс – для женщин, как выраженно удлиненный; при QTc, равном 359–329 мс для мужчин и 369–339 мс – для женщин, как укороченный, при QTc, равном или меньше 330 мс для мужчин и 340 мс – для женщин, как выраженно укороченный. Одними из первых и наиболее известных критериев диагностики СУДИ QT являются критерии P.J. Schwartz и соавт. 1985 г., которые впоследствии неоднократно дополнялись и обновлялись (табл. 1). В соответствии с этими критериями лица, набирающие 1 балл, имеют низкую вероятность СУДИ QT, от 2 до 3 баллов – промежуточную вероятность, 4 балла и более – высокую вероятность СУДИ QT [7]. В 2011 г. M.H Gollob и соавт. [2] предложили критерии диагностики синдрома укороченного интервала (СУКИ) QT, построенные на тех же принципах, что и критерии СУДИ QT (табл. 2). В соответствии с этими критериями при общем количестве баллов 4 или более определяется высокая вероятность СУКИ QT, при наличии 2 баллов или менее – низкая вероятность, в случае, если сумма баллов составляет 3 балла, то вероятность СУКИ QT оценивается как промежуточная.
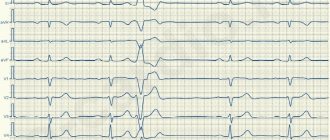
Cиндром удлиненного интервала QT Увеличение продолжительности реполяризации часто приводит к возникновению на мембране кардиомиоцитов желудочков интенсивных осцилляций, носящих название потенциалов ранней постдеполяризации, что в сочетании с выраженной гетерогенностью продолжительности потенциалов действия обусловливает возникновение в миокарде желудочков очагов повторного возбуждения и желудочковой тахикардии [3]. Наиболее характерным клиническим проявлением СУДИ QT является полиморфная желудочковая тахикардия torsades de pointes (TdP) (двунаправленная, «пируэтная» тахикардия). TdP характеризуется выраженным удлинением интервала QT в последнем предшествующем тахикардии синусовом сокращении, прогрессирующим изменением полярности комплексов QRS, визуально имитирующим их вращение вокруг изолинии, постоянным изменением амплитуды комплексов QRS, высокой ЧСС от 150 до 300 импульсов в мин и выраженной нерегулярностью интервалов RR (рис. 2). Для TdP характерно возникновение приступа после паузы, обусловленной брадикардией или экстрасистолией. Типичной для TdP является так называемая SLS (short-long-short) последовательность, характеризующаяся начальной суправентрикулярной экстрасистолой, приводящей к укорочению интервала RR (short-цикл), последующей длинной постэкстрасистолической паузой перед очередным синусовым комплексом (long-цикл) и повторной желудочковой экстрасистолой (short-цикл), являющейся началом пароксизма TdP. У больных СУДИ QT возникновение TdP нередко провоцируется интенсивной адренергической стимуляцией [8]. Приступы TdP у больных СУДИ QT обычно протекают кратковременно, купируются спонтанно и поэтому длительное время могут оставаться незамеченными. Однако эти приступы имеют тенденцию группироваться в повторяющиеся последовательности с короткими межприступными интервалами, обусловливая возникновение сердцебиений, головокружений, обмороков, предобморочных состояний и внезапной смерти вследствие фибрилляции желудочков (ФЖ).
В последние десятилетия достигнуты значительные успехи в определении генетических предпосылок возникновения СУДИ QT. Идентифицированы мутации в десяти генах, обусловливающие удлинение интервала QT. Тем не менее, подавляющее большинство клинически значимых случаев СУДИ QT связаны с мутациями в трех генах, проявляющимися тремя генетическими подтипами (LQT1, LQT2 и LQT3), которые имеют характерные клинические особенности и характеризуются определенной морфологией ЭКГ [9]. Для LQT1 характерны широкие волны Т на ЭКГ покоя, отсутствие паузы перед началом тахиаритмии, отсутствие укорочения интервала QT при физической нагрузке, высокая эффективность β-адреноблокаторов (БАБ). Развитие тахиаритмии при LQT1 провоцируется физическим и психическим стрессом, плаванием, нырянием. LQT2 отличается низкоамплитудными, зазубренными зубцами Т на ЭКГ покоя, наличием паузы перед началом тахиаритмии, нормальным укорочением интервала QT при физической нагрузке и меньшей, по сравнению с LQT1, эффективностью БАБ. Развитие тахиаритмии при LQT2 провоцируется физическим и психическим стрессом, внезапными громкими звуками. LQT3 характеризуется удлиненным изоэлектричным сегментом ST, узкими и высокими волнами Т на ЭКГ покоя, чрезмерным укорочением интервала QT при физической нагрузке. Эффективность БАБ не определена. Тахиаритмия чаще возникает в покое, во время сна.
Большинство случаев СУДИ QT представлены аутосомно-доминантными формами c различной пенетрантностью. Мутации чаще выявляются у лиц, родители которых сами являются носителями мутантных генов. У женщин риск обмороков и внезапной смерти снижается в период беременности, но вновь повышается в послеродовой период. Обмороки и внезапная смерть отмечаются преимущественно у детей и подростков и не характерны для лиц старше 40 лет [9]. Частота мутаций генов, ответственных за удлинение интервала QT, составляет примерно 1 на 2 тыс. человек, но частота манифестных форм существенно ниже, поскольку у большинства носителей дефектных генов симптомы отсутствуют в течение всей жизни.
Диагностика наследственного СУДИ QT основывается на выявлении характерных изменений ЭКГ, анализе клинических данных и семейного анамнеза в соответствии с критериями P.J. Schwartz и соавт. [7], а также на исключении приобретенных причин удлинения интервала QT. Заключительным этапом диагностики является генетическое тестирование, позволяющее выявить пораженный ген у 70–90% лиц с признаками наследственного СУДИ QT. Несмотря на свою высокую диагностическую значимость, генетическое тестирование не является панацеей и может давать как ложноположительные, так и ложноотрицательные результаты. Генетическое тестирование показано, главным образом, в двух случаях: 1) когда диагноз является вероятным и клинические данные указывают на поражение конкретного гена; 2) в семьях, в которых имеется пробанд с ранее установленным генетическим дефектом. В обоих случаях генетическое тестирование необходимо для уточнения диагноза, определения прогноза и выбора тактики долговременного лечения [9]. В последние годы было идентифицировано большое количество ненаследственных факторов, вызывающих удлинение интервала QT и TdP, в первую очередь это лекарственные средства, среди которых следует отметить антиаритмики класса Ia (хинидин, прокаинамид, дизопирамид) и класса III (дофетилид, ибутилид, соталол), нейролептики (галоперидол, дроперидол, тиоридазин, хлорпромазин), антидепрессанты (амитриптилин, дезипрамин, имипрамин, мапротилин, доксепин, флуоксетин), антибиотики группы хинолонов (левофлоксацин, моксифлоксацин) и макролидов (эритромицин, кларитромицин), противомалярийные средства (хинидин), противопротозойные средства (пентамидин), противогрибковые средства (азольная группа) и метадон [3]. В то же время прогностическое значение приобретенного удлинения интервала QT изучено недостаточно. Отмечается, что взаимосвязь между механизмом действия лекарственного агента и клиническими проявлениями СУДИ QT является нестрогой. В некоторых случаях даже выраженное удлинение интервала QT редко сопровождается развитием TdP (например, при использовании амиодарона), а в других – незначительное удлинение интервала QT может вызывать TdP [3].
Предполагается, что вероятность развития TdP увеличивается при сочетании нескольких факторов риска. К основным факторам риска приобретенного СУДИ QT относят электролитные нарушения (гипокалиемия, гипомагнезиемия, гипокальциемия), применение лекарственных средств, удлиняющих интервал QT, диуретиков и сердечных гликозидов, наличие сопутствующих заболеваний (печеночная и почечная недостаточность, брадикардия, сердечная недостаточность, гипертрофия левого желудочка, инфаркт миокарда, субарахноидальная геморрагия и другие формы поражения центральной нервной системы), диету с жидкими протеинами и другие формы голодания [3, 11]. Известно, что от 5 до 20% больных с лекарственно обусловленным TdP имеют мутации в генах, вызывающих СУДИ QT. В обычном состоянии эти пациенты характеризуются нормальным или пограничным QTc, но имеют склонность к удлинению интервала QT и развитию TdP при употреблении некоторых лекарств, под воздействием стресса или других факторов риска [3].
Синдром укороченного интервала QT СУКИ QT характеризуется наследственно обусловленным укорочением интервала QT, сопровождающимся высокой частотой возникновения ФП (24%) в виде постоянной или пароксизмальной форм, частыми обмороками, развитием полиморфной желудочковой тахикардии, ФЖ, остановки сердца и внезапной смерти. Могут также отмечаться депрессия сегмента PR, высокие в виде пиков зубцы Т без горизонтального уплощения сегмента ST, нарушения укорочения сегмента ST при увеличении ЧСС, парадоксальное укорочение интервала QT при брадикардии. ФП и ФЖ у больных СУКИ QT легко провоцируются программируемой электрокардиостимуляцией [11]. Электрофизиологической основой укорочения интервала QT является уменьшение продолжительности ТМПД вследствие снижения потоков деполяризации (INa, ICa), увеличения потоков реполяризации (Ito, IK1, IK-ATP, IACh, IKr, IKs) или их сочетания. Экспериментальные исследования показывают, что укорочение ТМПД при СУКИ QT отличается выраженной неоднородностью, сопровождающейся трансмуральной дисперсией реполяризации, являющейся субстратом для развития аритмий по механизму «reentry» [12].
В настоящее время описано пять генетических подтипов синдрома укороченного интервала QT (SQT1–5) с аутосомно-доминатной передачей, связанных с мутациями в пяти различных генах, кодирующих калиевые и кальциевые трансмембранные ионные каналы (IKr, IKs, IK1, ICa). Для SQT1 и SQT3–5 доказаны семейные случаи, SQT2 описан на примере единственного спорадического случая [12]. При SQT1 провоцирующим фактором нарушений сердечного ритма обычно является физическая нагрузка и громкие звуки, при SQT3 – внезапное ночное пробуждение [11]. Кроме наследственных форм укорочение интервала QT в клинической практике наиболее часто встречается при гиперкальциемии, обусловленной гиперпаратиреоидизмом, заболеваниями почек, остеолитическими формами рака, приемом тиазидных диуретиков, лития и витамина D. Среди других клинических ситуаций, ассоциирующихся с вторичным укорочение интервала QT, следует отметить синдром Бругада, синдром хронической усталости, гипертермию, синдром ранней реполяризации желудочков, ацидоз, влияние дигиталиса, атропина и катехоламинов [12, 13]. Вторичное укорочение интервала QT увеличивает риск аритмогенных событий [13].
Лечение Отсутствие многоцентровых рандомизированных контролируемых испытаний терапии синдромов удлиненного и укороченного интервала QT отражает как относительную редкость этих заболеваний, так и большое количество генетических типов, имеющих существенные различия по клиническим особенностям и тяжести течения. Пациенты с очень низким риском внезапной смерти (например, носители мутаций пожилого возраста с нормальной продолжительностью интервала QT) обычно не требуют лечения, но должны избегать приема лекарств, удлиняющих интервал QT [9].
Основу лечения пациентов с СУДИ QT составляют БАБ и имплантируемые кардиовертеры-дефибрилляторы (ИКД) [9]. Основным лечебным эффектом БАБ является препятствие учащению ЧСС при физической нагрузке и стрессе. Лечение БАБ больных с СУДИ QT проводится по общепринятым схемам с учетом всех возможных противопоказаний. Имеются данные, что терапия БАБ более эффективна у больных с LQT1, чем у больных с LQT2 и LQT3 [9]. Сопоставимый с БАБ лечебный эффект у больных СУДИ QT достигается при левосторонней шейной симпатэктомии (ЛШС) (ганглионэктомия звездчатого узла). Учитывая, что ЛШС является инвазивной операцией, она показана больным, имеющим противопоказания к БАБ [14].
ИКД широко применяются для профилактики жизнеугрожающих аритмий и внезапной смерти у больных с СУДИ QT. Основным контингентом для лечения ИКД являются: 1) лица, у которых симптомы развиваются в раннем возрасте до начала пубертатного периода; 2) больные с выраженно удлиненным интервалом QT (QTc>500 мс); 3) больные с повторными аритмогенными синкопе, возникающими на фоне лечения БАБ. Вопрос о более агрессивной тактике имплантации ИКД всем носителям мутантных генов, выявленным при семейном генетическом скрининге, остается дискуссионным [9]. Совместные рекомендации Северо-американского и Европейского обществ кардиологов по лечению и профилактике внезапной смерти при СУДИ QT представлены в таблице 3. Имплантация ИКД настоятельно рекомендуется всем больным с СУКИ QT для вторичной профилактики внезапной сердечной смерти, исключая случаи, когда имеются абсолютные противопоказания или отказ пациента. В то же время, использование ИКД для первичной профилактики внезапной смерти достоверно не доказано. Также весьма ограничены данные относительно фармакологического лечения СУКИ QT, относящиеся в основном к лечению SQT1. Одним из препаратов, подающих большие надежды, является гидрохинон, показавший устойчивое удлинение интервала QT и уменьшение эпизодов желудочковой тахикардии [12].
Заключение Удлинение и укорочение интервала QT нередко встречается в клинической практике и может являться причиной внезапной смерти больных. Своевременная диагностика позволяет выбрать оптимальную тактику лечения и действительно спасти жизнь таким пациентам. Поэтому знание методов диагностики и лечения синдромов удлиненного и укороченного интервала QT необходимо врачам всех специальностей в их повседневной работе.
Литература 1. Школьникова М.А. Первичный, наследственный синдром удлиненного интервала QT // Синдром удлиненного интервала QT / Под ред. М.А. Школьниковой. М.: Медпрактика, 2001. С. 9–45. 2. Gollob M.H., Redpath C.J., Roberts J.D. The Short QT Syndrome: Proposed Diagnostic Criteria // J. Am. Coll. Cardiol. 2011. Vol. 57. P. 802–812. 3. Nachimuthu S., Assar M.D., Schussler J.M. Drug-induced QT Interval Prolongation // Ther. Adv. in Drug Safe. 2012. Vol.3(5). P.241–253. 4. Rautaharju P.M., Surawicz B., Gettes L.S. AHA/ACCF/HRS Recommendations for the Standardization and Interpretation of the Electrocardiogram: Part IV: The ST Segment, T and U Waves, and the QT Interval: A Scientific Statement From the American Heart Association Electrocardiography and Arrhythmias Committee, Council on Clinical Cardiology; the American College of Cardiology Foundation; and the Heart Rhythm Society: Endorsed by the International Society for Computerized Electrocardiology // Circulation. 2009. Vol. 119. P.e241–e250. 5. Goldenberg I., Moss A.J., Zareba W. QT Interval: How to Measure It and What Is «Normal» // J. Cardiovasc. Electrophysiol. Vol.17. P. 333–336. 6. Viskin S. The QT interval: Too long, too short or just right // Heart Rhythm. 2009. Vol. 6. №.5. P. 711–715. 7. Schwartz P.J. et al. Diagnostic criteria for the long QT syndrome. An update // Circulation. 1993. Vol. 88. P. 782–784. 8. Khan L.A. Long QT Syndrome: Diagnosis and Management // Amer. Heart J. 2002. Vol.143(1) 9. Roden D.M. Long-QT Syndrome // N. Engl. J. Med. 2008. Vol. 358. P.169–176. 10. Roden D.M., Viswanathan P.C. Genetics of acquired long QT syndrome // J. Clin. Invest. 2005. Vol. 115. P. 2025–2032. 11. Morita H., Wu J., Zipes D.P. The QT syndromes: long and short // Lancet. 2008. Vol. 372. P. 750–763. 12. Patel C., Yan G.-X., Antzelevitch C. Short QT Syndrome: From Bench to Bedside // Circ. Arrhythm. Electrophysiol. 2010. Vol.3. P.401–408. 13. Bjerregaard P., Nallapaneni H., Gussak I. Short QT interval in clinical practice // Journal of Electrocardiology. 2010. Vol. 43. P. 390–395. 14. The Cardiac Society of Australia and New Zealand (CSANZ). Guidelines for the diagnosis and management of Familial Long QT Syndrome 2011. https://www.csanz.edu.au/documents/guidelines/clinical_practice/Familial_Long_QT_Syndrome.pdf
Виды компенсаторных пауз
Компенсаторные паузы бывают двух видов:
- Полная.
- Неполная.
Полная компенсаторная пауза после желудочковых экстрасистол появляется как следствие того, что не наблюдается прохождения внеочередного импульса сквозь атриовентрикулярный узел. Заряд синусового узла при этом не уничтожается.
Следующий синусовый импульс доходит до желудочков в то время, когда в них происходит внеочередное сокращение. Этот период называется рефрактерным. Происходит ответ желудочков лишь на очередной синусовый импульс, что по времени равно двум сердечным циклам.
Это значит, что время, обозначающее интервалы до и после экстрасистол, приравнивается к двум нормальным интервалам R – R.
Неполная компенсаторная пауза характеризуется появлением возбуждения в эктопическом очаге. Импульс доходит до ретроградного синусового узла, после чего происходит уничтожение образовавшегося в нем заряда. В этот момент образуется очередной нормальный синусовый импульс. Это означает, что промежуток, появившийся после экстрасистолы, приравнивается к одному обычному интервалу R – R и времени, за которое экстрасистолический импульс проходит от эктопического очага до синусового узла. То есть такая ситуация говорит о том, что расстояние от синусового узла до эктопического очага влияет на паузу после экстрасистолы.
Расположение эктопического очага и атриовентрикулярного узла влияет на интервал предсердной экстрасистолы P – Q. Нахождение узла недалеко от очага значительно укорачивает P – Q.
Классификация
Синусовая
Предсердная
- предсердная
- нижнепредсердная
- левопредсердная
Из АВ-соединения
- с одновременным возбуждением предсердий и желудочков
- с предшествующим возбуждением предсердий и желудочков:
- ретроградная блокада 1 степени
- с полной ретроградной блокадой
- с полной антероградной блокадой
Желудочковая
- перегородочная
- париетальная
Чем подобное явление грозит здоровью человека?
Компенсаторная пауза — повод для волнения, и ее появление всегда негативно влияет на насосную функцию сердца. Такое состояние может появиться после эмоционального возбуждения, большого количества выпитого кофе, злоупотребления никотином, нарушения сна.
Особую опасность представляют собой компенсаторные паузы, возникающие в результате сигналов в районе ишемических и инфарктных зон. Такие случаи, судя по статистическим данным, нередко приводят к развитию спонтанной фибрилляции желудочков, что, в свою очередь, заканчивается смертью пациента.
Компенсаторная пауза может быть свидетельством серьезных заболеваний:
- порока сердца,
- миокардита,
- ишемической болезни,
- инфаркта миокарда,
- артериальной гипертензии,
- сердечной недостаточности хронического течения.
Лечение
Для того, чтобы избавиться от компенсаторных пауз, важно излечить основное заболевание, которое их спровоцировало. Для этого применяются бета-адреноблокаторы, седативные препараты и транквилизаторы, с помощью которых уменьшаются экстрасистолы. Отлично справляются с аритмией препараты, основанные на хинидине.
Кроме этого иногда необходимо прибегнуть к помощи психотерапевта.