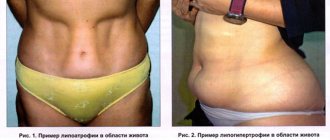
Общие сведения
Углеводный обмен во многом определяет общее состояние метаболизма. Углеводы принимают участие практически во всех видах обмена веществ: белков (гликопротеины), нуклеиновых кислот (рибоза/дезоксирибоза), липидов (гликолипидов), нуклеотидов (АТФ, АМФ, АДФ), нуклеозидов (аденозин), ионов. Простые и сложные углеводы являются одним из основных источников энергии, обеспечивающих жизнедеятельность организма, и относятся к обязательному компоненту рациона питания. Расстройства углеводного обмена объединяют в несколько типовых форм (групп) патологии: гипо- и гипергликемия, агликогенозы, гликогенозы, гексоз‑ и пентоземии.
Гипергликемия представляет собой клинический симптом, для которого характерно повышение глюкозы в крови (в плазме крови) более 6,5 ммоль/л натощак и более 8,9 ммоль/л в любое время суток). Код гипергликемии по МКБ-10: R73.9 — Гипергликемия неуточненная. По показателю содержания глюкозы (GLU) различают слабо выраженное состояние 6,7-11,1. Характеризуется значительным и стойким увеличением ГПК до уровня 10,5-11,0 ммоль/л и сочетается с расстройством жизнедеятельности организма. Такого рода гипергликемия определяется как гипергликемический синдром. Наиболее тяжелым проявлением является гипергликемический криз (ГПК> 16,5).
Предметом статьи является ранние нарушения углеводного обмена, которые некоторые авторы определяют как «предиабет». К ранним нарушениям углеводного обмена принято относить состояния нарушенной толерантности к глюкозе (НТГ) и нарушенную гликемию натощак (НГН) или сочетание этих состояний (НТГ+НГН). Принято считать, что предиабет сопровождается высоким риском развития СД2-типа, но в ряде случаев предиабет в СД2Т не конвертируется и оценивается рядом авторов как самостоятельный фактор риска развития сердечно-сосудистых заболеваний. По сути, это пограничные нарушения углеводного обмена, предшествующие развитию сахарного диабета, т.е. гипергликемия при значениях глюкозы, недостаточных для диагноза СД.
Установлено, что при НГН инсулинорезистентность печени и гиперпродукция глюкозы печенью более выражена чем при изолированной НТГ, подтверждением чего является более высокая выработка печенью глюкозы и показатель индекса инсулинорезистентности. Для НТГ характерна периферическая инсулинорезистентность, подтверждением чего являются более низкие показатели индекса чувствительности к инсулину. В случаях комбинации этих состояний (НТГ+НГН) нарушена первая фаза секреции инсулина.
Согласно литературным данным общемировая распространенность НТГ у лиц в возрасте от 30 до 70 лет составляет около 6,7% и продолжает нарастать, а в РФ предиабет имеют около 19% активного населения, то есть эти лица находятся в группе риска развития диабета. Предиабет, как и СД2, ассоциируется с возрастом обследуемых и увеличением массы тела. Гендерные различия в распространенности ранних нарушений углеводного обмена не выявлены.
По экспертным данным риск развития СД2-го типа у лиц с НТГ в 6 раз выше, чем у лиц с нормальной толерантностью к глюкозе, а в случаях сочетания НТГ/НГН риск выше в двенадцать раз. Относительный риск общей смертности у лиц с НТГ в 1,48 раза выше, чем в норме, при этом риск сердечно-сосудистых осложнений повышается в 1,66 раза. При наличии НГН риск развития СД2 в 4,7 раза выше, чем у лиц с нормальной толерантностью к глюкозе. Также НГН ассоциируется с относительно высоким риском развития сердечно-сосудистых осложнений.
Таким образом активное вмешательство необходимо проводить уже на предиабетическом уровне гликемии (этапе НГН и НТГ), тем самым предотвращая развитие СД2-типа, который сопровождается различными осложнениями в виде нарушений зрения, атеросклероза сосудов сердца, нижних конечностей и мозга, нефропатии, поражения нервной системы.
С этой целью всем лицам необходим регулярно проводимый скрининг, позволяющий максимально рано выявить НТГ, НГН, а также СД2-типа и соответственно начать своевременное лечение, а значит, предотвращая тем самым риск развития тяжелых осложнений и потенциальную инвалидизацию пациента в будущем. С этой целью должен регулярно проводиться тест «Постпрандиальная глюкоза», особенно лицам с высоким риском СД, который определяет уровень сахара в крови после приема пищи (через 2 часа). Этот тест позволяет выявить состояние предиабета на ранней стадии, когда еще показатели тощаковой гликемии находятся в норме. Частота самоконтроля уровня глюкозы регулируется в зависимости от потребностей, конкретных обстоятельств и целей пациента. Появление индивидуальных глюкометров различного типа для измерения уровня гликемии позволяет сделать самоконтроль относительно простым и доступным большинству заинтересованных лиц.
Показатели теста постпрандиальной глюкозы кроме диагностики ранних стадий сахарного диабета используются также для оценки риска осложнений со стороны сердечно-сосудистой системы (атеросклероз, ИБС) при СД2.
Иркутская городская клиническая больница № 9
Памятка для пациента:
Что сделать, чтобы предупредить развитие гипергликемии и сахарного диабета.
Факты о гипергликемии и сахарном диабете:
- Каждые 20 минут в США регистрируется новый случай заболевания диабетом, а в Европе — каждые сорок минут.
- В настоящее время распространенность явного сахарного диабета среди населения экономически развитых стран достигает 4-7 %. Однако массовые обследования показали, что больных скрытыми формами диабета — в 2 раза больше.
- У лиц, масса тела которых превышает норму на 20 %, сахарный диабет выявляется в 10 раз чаще, чем в популяции. Среди лиц с резко выраженным ожирением заболеваемость диабетом увеличивается в 30 раз. Показано, что сочетание нескольких факторов риска увеличивает вероятность развития клинического сахарного диабета примерно в 29 раз.
- Смертность среди больных сахарным диабетом, перенесших инфаркт миокарда в 1,5 – 2,5 раза выше, чем у лиц без нарушений углеводного обмена.
Гипергликемия (повышенное содержание сахара в крови) возникает, когда уровень сахара в крови поднимается выше нормы. Это происходит, если поджелудочная железа не вырабатывает достаточное количество инсулина, или он не работает так, как надо. Тогда глюкоза – основной источник энергии не усваивается клетками, клетки начинают «голодать», развивается слабость; сахар в крови, наоборот, повышается и вытягивает воду из клеток – появляется жажда; из-за нарушения обмена быстро поражаются мелкие и крупные сосуды головного мозга, сердца, почек и других органов, нарушается иммунитет.
Проверьте, нет ли у Вас признаков сахарного диабета?
- сильная жажда;
- сонливость;
- нечеткое зрение;
- частое мочеиспускание;
- раздражительность;
- зуд (особенно в области промежности);
- сухость кожи, гнойнички и фурункулы;
- повышенный аппетит;
- липкая моча.
Если уровень глюкозы в крови слишком высок, развивается сахарный диабет. В 95% случаев это сахарный диабет 2 типа, встречающейся чаще у людей после 40 лет, ведущих неправильный образ жизни. Посмотрите, может быть, факторы риска этого опасного заболевания есть и у Вас?
- возраст старше 45 лет;
- сахарный диабет у родственников;
- избыточная масса тела;
- низкая физическая активность;
- случайно обнаруженный повышенный уровень глюкозы при обследовании;
- повышение сахара крови при беременности и рождение крупного плода;
- высокое артериальное давление, выше 140/90 мм.рт.ст.;
- изменения в обмене холестерина (низкий уровень липопротеидов высокой плотности ≤ 0,9 ммоль/л и/или уровень триглицеридов ≥ 2,82 ммоль/л);
- поликистоз яичников;
- перенесенные инсульты, инфаркты.
Если что-то Вас насторожило, то единственный способ проверить, есть или нет сахарный диабет, – сделать анализ крови: определить уровень глюкозы натощак и/или через 2 часа после приема 75 грамм глюкозы. Частота обследования зависит от группы риска, в которую Вы попадаете.
| Группа риска | Частота обследования |
| Лица старше 45 лет | Не реже 1 раза в 3 года; |
| Сочетание 3-х и более факторов риска | Не реже 1 раза в 3 года; |
| Лица с предиабетом, особенно с избыточным весом | 1 раз в 1-2 года |
Уровень глюкозы в капиллярной крови
| Проведение анализа | Норма | Предиабет | Диабет |
| Натощак | 3,3-5,5ммоль/л | 5,5-6,1ммоль/л | > 6,1ммоль/л |
| Через 2 часа после приема 75 грамм сахара или в любое время дня | < 7,8ммоль/л | 7,8-11,1ммоль/л | >11,1ммоль/л |
Также Вы можете проверить риск развития у Вас предиабета или сахарного диабета 2 типа в ближайшие 10 лет по опроснику:
- Возраст: до 45 лет (0 баллов), 45-54 лет (2 балла), 55-64 года (3 балла), старше 65 лет (4 балла).
- Индекс массы тела – рост (м), деленный на массу тела (кг) в квадрате, например, при росте 165 см и массе 73 кг индекс равен 73: (1,65 м Х 1,65 ) = 26,8=27 кг/м2: ниже 25 кг/м2 (0 баллов), 25-30 кг/м2 (1 балл), больше 30 кг/м2 (3 балла).
- Объем талии — измеряется под ребрами на уровне пупка. Мужчины: меньше 94 см (0 баллов), 94-102 см (3 балла), больше 102 см (4 балла). Женщины: меньше 80 см (0 баллов), 80-88 см (3 балла), больше 88 см (4 балла).
- Как часто Вы едите овощи, фрукты или ягоды? Каждый день (0 баллов), не каждый день (1 балл);
- Занимаетесь ли Вы физическими упражнениями регулярно? Делаете ли Вы физические упражнения по 30 минут каждый день или 3 часа в течение недели? Да (0 баллов), нет (2 балла);
- Принимали ли Вы когда-либо регулярно лекарства для снижения артериального давления? Нет (0 баллов), да (2 балла).
- Определяли ли у Вас когда-либо уровень сахара в крови выше нормы (на профилактических осмотрах, во время болезни или беременности)? Нет (0 баллов), да (5 баллов).
- Был ли у Ваших родственников сахарный диабет 1 или 2 типа? Нет (0 баллов), да: дедушка/бабушка, тетя/дядя, двоюродные братья/сестры (3 балла), родители, брат/сестра или собственный ребенок (5 баллов).
ОБЩЕЕ КОЛИЧЕСТВО БАЛЛОВ__________________________
Ваш риск развития сахарного диабета 2 типа в течение 10 лет составил:
| Общее количество баллов | Уровень риска СД 2 | Вероятность развития СД 2 |
| Менее 7 | Низкий риск | 1 из 100 (1%) |
| 7-11 | Слегка повышен | 1 из 25 (4%) |
| 12-14 | Умеренный | 1 из 6 (17%) |
| 15-20 | Высокий риск | 1 из 3 (33%) |
| более 20 | Очень высокий риск | 1 из 2 (50%) |
- Если Вы набрали менее 12 баллов, у Вас хорошее здоровье и Вы должны поддерживать здоровый образ жизни.
- Если Вы набрали 12-14 баллов, у Вас возможен предиабет. Вы должны поинтересоваться у Вашего врача об измении образа жизни.
- Если Вы набрали 15-20 баллов, у Вас возможен предиабет или сахарный диабет типа 2. Вам желательно проверить уровень сахара в крови. Вы должны изменить свой образ жизни, а, может, Вам понадобятся и лекарства для контроля уровня сахара в крови.
- Если Вы набрали более 20 баллов, по всей вероятности, у Вас есть сахарный диабет типа 2. Вы должны регулярно глюкометром измерять уровень сахара в крови. Вам нужно изменить свой образ жизни, и Вам необходимы лекарства для контроля уровня сахара в крови.
Профилактика диабета должна начинаться с кухни.
Около 80% пациентов с сахарным 2 типа имеют избыточный вес, который ослабляет действие инсулина. Поэтому первоочередная задача в этой ситуации — снижение веса (не до полной нормы, но на 5-10% ниже исходного) и поддержание его на этом уровне за счет продолжающегося соблюдения диеты. Эта диета должна быть вкусной, разнообразной, не вызывать чувство голода, но содержать меньше калорий, чем пациент употреблял раньше, для этого нужно всего лишь выполнять некоторые правила:
Эти продукты надо резко ограничить:
а) Сильно повышают сахар крови:
- Сахар, мед, сухофрукты, фруктовые соки, кондитерские изделия, сладости, варенье, лимонады (“Фанта”, “Пепси” и т.п.), натуральный квас.
- Манная каша, картофельное пюре, сильно «разваренные» каши.
б) Содержат много калорий:
- Масло сливочное, растительное (особенно в салатах, винегретах и при разогревании пищи), сметана, майонез, заменители масла (Rama и т.п.).
- Сало, сосиски и сардельки, колбасы и паштеты, копчености, жирное мясо, жирная рыба, мясные субпродукты (ливер, печень), куриные окорочка, кожа птиц.
- Жирные (“желтые” и плавленые) сыры, сливки, жирный творог.
- Орехи и семечки, пироги и пирожки.
Потребление этих продуктов нужно сократить вдвое:
- Хлеб (черный или белый), крупы (рис, гречневая, овсяная и др.).
- Картофель, макаронные изделия, кукуруза и соевые продукты, крекер, сушки (несладкие) и т.п.
- Фрукты: распределить в течение дня.
- Конфеты, вафли и т.п.: в виде “нечастого лакомства” (1 раз в неделю).
- Допустимы в умеренных количествах: нежирные мясо, рыба, творог.
Увеличить потребление:
- Овощи (но без добавления жиров) в виде овощных гарниров: капуста, цветная капуста, морковь, свекла, репа, редис, огурцы, помидоры, зелень.
- Напитки без сахара: минеральная вода, чай).
| Физические нагрузки для профилактики сахарного диабета Показаны аэробные упражнения, такие как: ходьба, бег трусцой, плавание, теннис, катание на велосипеде, ритмическая гимнастика (способствуют более интенсивному усвоению организмом кислорода и полезны для сердца и кровеносных сосудов). Аэробные физические нагрузки обеспечивают максимальную доставку кислорода к органам и тканям, поэтому они должны выполняться на определенном пульсе, для каждого человека он рассчитывается индивидуально.
|
Патогенез
Патогенез предиабета обусловлен качественным/количественными дефицитом инсулина в основе которого лежит снижение активности инсулина в адипоцитах, мышечной ткани и гепатоцитах, обусловленное дефицитом выработки инсулина β-клетками поджелудочной железы и инсулинорезистентность (снижение чувствительности рецепторов к инсулину). Эти нарушения пострецепторного действия инсулина совместно с нарастающим снижением продуцирования инсулина способствуют повышению глюкозы до соответствующих значений НГН (6,1– 6,9 ммоль/л) и/или НТГ (7,8–11,0 ммоль/л после ПГТТ с глюкозой). У пациентов с умеренной гипергликемией в основе лежит в снижении чувствительности к инсулину периферических тканей, преимущественно мышечной ткани. А при гипергликемии натощак негативно действующим дополнительным фактором может быть увеличение продукции глюкозы печенью.
Лечение гипергликемии в условиях стационара
Взаимоотношения между гипергликемией и острыми заболеваниями сложны [1,3,4]. Гипергликемия нередко имеет место у госпитализированных пациентов вследствие повышения уровней гормонов стресса. Исследования в экспериментальных условиях показали, что выраженная гипергликемия [уровень глюкозы крови выше 250 мг/дл (13,9 ммоль/л)] оказывает негативное действие на сердечно–сосудистую и иммунную системы (рис. 1) [1,3,4]. В нескольких ретроспективных исследованиях показано, что гипергликемия связана с летальными исходами у стационарных больных. Уровень глюкозы после операции является важным прогностическим фактором вероятности развития инфекционных осложнений у больных, которым были произведены операции на сердце [5,6]. По данным исследования, включавшего больных сахарным диабетом, перенесших инфаркт миокарда, повышенный уровень глюкозы при госпитализации был связан со смертностью как в период госпитализации, так и в течение первого года после инфаркта [7]. Сходные результаты были получены у пациентов, находящихся на лечении в палатах интенсивной терапии (ПИТ) [8], больных после операций [9], а также людей, перенесших отличные от инфаркта острые сердечно–сосудистые нарушения, включая инсульт [10–12]. Связь между уровнем глюкозы крови и риском смерти продолжала оставаться достоверной даже с учетом тяжести заболевания [12]. Подобные наблюдения не ограничиваются больными диабетом [10–12]. По данным одного из исследований, смертность в период нахождения в стационаре выше у больных, у которых гипергликемия выявлена впервые, по сравнению с имевшими диагноз сахарный диабет [13]. Подобные данные, хотя и интересны, не позволяют говорить о наличии причинно–следственной связи. Вопрос о том, является ли повышение уровня глюкозы потенциально устранимым механизмом развития осложнений или же это просто симптом, сопутствующий тяжелым заболеваниям, продолжает оставаться открытым. Если повышение уровня глюкозы само по себе опасно, то интенсивная его коррекция может быть просто необходимой. Очевидно, что инсулинотерапия и контроль за ее результатами требуют времени и денег. Кроме того, подобное лечение повышает риск развития гипогликемии, способной приводить к серьезным осложнениям. Каковы же доказательства того, что жесткий контроль уровня глюкозы в период нахождения в стационаре улучшает результаты лечения? Стратегии и доказательства В нескольких работах изучены эффекты тщательного контроля уровня глюкозы крови в условиях реанимационных отделений, однако в этих исследованиях участвовали весьма разнородные группы больных (с и без диабета). Кроме того, сильно различались дизайн исследований, цели лечения и методики введения инсулина. Соответственно и полученные результаты были весьма различными. В работе, включившей 1499 пациентов, находившихся на лечении в ПИТ отделения кардио–торакальной хирургии, применение инсулина в форме инфузии с целью снижения уровня глюкозы до 150–200 мг/дл (8,3–11,1 ммоль/л) в течение 24 часов после открытых операций на сердце приводило к значительному снижению частоты инфицирования послеоперационных ран по сравнению с больными, которым лечение инсулином проводили по стандартной схеме (0,8% vs. 2,0%). Отсутствие рандомизации осложняет трактовку этих результатов в связи с тем, что контрольная группа была сформирована ретроспективно и за время, прошедшее с момента нахождения этих больных в стационаре, качество оказания медицинской помощи могло улучшиться. Следует, впрочем, отметить, что аналогичные результаты были получены в рандомизированном и нерандомизированном исследованиях меньшего масштаба, в которых также изучалась эффективность контроля уровня глюкозы крови после кардиологических операций. В исследовании Diabetes Insulin–Glucose Infusion in Acute Myocardial Infarction (DIGAMI) 620 больных диабетом, перенесших инфаркт миокарда, были рандомизированы на проведение интенсивной или стандартной коррекции уровня глюкозы в период нахождения в стационаре и в течение 3 месяцев после выписки [16]. Интенсивное лечение с применением инфузии инсулина в течение первых 24 часов после госпитализации с целью снижения уровня глюкозы до 126–196 мг/дл (7,0–10,9 ммоль/л) с последующими многократными инъекциями инсулина для поддержания средней концентрации глюкозы на уровне 173 мг/дл (9,6 ммоль/л) существенно отличалость от стандарного, на фоне которого средний уровень глюкозы составил 211 мг/дл (11,7 ммоль/л) (p<0,001). В группе больных, получавших интенсивное лечение, смертность в течение первого года была на 29% ниже по сравнению с группой, получавшей стандартное лечение (18,6% vs. 26.1%, p=0,03), достоверное различие показателей смертности сохранялось при наблюдении в течение 5 лет [17]. Однако дизайн исследования не позволял сделать определенного вывода о том, какое именно лечение, стационарное или амбулаторное, приводило к улучшению выживаемости. Целью исследования DIGAMI–2 являлось разрешение этого вопроса, для чего 1253 пациента с диабетом были рандомизированы на получение трех различных видов лечения после острого инфаркта миокарда: интенсивное стационарное [инфузия инсулина, целевая концентрация глюкозы от 126 до 180 мг/дл (от 7,0 до 10,0 ммоль/л)] и амбулаторное лечение, интенсивное лечение только в условиях стационара и стандартное лечение [18]. Существенных различий в смертности и частоте осложнений между группами не было, однако статистическая достоверность исследования была слабой и различия в средних уровнях глюкозы между группами были небольшими. В связи с этим из результатов данного и еще одного, имевшего те же недостатки исследования, сложно сделать определенные выводы [19]. Работы, в которых изучалась эффективность инфузии глюкозы, инсулина и калия (ГИК), также дали противоречивые результаты [20]. В этих исследованиях целью являлось не достижение определенного уровня глюкозы крови, а оценка потенциальных положительных эффектов самого введения инсулина во время или вскоре после инфаркта миокарда. По данным наиболее крупного из исследований, включавшего 20 тыс. пациентов, введение ГИК не приводило к улучшению результатов лечения, хотя следует отметить, что уровни глюкозы в основной группе были выше, чем в контрольной. Тем не менее существуют достаточно убедительные доказательства, что жесткий контроль уровня глюкозы крови в условиях ПИТ улучшает результаты лечения. Так, в рандомизированном исследовании, включавшем 1548 интубированных пациентов, находившихся в хирургической ПИТ (у 13% был диагноз сахарный диабет), сравнивали интенсивное лечение, включавшее инфузию инсулина [целевая концентрация глюкозы от 80 до 110 мг/дл (от 4,4 до 6,1 ммоль/л)] со стандартным лечением [внутривенное введение инсулина только тем больным, у которых уровень глюкозы превышал 215 мг/дл (11,9 ммоль/л)] [22]. В группе, получавшей интенсивное лечение, смертность была на 42% ниже (4,6% vs. 8,0%, p<0,04). Это снижение имело место прежде всего у больных, находившихся в ПИТ более 5 дней. Кроме того, у больных, получавших интенсивное лечение, отмечена достоверно более низкая частота диализа и септицемии, а также возникновения необходимости в переливании крови или искусственной вентиляции легких. В другом исследовании, включавшем 1200 пациентов общей ПИТ, проведенном по той же схеме, результаты оказались менее однозначными [23]. В целом внутрибольничная смертность не была достоверно снижена у больных, получавших интенсивное лечение, по сравнению со стандартным (37,3% vs. 40,0%, p=0,33). В то же время интенсивное лечение приводило к уменьшению частоты осложнений (включая снижение длительности искусственной вентиляции легких) и более ранней выписке. Кроме того, в группе больных, находившихся в ПИТ в течение 3–х дней и более (767 пациентов), интенсивное лечение приводило к снижению внутрибольничной смертности (43,0% vs. 52,5%, p=0,009). Впрочем, заранее прогнозировать длительность нахождения в ПИТ невозможно, а интенсивное лечение повышало смертность среди больных, находившихся в ПИТ менее 3 дней. Данное повышение, хотя и не оказалось статистических достоверным (относительный риск 1,09; 95%–й доверительный интервал от 0,89 до 1,32), может иметь большое значение. В обоих исследованиях гипогликемия [определяемая как уровень глюкозы менее 40 мг/дл (2,2 ммоль/л)] значительно чаще встречалась у больных, получавших интенсивное лечение, по сравнению со стандартной терапией (5,2% vs. 0,7% в хирургической ПИТ [22] и 18,7% vs. 3,1% в общей ПИТ [23]). Хотя гипогликемия не приводила к гемодинамическим нарушениям или судорогам, ее значение у тяжелых больных остается не до конца ясным. Более того, в исследовании, проведенном в общей ПИТ, гипогликемия была независимым прогностическим фактором риска смерти. Возможности более осторожного интенсивного лечения были изучены в исследовании, включавшем смешанную группу пациентов из хирургической и общей ПИТ, в которой инсулин вводили подкожно с целью достижения уровня глюкозы ниже 140 мг/дл (7,8 ммоль/л). Инсулин в форме инфузии вводили, только если уровень глюкозы превышал 200 мг/дл [24]. Внутрибольничная смертность была значительно ниже среди больных, получавших интенсивное лечение, по сравнению с группой контроля, сформированной по данным историй болезни (14,8% vs. 20,9%, p=0,002). К настоящему времени нет данных относительно эффективности интенсивного лечения гипергликемии у стационарных больных вне ПИТ. Факторы, влияющие на выбор метода лечения На инсулинорезистентность и способность организма больных секретировать этот гормон оказывает влияние ряд факторов, включая тяжесть заболевания, принимаемые препараты (прежде всего глюкокортикоиды и прессорные агенты). Кроме того, питанию больных в стационаре нередко мешают обследования и операции, которые также могут нарушать режим приема медикаментозных препаратов, что препятствует адекватному контролю за уровнем глюкозы крови [3,4,25]. Важно знать, есть ли у больного диабет, и если есть – его тип (так как у пациентов с диабетом 1 типа повышен риск развития кетоацидоза), а также то, каким образом проводилась коррекция уровней глюкозы до госпитализации. Следует также обращать внимание на: – особенности питания больного, которые определяют дозировку инсулина; – обычный уровень глюкозы крови, который важен для принятия решения об интенсивности лечения и скорости коррекции гипергликемии; – степень контроля над уровнем глюкозы крови до госпитализации; – уровень гликированного гемоглобина (может позволить оценить необходимость в более интенсивном лечении у больных с сахарным диабетом, ау больных с впервые выявленной гипергликемией повышение концентрации гликированного гемоглобина указывает на наличие диабета до госпитализации). При определении целесообразности проведения интенсивной терапии необходимо оценить длительность нахождения больного в стационаре. Пероральные препараты Инсулин является предпочтительным препаратом для лечения стационарных больных, так как его доза может быть более тщательно и быстро подобрана и не имеет ограничений. Тем не менее у определенных больных (особенно при нетяжелом состоянии и возможности нормального питаться) можно продолжить прием пероральных препаратов при их эффективности до госпитализации. С особым вниманием следует относиться к назначению метформина, учитывая противопоказания к его применению (включая почечную недостаточность, сердечную недостаточность и необходимость в проведении рентгенологических исследований с введением контрастного вещества). Прием тиазолидиндионов следует прекратить при наличии признаков сердечной или печеночной недостаточности (даже после прекращения приема антигипергликемическое действие этих препаратов может сохраняться в течение нескольких недель). Для пациентов, которые питаются нерегулярно, препараты, вызывающие выделение инсулина (например, из группы сульфонилмочевины), особенно опасны, а ингибиторы альфа–глюкозидазы неэффективны. Умеренное снижение дозировки препаратов может быть произведено у пациентов, находящихся на стационарном лечении и получающих диету с ограниченной калорийностью, так как подобное питание может уменьшать выраженность гипергликемии. Если уровень глюкозы значительно повышен при поступлении или если контроль над ним ухудшается во время нахождения в больнице что бывает довольно часто следует начать лечение инсулином. Инсулин В условиях ПИТ инсулин обычно вводят путем длительной внутривенной инфузии. Существует несколько общепринятых протоколов введения [3,22,26–30]. Наиболее эффективными являются те, в которых применяется динамическая шкала, обеспечивающая изменение дозы в зависимости от изменений уровня глюкозы [29,31]. Частое измерение уровня глюкозы (обычно каждый час) крайне важно для минимизации риска гипогликемии. По мере улучшения состояния пациента можно перейти к подкожному введению инсулина; при этом для расчетов используют последнюю скорость инфузии, умноженную на промежутки между введениями, итоговую дозу делят на основную и связанную с едой части (рис. 2). Следует отметить, что необходимо избегать больших перерывов между внутривенным и подкожным введением, особенно у пациентов с сахарным диабетом 1 типа. Пациенты с диабетом 2 типа, которые нуждаются менее чем в 2 единицах инсулина в час, могут получать менее интенсивное лечение; для некоторых больных может быть достаточно пероральных препаратов. За пределами отделений интенсивной терапии все еще широко применяются шкалы для определения дозировки инсулина в зависимости от уровня гипергликемии [4]. Применение подобной тактики, как правило, недостаточно эффективно [32], особенно у пациентов с диабетом 1 типа, которые нуждаются в постоянном поступлении инсулина для подавления кетогенеза. Лучший контроль может быть достигнут при предупреждающей тактике введения. Методы введения, включающие базальный инсулин (среднего или длительного действия) и инсулин короткого действия, который вводят перед едой с целью снизить выраженность постпрандиальной гипергликемии, позволяют достичь результатов, наиболее близких к физиологическому уровню [3,33–35]. Быстродействующие аналоги инсулина (лиспро, аспарт и глулизин) следует вводить сразу перед едой. Стандартный человеческий инсулин следует вводить за 30 минут до еды, что часто бывает сложно в условиях стационара в связи с занятостью персонала. Кроме того, быстродействующие препараты лучше контролируют постпрандиальную гипергликемию. У пациентов, диета которых является неопределенной, следует придерживаться консервативной тактики. Альтернативой является введение быстродействующего инсулина сразу после еды, доза определяется в зависимости от объема поглощенной пищи. Дополнительные корректирующие дозы могут быть введены вместе с прандиальным инсулином с целью компенсации гипергликемии, возникающей перед едой. Чувствительные к инсулину пациенты (большинство пациентов с диабетом 1 типа, худые пациенты, получающие относительно небольшие дозы инсулина (менее 30–40 единиц в сутки), а также склонные к гипогликемии) нуждаются в небольших корректирующих дозах (например, 1 единица для коррекции уровня глюкозы 150 мг/дл (8,3 ммоль/л), 2 единицы для 200 мг/дл (11,1 ммоль/л) и т.д.). Большинство пациентов с сахарным диабетом 2 типа (имеющие излишний вес или получающие умеренные дозы инсулина – от 40 до 100 единиц в день) нуждаются в умеренных корректирующих дозах (например, 2 единицы для коррекции уровня глюкозы 150 мг/дл, 4 единицы для коррекции 200 мг/дл и т.д.). Некоторым пациентам с диабетом 2 типа и выраженной резистентностью к инсулину (с выраженным ожирением, получающие инсулин в больших дозах (более 100 единиц в сутки) или принимающие кортикостероиды) следует вводить большие корректирующие дозы (например, 4 единицы при уровне глюкозы крови 150 мг/дл, 8 единиц при 200 мг/дл и т.д.). По мере улучшения общего состояния больного может повышаться чувствительность к инсулину. Как правило, если состояние пациента стабильно, соотношение доз основного и прандиального инсулина составляет 1:1. Дозу основного инсулина подбирают в зависимости от общей динамики изменения концентрации глюкозы. Если применяется гларгин или детемир, определение дозы производят на основании утренних концентраций глюкозы. При применении НПХ его дозировку рассчитывают, отталкиваясь от утренней концентрации глюкозы или же от ее значений перед вечерним приемом пищи. В период подбора дозы можно также включать корректирующую дозу в основную, добавляя 50% от корректирующей дозы, применявшейся в предшествующий день к основной. Дозу прандиального инсулина определяют на основании уровней постпрандиальной гипергликемии. Корректирующая дозировка инсулина может быть подобрана на основании эффективности применявшейся ранее дозы. Для обеспечения безопасности больного его потребность в инсулине должна быть переоценена сразу после любых изменений в диете. Некоторым больным диабетом 2 типа может быть достаточно проведения менее агрессивного лечения, в частности, введения только основного инсулина (например, гларгин один раз в день, детемир один или два раза в день или НПХ два раза в день) или удобных смешанных препаратов, включающих инсулин среднего и короткого или очень короткого действия (например, «70/30»). Подобный подход может быть оправданным у пациентов с умеренной гипергликемией, особенно если планируется выписка и нет времени для тщательного подбора дозы инсулина. Если пациент, получающий инсулин, не ест, следует вводить только основную дозу в форме стандартного инсулина каждые 6 часов. Это совершенно необходимо у пациентов с сахарным диабетом 1 типа и желательно у пациентов с сахарным диабетом 2 типа. В подобных случаях также можно применять инфузию инсулина, особенно если вызывает сомнение адекватность абсорбции из подкожных тканей. У пациентов, которые самостоятельно питаются и получают инсулин, режим введения препарата, применявшийся до госпитализации, может быть сохранен при его эффективности. Как и в случае пероральных препаратов, в зависимости от клинической ситуации возможно снижение дозы инсулина при уменьшении калорийности питания. Это особенно актуально для больных сахарным диабетом 2 типа. Если концентрация глюкозы при поступлении высока (более 200 мг/дл), дозу инсулина следует увеличить. Следует рассмотреть возможность перехода к корректирующим дозам. Если выраженная гипергликемия [уровень глюкозы от 300 до 400 мг/дл (от 16,7 до 22,2 ммоль/л)] сохраняется в течение более 24 часов и не поддается коррекции увеличенными дозами подкожного инсулина, следует рассмотреть возможность его внутривенной инфузии. Следует отметить, что в связи с коротким периодом полувыведения инсулина при внутривенном введении (5–9 минут), при развитии гипогликемии она может быть быстро устранена. По соображениям безопасности при применении инфузии инсулина в общих палатах (по сравнению с ПИТ) следует стремиться к несколько более высоким концентрациям глюкозы крови. Контроль за концентрацией глюкозы у пациентов, получающих постоянное энтеральное питание через зонд, лучше всего достигается при применении основного инсулина, с добавлением корректирующих доз по необходимости каждые 6 часов. Если кормление прервано, следует внутривенно ввести то же количество углеводов (например, декстрозы), которое должно вводится энтерально для предотвращения гипогликемии. В случае если пациент находится полностью на парентеральном питании, инсулин можно добавлять непосредственно во флаконы с последним. Дозу титруют с шагом 5–10 единиц на литр для достижения оптимального контроля. Для хорошего контроля необходима частая оценка концентрации глюкозы крови, на основании которой каждые 1–2 дня следует корректировать дозировку инсулина. Впрочем, прежде чем увеличивать дозировку препарата, следует оценить возможные причины гипергликемии (например, пропущенные дозы, излишнее питание, инфекция) и устранить их. Несвоевременный контроль концентрации глюкозы, питание и введение прандиального инсулина также являются частыми причинами колебаний уровня глюкозы в больничных условиях. Для качественного контроля уровня глюкозы необходима координация действий медсестер и сотрудников, обеспечивающих питание больных. В идеале исследование крови из пальца необходимо выполнять каждый раз перед едой и перед сном. Раннее исследование постпрандиальной гликемии (в течение 2–3 часов после еды) может приводить к излишне интенсивному лечению инсулином, чего следует избегать за исключением особых ситуаций (например, лечения беременных женщин). Перед выпиской схема введения инсулина должна быть упрощена в зависимости от возможностей больного. У некоторых больных сахарным диабетом 2 типа может быть возможным назначение длительнодействующего инсулина 1 раз в день. У других больных, которым в период нахождения в стационаре требовались небольшие дозы инсулина или же при отличном контроле уровня глюкозы крови при введении менее чем 25–30 единиц в день, достаточными могут быть коррекция диеты или пероральные препараты. В случае назначения или отмены антигипергликемических препаратов или изменения их дозировки в период нахождения в стационаре, необходим повторный осмотр пациентов через 1–2 недели после выписки. Подобным образом следует вести стационарных больных с впервые выявленной гипергликемией, хотя у части пациентов нет необходимости в продолжении лечения, направленного на снижение уровня глюкозы, после компенсации основного заболевания. У таких больных концентрация глюкозы натощак (и, если возможно, гликированного гемоглобина) должны контролироваться через 1–2 месяца после выписки. Рекомендации В двух работах [2,36] представлены рекомендации по контролю уровня глюкозы крови у стационарных больных (табл. 1). Эти данные неоднозначны, поскольку проведено небольшое количество рандомизированных исследований. Общепринято, что инсулин следует вводить внутривенно в условиях ПИТ и что другие методы введения инсулина должны быть максимально приближены к физиологическим условиям, особенно у пациентов с сахарным диабетом 1 типа [1–4,25]. В связи с отсутствием исследований эффективности подкожного введения инсулина в условиях стационара рекомендации базируются на клиническом опыте. Неясные области Накоплено мало данных о роли жесткого контроля уровней глюкозы крови у стационарных больных. Хотя большинство исследований показывают, что снижение уровня глюкозы у тяжело больных пациентов улучшает выживаемость [37], точная целевая концентрация, оптимальная методика введения и группа пациентов, в наибольшей степени нуждающихся в подобном подходе (как и методы ее определения), продолжают оставаться неизвестными [38,39]. Поскольку интенсивная инсулинотерапия снижает смертность преимущественно среди больных, находящихся в ПИТ длительное время, можно сделать вывод, что не у всех тяжелобольных пациентов эффективность жесткого контроля уровней глюкозы крови одинакова [22,23,40]. Продолжающиеся исследования интесивного лечения инсулином в ПИТ предоставят новую информацию по данному вопросу [41]. Оптимальный подход к коррекции гипергликемии у пациентов, перенесших инфаркт миокарда, неизвестен [14–17,42]. Особого внимания заслуживают данные двух недавних исследований, продемонстрировавших взаимосвязь между развитием гипергликемии в период госпитализации по поводу инфаркта миокарда и повышенным риском смерти [43,44]. Хотя при острых коронарных синдромах инсулин обладает не только гипогликемическим действием (но еще и антилиполитическим, сосудорасширяющим, противовоспалительным и профибринолитическим) [45], клиническое значение этого явления неясно и противоречиво [21]. Неясно, можно результаты исследований в ПИТ распространять на не столь тяжелых пациентов. Следует тщательно оценить соотношение между возможной выгодой и опасностями (прежде всего развития гипогликемии). Заключение и рекомендации В хирургических и общих ПИТ концентрацию глюкозы крови следует поддерживать на уровне менее 140 мг/дл [24,39] и, возможно, даже менее 110 мг/дл [22,23]. Оптимальные показатели концентрации глюкозы у больных в отделениях кардиореанимации являются более спорными: вполне вероятно, что стремиться следует к более высоким значениям (до 180 мг/дл) [15]. Внутривенное введение инсулина позволяет быстрее подобрать дозу у тяжелобольных пациентов, чем при подкожных инъекциях. У хирургических и терапевтических больных, не находящихся в тяжелом состоянии, целесообразным остается достижение концентрации глюкозы перед едой от 90 до 150 мг/дл (от 5,0 до 8,3 ммоль/л) [39] не только с целью снижения вероятности гипергликемии, но и во избежание гипогликемии. Важно отметить, что жесткий контроль за концентрацией глюкозы должен осуществляться под руководством квалифицированного персонала. Хотя точные целевые концентрации глюкозы у стационарных больных остаются неопределенными [1–3,38,39], важно понимать, что во время госпитализации лечение инсулином должно быть активным, с частой коррекцией дозы, в форме внутривенной инфузии. При выписке больному надо разъяснить схему лечения в амбулаторных условиях.
Реферат подготовлен В.В. Иремашвили по материалам статьи Inzucchi S.E. « Management of Hyperglycemia in the Hospital Setting». New England Journal of Medicine 2006; No.355: pp.1903–1911.
Литература 1. Clement S, Braithwaite SS, Magee MF, et al. Management of diabetes and hyperglycemia in hospitals. Diabetes Care 2004; 27:553–91. [Errata, Diabetes Care 2004;27: 856, 1255.] 2. Garber AJ, Moghissi ES, Bransome ED Jr, et al. American College of Endocrinology position statement on inpatient diabetes and metabolic control. Endocr Pract 2004;10:77–82. 3. Trence DL, Kelly JL, Hirsch IB. The rationale and management of hyperglycemia for in–patients with cardiovascular disease: time for change. J Clin Endocrinol Metab 2003;88:2430–7. 4. Metchick LN, Petit WA Jr, Inzucchi SE. Inpatient management of diabetes mellitus. Am J Med 2002;113:317–23. 5. Zerr KJ, Furnary AP, Grunkemeier GL, Bookin S, Kanhere V, Starr A. Glucose control lowers the risk of wound infection in diabetics after open heart operations. Ann Thorac Surg 1997;63:356–61. 6. Golden SH, Peart–Vigilance C, Kao WHL, Brancati FL. Perioperative glycemic control and the risk of infectious complications in a cohort of adults with diabetes. Diabetes Care 1999;22:1408–14. 7. Malmberg K, Norhammar A, Wedel H, Ryden L. Glycometabolic state at admission: important risk marker of mortality in conventionally treated patients with diabetes mellitus and acute myocardial infarction: long–term results from the Diabetes and Insulin–Glucose Infusion in Acute Myocardial Infarction (DIGAMI) study. Circulation 1999;99:2626–32. 8. Krinsley JS. Association between hyperglycemia and increased hospital mortality in a heterogeneous population of critically ill patients. Mayo Clin Proc 2003; 78:1471–8. 9. Pomposelli JJ, Baxter JK III, Babineau TJ, et al. Early postoperative glucose control predicts nosocomial infection rate in diabetic patients. JPEN J Parenter Enteral Nutr 1998;22:77–81. 10. Capes SE, Hunt D, Malmberg K, Gerstein HC. Stress hyperglycaemia and increased risk of death after myocardial infarction in patients with and without diabetes: a systematic overview. Lancet 2000;355:773–8. 11. Capes SE, Hunt D, Malmberg K, Pathak P, Gerstein HC. Stress hyperglycemia and prognosis of stroke in nondiabetic and diabetic patients: a systematic overview. Stroke 2001;32:2426–32. 12. Kosiborod M, Rathore SS, Inzucchi SE, et al. Admission glucose and mortality in elderly patients hospitalized with acute myocardial infarction: implications for patients with and without recognized diabetes. Circulation 2005;111:3078–86. 13. Umpierrez GE, Isaacs SD, Bazargan N, You X, Thaler LM, Kitabchi AE. Hyperglycemia: an independent marker of inhospital mortality in patients with undiagnosed diabetes. J Clin Endocrinol Metab 2002;87:978–82. 14. Lazar HL, Chipkin SR, Fitzgerald CA, Bao Y, Cabral H, Apstein CS. Tight glycemic control in diabetic coronary artery bypass graft patients improves perioperative outcomes and decreases recurrent ischemic events. Circulation 2004;109:1497–502. 15. Hruska LA, Smith JM, Hendy MP, Fritz VL, McAdams S. Continuous insulin infusion reduces infectious complications in diabetics following coronary surgery. J Card Surg 2005;20:403–7. 16. Malmberg K, Ryden L, Efendic S, et al. Randomized trial of insulin–glucose infusion followed by subcutaneous insulin treatment in diabetic patients with acute myocardial infarction (DIGAMI study): effects on mortality at 1 year. J Am Coll Cardiol 1995;26:57–65. 17. Malmberg K. Prospective randomised study of intensive insulin treatment on long term survival after acute myocardial infarction in patients with diabetes mellitus. BMJ 1997;314:1512–5. 18. Malmberg K, Ryden L, Wedel H, et al. Intense metabolic control by means of in– sulin in patients with diabetes mellitus and acute myocardial infarction (DIGAMI 2): effects on mortality and morbidity. Eur Heart J 2005;26:650–61. 19. Cheung NW, Wong VW, McLean M. The Hyperglycemia: Intensive Insulin Infusion in Infarction (HI–5) study: a randomized controlled trial of insulin infusion therapy for myocardial infarction. Diabetes Care 2006;29:765–70. 20. Fath–Ordoubadi F, Beatt KJ. Glucoseinsulin–potassium therapy for treatment of acute myocardial infarction: an overview of randomized placebo–controlled trials. Circulation 1997;96:1152–6. 21. Mehta SR, Yusuf S, Diaz R, et al. Effect of glucose–insulin–potassium infusion on mortality in patients with acute ST–segment elevation myocardial infarction: the CREATE–ECLA randomized controlled trial. JAMA 2005;293:437–46. 22. Van den Berghe G, Wouters P, Weekers F, et al. Intensive insulin therapy in critically ill patients. N Engl J Med 2001; 345:1359–67. 23. Van den Berghe G, Wilmer A, Hermans G, et al. Intensive insulin therapy in the medical ICU. N Engl J Med 2006;354: 449–61. 24. Krinsley JS. Effect of an intensive glucose management protocol on the mortality of critically ill adult patients. Mayo Clin Proc 2004;79:992–1000. [Erratum, Mayo Clin Proc 2005;80:1101.] 25. Moghissi ES, Hirsch IB. Hospital management of diabetes. Endocrinol Metab Clin North Am 2005;34:99–116. 26. Furnary AP, Gao G, Grunkemeier GL, et al. Continuous insulin infusion reduces mortality in patients with diabetes undergoing coronary artery bypass grafting. J Thorac Cardiovasc Surg 2003;125:1007–21. 27. Markovitz LJ, Wiechmann RJ, Harris N, et al. Description and evaluation of a glycemic management protocol for patients with diabetes undergoing heart surgery. Endocr Pract 2002;8:10–8. 28. Goldberg PA, Siegel MD, Sherwin RS, et al. Implementation of a safe and effective insulin infusion protocol in a medical intensive care unit. Diabetes Care 2004; 27:461–7. 29. Goldberg PA, Roussel MG, Inzucchi SE. Clinical results of an updated insulin infusion protocol in critically ill patients. Diabetes Spectrum 2005;18:188–91. 30. Ku SY, Sayre CA, Hirsch IB, Kelly JL. New insulin infusion protocol improves blood glucose control in hospitalized patients without increasing hypoglycemia. Jt Comm J Qual Patient Saf 2005;31:141–7. 31. Meijering S, Corstjens A, Tulleken JE, Meertens JHJM, Zijlstra JG, Ligtenberg JM. Towards a feasible algorithm for tight glycaemic control in critically ill patients: a systematic review of the literature. Crit Care 2006;10:R19. 32. Queale WS, Seidler AJ, Brancati FL. Glycemic control and sliding scale insulin use in medical inpatients with diabetes mellitus. Arch Intern Med 1997;157:545–52. 33. Hirsch IB. Insulin analogues. N Engl J Med 2005;352:174–83. 34. Riddle MC. Glycemic management of type 2 diabetes: an emerging strategy with oral agents, insulins, and combinations. Endocrinol Metab Clin North Am 2005;34:77–98. 35. Edelman SV, Morello CM. Strategies for insulin therapy in type 2 diabetes. South Med J 2005;98:363–71. 36. American Diabetes Association. Standards of medical care in diabetes. Diabetes Care 2005;28:Suppl 1:S4–S36. [Erratum, Diabetes Care 2005;28:990.] 37. Pittas AG, Siegel RD, Lau J. Insulin therapy for critically ill hospitalized patients: a meta–analysis of randomized controlled trials. Arch Intern Med 2004; 164:2005–11. 38. Bryer–Ash M, Garber AJ. Point: inpatient glucose management: the emperor finally has clothes. Diabetes Care 2005; 28:973–5. 39. Inzucchi SE, Rosenstock J. Counterpoint: inpatient glucose management: a premature call to arms? Diabetes Care 2005;28:976–9. 40. Falciglia M, D’Alessio DA, Almenoff PLMD, Freyberg RW, Diab D, Render ML. Hyperglycemia and mortality in 252,000 critically ill patients. Presented at the 66th Scientific Sessions of the American Diabetes Association, Washington, DC, June 9–13, 2006. abstract. 41. ClinicalTrials.gov. Normoglycaemia in intensive care evaluation and survival using glucose algorithm regulation (NICESUGAR study). (Accessed October 6, 2006, at https://www.clinicaltrials.gov/ct/show/NCT00220987.) 42. Furnary AP, Zerr KJ, Grunkemeier GL, Starr A. Continuous intravenous insulin infusion reduces the incidence of deep sternal wound infection in diabetic patients after cardiac surgical procedures. Ann Thorac Surg 1999;67:352–62. 43. Pinto DS, Skolnick AH, Kirtane AJ, et al. U–shaped relationship of blood glucose with adverse outcomes among patients with ST–segment elevation myocardial infarction. J Am Coll Cardiol 2005; 46:178–80. 44. Svensson AM, McGuire DK, Abrahamsson P, Dellborg M. Association between hyper– and hypoglycaemia and 2 year allcause mortality risk in diabetic patients with acute coronary events. Eur Heart J 2005;26:1255–61. 45. Chaudhuri A, Janicke D, Wilson MF, et al. Anti–inflammatory and profibrinolytic effect of insulin in acute ST–segmentelevation myocardial infarction. Circulation 2004;109:849–54. 46. Cryer PE. Hypoglycaemia: the limiting factor in the glycaemic management of the critically ill? Diabetologia 2006;49: 1722–5. 47. Inpatient diabetes and glycemic control: management: a call to action conference, January 2006. AACE–ADA Consensus Development Conference position statement. (Accessed October 6, 2006, at https://www.aace.com/meetings/consensus/IIDC/.)
Причины
Причины повышения глюкозы в крови варьируют в широких пределах, основными из которых являются:
- Гормонально-обусловленная гипергликемия (гипертиреоз, сахарный диабет, семейный полиэндокринный аденоматоз, акромегалия, феохромоцитома, болезнь Иценко-Кушинга).
- Гипергликемия центрального происхождения (отравления, травмы головного мозга с кровоизлияниями в ІV желудочек мозга, энцефалит, опухоли).
- Психогенные расстройства (стресс).
- Заболевания поджелудочной железы (панкреатит), печеночная недостаточность.
- Глубокая недоношенность ребенка.
- Гипергликемия на фоне развития различных критических состояниях.
- Алиментарно-обусловленная гипергликемия (расстройства питания — булимия/длительное избыточное потребление легкоусваивающихся углеводов; синдром Прадера-Вилли — предрасположенность на фоне ожирения к развитию инсулинрезистентного СД в детском возрасте; липодистрофия Сайпа-Лоренса — предрасположенность к развитию СД2Т; синдром Урбаха-Вите — склонность к гипергликемии натощак).
- Лекарственно-индуцированная гипергликемия (глюкокортикостероиды, антипсихотики второго поколения, станины, тиазидные диуретики, ингибиторы кальциневрина и др.).
К факторам риска развития нарушений углеводного обмена относятся:
- Наличие родства с больными СД2.
- Возраст 40 лет и старше с ИМТ ≥25 кг/м.
- Низкая (недостаточная) физическая активность.
- Лица с артериальной гипертензией, ИБС.
- Синдром поликистозных яичников.
Симптомы
Особенностью предиабета является отсутствие четкой специфической клинической симптоматики, характерной для сахарного диабета, что обусловлено в первую очередь сохраненным обеспечением энергией тканей и органов и незначительной глюкозурией. В редких случаях симптомы гипергликемии на этапе НГН и НТГ проявляются в виде неспецифических жалоб пациента на повышенную утомляемость, снижение трудоспособности, ухудшение заживления раневых дефектов.
К косвенным признакам гипергликемии на ранней стадии относят:
- ожирение или избыточную массу тела;
- артериальную гипертензию;
- нарушения со стороны сердечно-сосудистой системы;
- атерогенную дислипидемию (повышение уровней триглицеридов и снижение уровня холестерина за счет ЛПВП (липопротеинов высокой плотности);
- повышение содержания мочевой кислоты в крови (гиперурикемия);
- нарушение фибринолиза.
При осмотре у большинства пациентов с преддиабетом отмечается увеличение окружности талии до показателей >94 см у лиц мужского пола и >80 см у женщин. При этом, жировая масса распределена преимущественно на туловище при ее относительном уменьшении в области бедер/ягодиц.
Гипергликемия у детей
Углеводы играют большую роль в развитии и росте ребенка и являются обязательным и емким компонентом пищи. Они включаются почти во все виды обмена: нуклеиновых кислот, белков, липидов нуклеозидов. Углеводы необходимы для оптимальной жизнедеятельности, особенно для функции головного мозга. Учитывая высокую интенсивность метаболизма у детей, даже незначительные отклонения в обмене углеводов вызывают нарушение других видов обмена.
Причинами гипергликемии в детском возрасте являются:
- нейрогенные расстройства;
- различные эндокринопатии;
- патология печени;
- психогенные факторы;
- переедание.
В неонатальном периоде чаще встречается гипергликемия которая, обнаруживается у 20-80% недоношенных детей с весом меньше 1500 г. Это состояние — прогностически неблагоприятный признак в этом периоде, который может привести к смерти. Основная причина гипергликемии — избыточное вливание растворов глюкозы при интенсивной терапии. Также не исключается, как причина, инфекционный процесс. Гипергликемии часто встречаются у детей, которые перенесли асфиксию и имели дыхательные расстройства. Повышение уровня сахара может быть проявлением преходящего неонатального диабета (снижение функции поджелудочной железы).
Эндокринопатии связаны с повышенной активностью гипергликемизирующих гормонов: при избытке глюкагона активируется образование глюкозы из аминокислот и интенсивный распад гликогена, что сопровождается повышением сахара в крови. Избыток глюкокортикостероидов стимулирует образование глюкозы, а избыток катехоламинов стимулирует распад гликогена. При гипертиреозе усиливается гликогенолиз (расщепление гликогена), тормозится гликогенез (образование гликогена из глюкозы, стимулируется образование глюкозы и ее всасывание в кишечнике.
Повышенная секреция соматотропного гормона усиливает расщепление гликогена и тормозит расходование глюкозы. Нейро- и психогенные расстройства вызывают активацию симпатоадреналовой системы, надпочечников и выброс гормонов щитовидной железы. Гормоны этих систем активируют расщепление гликогена в печени и образование избытка глюкозы.
Переедание (длительное время потребление чрезмерного количества простых углеводов) рассматривается как причина гипергликемии. При этом глюкоза быстро всасывается в кишечнике, повышается ее уровень в крови, а печень не в состоянии преобразовать ее в гликоген в таком количестве. При нарушении функции печени всегда возникает преходящая гипергликемия после еды, что связано с неспособностью клеток печени быстро утилизировать глюкозу.
Гипергликемия проявляется у детей гипергликемическим синдромом и гипергликемической комой.
Гипергликемический синдром включает:
- Стойкое повышение уровня сахара до 10,5–11,5 ммоль/л.
- Выявление сахара в моче (глюкозурия, чего не должно быть в норме).
- Выраженная, неутолимая жажда (полидипсия).
- Полиурия — обильное мочеиспускание (выделение мочи более 3 л/день) вследствие увеличения клубочковой фильтрации, повышения осмоляльности мочи и уменьшения реабсорбции (обратного всасывания) воды в канальцах.
- Сухость кожи и признаки обезвоживания в следствие полиурии.
- Снижение артериального давления в результате потери жидкости и уменьшения сердечного выброса.
- Гипергликемическая (гиперосмолярная) кома у детей развивается при сахарном диабете при недостстке инсулина. Отмечается повышение сахара 22–28 ммоль/л и более. Гипергликемия вызывает повышение осмолярности плазмы. Нарастание осмолярности вызывает увеличение проницаемости гематоэнцефалического барьера, что вызывает неврологическую симптоматику. У новорожденных повышенная осмолярность не только угнетает ЦНС и вызывает отёк мозга, но и вызывает кровоизлияния внутрь желудочков мозга. У новорожденных с повышенным уровнем непрямого билирубина увеличивается его нейротоксичность.
Нарушение функции ЦНС полностью зависит от уровня повышения сахара:
- угнетение сознания;
- тонико-клонические судороги;
- обезвоживание;
- дыхательная недостаточность;
- апноэ;
- нарушения сердечно-сосудистой системы;
- развитие комы.
Что делать, если у вас гипергликемия (или вы подозреваете её)
Первым делом — обратиться к терапевту. Вам предложат сдать анализ крови на сахар, чтобы установить его уровень. Если гипергликемия подтвердится, врач начнёт разбираться с её причинами. И, как выше было сказано, с высокой вероятностью заподозрит диабет или состояние ему предшествующее.
В зависимости от поставленного диагноза вам могут назначить лекарственные препараты. Чаще всего инсулин или другие лекарства для снижения уровня глюкозы. Кроме того, вам понадобится регулярно измерять уровень сахара в крови, чтобы отслеживать своё состояние и не допускать затянувшихся приступов гипергликемии. Врач даст подробные инструкции, как это делать.
Но не лекарствами едиными. Вернуть сахар к норме можно, внеся простые изменения в образ жизни.
Пейте больше воды
Жидкость позволяет удалить избыток сахара из крови с помощью участившегося мочеиспускания.
Измените свои предпочтения в еде
Вам стоит уменьшить количество быстрых углеводов (особенно тортов, пирожных, магазинной выпечки, сладких напитков), а также снизить размеры порций и перейти на регулярное питание без перекусов. Возможно, на этом шаге понадобится помощь квалифицированного диетолога, который вместе с вами пропишет здоровый рацион.
Больше двигайтесь
Когда вы активничаете, органы и ткани потребляют больше глюкозы. А значит, уровень сахара в крови снижается. Но тут есть важный нюанс: в некоторых случаях при диабете физические нагрузки нежелательны.
Поэтому прежде чем записываться в спортзал или выходить на утреннюю пробежку, обязательно проконсультируйтесь с наблюдающим вас врачом. Он подскажет, как часто и много вам можно тренироваться, а также какие упражнения предпочтительны.
Не забывайте о приёме лекарств
Это важно. Случайно пропущенная инъекция инсулина приведёт к скачку глюкозы и ухудшит ваше состояние. Если же, наоборот, забыть, что вы уже использовали препарат, и употребить его повторно, есть риск заработать гипогликемию — состояние, которое может быть не менее опасным, чем его гипервариант.
Диета
Диета 9-й стол
- Эффективность: лечебный эффект через 14 дней
- Сроки: постоянно
- Стоимость продуктов: 1400 — 1500 рублей в неделю
Диета при инсулинорезистентности
- Эффективность: лечебный эффект через месяц
- Сроки: постоянно
- Стоимость продуктов: 1500-1600 руб. в неделю
Основные принципы питания пациентов с гипергликемией включают:
- Снижение общей калорийности до 1500 ккал в день.
- Исключение простых углеводов (сахар, сладости, выпечка, сладкие десерты, кондитерские изделия, мороженое, варенье, сгущенное молоко, сладкие напитки).
- Ограничение потребления жиров из-за их высокой калорийности.
- Увеличение количества белков, а также клетчатки до 30 г/сутки за счет овощей с низким гликемическим индексом.
Гликемический индекс отражает скорость расщепления углеводов до сахара и поступление в кровоток. Продукты с высоким индексом резко повышают уровень сахара в крови, а их преобладание в рационе будет сопровождаться постоянной гипергликемией. В рационе пациентов должны преобладать продукты, содержащие клетчатку, которая медленно переваривается не дает резких скачков повышения сахара в крови. Это могут быть зеленые овощи, листовой салат, все виды капусты, несладкие фрукты, бобовые, цельнозерновые продукты.
Исключаются или резко ограничиваются овощи, имеющие высокий индекс: картофель, морковь, свекла, томаты. Более подробные рекомендации можно найти в статьях Диета при повышенном сахаре крови, Диета 9-й стол и Диета при инсулинорезистентности.
Откуда берётся гипергликемия
Вот несколько причин Hyperglycemia in diabetes , которые могут вызвать гипергликемию. Спойлер: самая распространённая — в конце списка.
Вы слишком много едите
И особенно поднажимаете на углеводистую пищу. Органы и ткани берут из крови ровно столько глюкозы, сколько им необходимо. И если после того, как они получили свою дозу, в крови ещё остаётся много сахара, развивается она — гипергликемия.
У вас слишком пассивный образ жизни
Из‑за малой подвижности глюкоза в крови долго остаётся невостребованной.
Вы перенервничали и продолжаете это делать
Когда мозг считает, что вам угрожает опасность, он включает реакцию «Бей или беги». Для побега или схватки необходима энергия, поэтому организм резко повышает Blood sugar levels can fluctuate for many reasons уровень глюкозы в крови, чтобы наверняка обеспечить органы и ткани питанием.
Если вы действительно броситесь в бой или сбежите, этот сахар быстро израсходуется. А вот если вы нервничаете, но не двигаетесь, деваться глюкозе некуда, ведь клетки организма не голодны и не нуждаются в дополнительной энергии. Так, благодаря стрессу уровень сахара в крови надолго остаётся повышенным.
Ваш организм борется с внутренней инфекцией или перенёс травму
Это разновидность стресса, на которую организм реагирует так же, как на физическую угрозу.
У вас заболевание печени
Печень умеет накапливать глюкозу, чтобы в нужный момент по команде мозга выбросить её в кровь. Однако если печень повреждена, она может действовать и без команды, поддерживая постоянно высокий уровень сахара в крови.
У вас диабет
Это болезнь, при которой органы и ткани просто не могут принять глюкозу, и она остаётся в крови. Дело тут в инсулине: этот гормон является своеобразным ключиком, который «открывает» клетки тела и впускает в них глюкозу.
Иногда инсулина в организме катастрофически не хватает, а значит, клетки нечем «открыть» — в этом случае говорят о диабете 1 типа. Иногда он есть, но клетки к нему нечувствительны (инсулинорезистентны) — в этом суть диабета 2 типа.
Чаще всего гипергликемия — следствие одного из типов диабета.
Профилактика
- Здоровое питание.
- Снижение веса и постоянный контроль веса.
- Повышение физической активности.
- Выявление групп высокого риска (наличие абдоминального ожирения, наследственность по сахарному диабету, нарушение липидного обмена, повышенное давление, наличие жировой дистрофии печени, поликистоз яичников) и контроль в этой группе уровня сахара.
- Выявление больных с нарушенной толерантностью к глюкозе, гликемией натощак или HbA1C от 5,7-6,4%.
- Этим пациентам особенно важно соблюдать диету и повысить физическую активность.
- Периодический осмотр врачом (раз в полгода) и решение вопроса о приеме метформина при неэффективности немедикаментозного лечения.
Диагностика
Диагностику проводят в несколько этапов: определяются история заболевания, симптоматика (основной этап), проводятся лабораторные исследования. Внимание обращается на повышенную жажду и сухость в полости рта, необоснованное повышение аппетита, полиурию. При патологии случаются затруднения в дыхании и появляются мышечные боли, медленно заживают раны и порезы, кожные покровы быстро становятся сухими и часто отмечается зуд, человек очень быстро устает, возникает одышка. Еще одним симптомом считают затуманенное или ухудшенное зрение. Иногда есть риск развития инфекций, которые практически невозможно вылечить стандартными методами (отит или кандидоз). Суть анализов заключается в заборе утренней крови. Перед этим больной не должен есть (анализ проводиться не менее чем через 8 часов после еды). В некоторых случаях назначают повторные анализы, перерыв между которыми 5-7 дней, это делают для того, чтобы исключить или подтвердить возможные стрессовые факторы. Помимо этого, факторами могут выступать воспалительные процессы или прием определенных препаратов. В таком случае нужно сдать биохимические анализы.
Список источников
- Демидова Т.Ю., Галиева O.P. Профилактика и управление предиабетическими нарушениями углеводного обмена у больных с метаболическим синдромом. «Ожирение и метаболизм», №4 (13), 2007; С.19-С.24.
- Недогода С. В., Барыкина И. Н., Саласюк А. С., Смирнова В. О., Попова Е. А. Преддиабет: основные причины, симптомы, профилактика и лечение//Лекарственный вестник № 2 (70). 2021. Том 12.
- Актуальные вопросы эндокринологии в терапевтической практике: рук. для врачей / Под ред. М. Н. Калинкина, Л. В. Шпак. — Тверь: Фактор и К, 2014. — 698 с.
- Пасиешвили Т.М., Коряк В.В. Пациент с гипергликемией на приеме семейного врача / Восточноевропейский журнал внутренней и семейной медицины. — 2021.— № 2.— с. 35-39.
- П.Ф. Литвицкий, Л.Д. Мальцева Расстройства углеводного обмена у детей: гипогликемия, гипергликемия, гликогеноз, агликогеноз, гексоземия /Вопросы современной педиатрии. — 2021.- ТОМ 16/ № 5 с. 362-368.