АРТЕРИА́ЛЬНОЕ ДАВЛЕ́НИЕ
АРТЕРИА́ЛЬНОЕ ДАВЛЕ́НИЕ, давление крови в артериях. Уровень А. д. выражается в миллиметрах ртутного столба (мм рт. ст.) и зависит от нагнетающей силы сердца, периферич. сопротивления сосудов и объёма циркулирующей крови. Систолическое давление отражает макс. давление крови на стенки артерий при сокращении сердца, диастолическое – в момент его расслабления и зависит в осн. от периферич. сопротивления сосудов. У человека, напр., соотношение систолич. и диастолич. давления составляет в норме соответственно 120/80, у жирафа 340/230, у собаки 156/100, у акулы 32/16 мм рт. ст. Различают также пульсовое давление (разность между систолическим и диастолическим), зависящее от объёма крови, выбрасываемого при каждом сокращении сердца, и эластических свойств аорты, и среднее А. д. (равно сумме диастолического и 1/3 пульсового давления), пропорциональное объёму крови, выбрасываемому сердцем за 1 мин, и общему периферич. сопротивлению системы кровеносных сосудов. У большинства млекопитающих (в т. ч. у человека) оно составляет 100 мм рт. ст. Значения А. д. снижаются по мере удаления сосуда от сердца. Напр., у здорового взрослого человека систолич. давление в аорте равно 110–130 мм рт. ст., в артериолах – 20–50 мм рт. ст. В течение суток оно колеблется в зависимости от функциональной активности и существенно понижается ночью во время сна (70–80 мм рт. ст.). В сосудах, расположенных выше уровня сердца, давление уменьшается пропорционально величине гидростатического столба. Жираф, напр., нуждается в высоком А. д., чтобы кровь могла достичь головы. Макс. значения А. д. у кольчатых червей и членистоногих составляют 5–10 мм рт. ст., у активных рыб (напр., лосось, угорь) – 65–75, у зелёной лягушки – ок. 40, у птиц – 140–180 мм рт. ст. У самцов теплокровных животных А. д. выше, чем у самок, а холоднокровные животные имеют более низкое А. д., чем теплокровные.
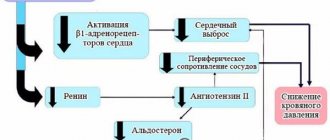
У позвоночных сохранение относит. постоянства уровня А. д. обеспечивается системой регуляции, благодаря чему достигается определённое соотношение между работой сердца, просветом сосудов, ёмкостью сосудистого русла и количеством циркулирующей крови. Действие физиологич. механизмов регуляции может быть кратковременным и длительным. К первым относятся ренин-ангиотензин-альдостероновая система и сердечно-сосудистые рефлексы. Эти рефлексы, опосредуемые через центр. нервную систему (т. н. барорефлекс, хеморефлекс, цереброишемическая реакция), поддерживают нормальный уровень А. д. от неск. минут до неск. часов.
Барорецепторы, расположенные в стенке дуги аорты и в области разветвления общей сонной артерии (каротидный синус), реагируют на степень растяжения сосудистой стенки при повышении А. д. Частота импульсов, идущих от барорецепторов в сердечно-сосудистый центр в продолговатом мозге, увеличивается, что приводит к рефлекторному снижению сердечного выброса и сопротивления периферич. сосудов и, как следствие, снижению А. д. Чем выше давление в дуге аорты и каротидном синусе, тем сильнее нервные влияния, ведущие к снижению А. д. При падении А. д. частота импульсов, идущих от барорецепторов, уменьшается, рефлекторно повышается сердечный выброс и сопротивление мелких артерий и артериол и, следовательно, давление. Барорефлекс выполняет роль буфера, сглаживая быстрые колебания А. д., напр. при резком переходе из горизонтального положения в вертикальное не ощущается явлений, связанных с нарушением кровоснабжения головного мозга.
Хеморефлекс запускается как с периферич. рецепторов, расположенных в аортальной и каротидной рефлексогенных зонах, так и с центр. хеморецепторов, локализованных в продолговатом мозге. Первые активируются преим. при дефиците кислорода в крови, вторые реагируют на избыток в ней углекислого газа. Активация хеморецепторов приводит к рефлекторной активации симпатоадреналовой системы. В итоге из симпатич. нервных окончаний выбрасывается норадреналин, который действует на т. н. альфа-1 адренорецепторы гладких мышц кровеносных сосудов и вызывает их сужение; через бета-1 адренорецепторы опосредуется увеличение сердечного выброса. Выделяемый надпочечниками адреналин через активацию бета-2 адренорецепторов расширяет бронхи, активирует гликогенолиз, что приводит к увеличению содержания глюкозы в крови.
Цереброишемическая реакция возникает при существенном уменьшении кровоснабжения нейронов сердечно-сосудистого центра. При значит. кровопотере среднее А. д. может снизиться до 60–70 мм рт. ст., что приводит к дефициту кровоснабжения сердечно-сосудистого центра и прямому возбуждению симпатоадреналовой системы и частичной нормализации А. д. При кровопотерях, сопровождающихся снижением А. д. до 40–30 мм рт. ст., геморрагический шок, как правило, становится необратимым.
При активации ренин-ангиотензинной системы повышение А. д. обусловлено образованием ангиотензина-II (образуется при участии ренина), который вызывает сужение сосудов, и увеличением секреции альдостерона, что приводит к увеличению объёма циркулирующей крови.
Длительная регуляция А. д. осуществляется при участии почек, которые обеспечивают баланс между потреблением и выделением ионов натрия и воды; даже небольшое повышение А. д. сопровождается существенным повышением выделения жидкости почками. Именно хорошо функционирующие почки на протяжении всей жизни человека поддерживают среднее А. д. в диапазоне нормальных значений.
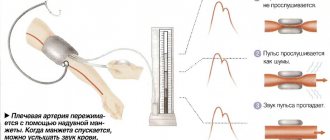
Наиболее точно А. д. измеряется прямым способом с помощью введённых в кровеносные сосуды катетеров, соединённых с датчиками давления. Менее точный метод измерения, предложенный рос. хирургом Н. С. Коротковым в нач. 20 в., регистрирует величину А. д. с помощью тонометра – манометра, соединённого с резиновой манжетой, укрепляемой у человека вокруг руки, у животных – вокруг конечности или хвоста (у крыс). Нагнетаемый в манжету воздух сжимает артерию и момент, когда сосуд перестаёт пропускать кровь, определяется с помощью фонендоскопа по прекращению пульсовых звуковых колебаний. Медленно выпуская воздух из манжеты, фиксируют момент появления звука, вызванного сокращением сердца, и по манометру устанавливают значение систолич. давления. Показания манометра в момент исчезновения пульса соответствуют значению диастолич. давления.
У человека повышенным считается А. д., при котором значения систолич. и диастолич. давления превосходят соответственно 140 и 90 мм рт. ст. Долгосрочное увеличение А. д. человека – артериальная гипертензия, снижение – артериальная гипотензия.
Центральное аортальное давление и жесткость сосудов: актуальность в современной кардиологии
Рост сердечно-сосудистых заболеваний, наблюдающийся во всех развитых странах мира, требует пристального внимания к вопросам профилактики и эффективного лечения заболеваний сердца и сосудов.
Данные исследований свидетельствуют, что артериальной гипертензией страдают около 65 млн американцев в возрасте 18–39 лет и 1 млрд людей во всем мире. Артериальная гипертензия (АГ) является фактором риска развития и прогрессирования атеросклероза, ишемической болезни сердца, хронической сердечной недостаточности и острых нарушений мозгового кровообращения. Изменения сосудов эластического типа (аорта, легочная артерия и отходящие от них крупные артерии) являются важным звеном патогенеза при АГ. В норме эластические свойства указанных сосудов, особенно аорты, способствуют сглаживанию периодических волн крови, производимых левым желудочком в период систолы и их преобразованию в непрерывный периферический кровоток. Эластические свойства аорты модулируют функцию левого желудочка, уменьшая посленагрузку на него и его конечный систолический и диастолический объемы. Это ведет к уменьшению напряжения стенок левого желудочка, в результате чего улучшается трофика наиболее чувствительных к гипоксии субэндокардиальных слоев миокарда и улучшается коронарный кровоток. Одной из значимых характеристик сосудов эластического типа является жесткость, которая определяет способность артериальной стенки к сопротивлению деформации. Жесткость сосудистой стенки зависит от возраста, выраженности атеросклеротических изменений, скорости и степени возрастной инволюции важнейших структурных белков эластина и фибулина, возрастного повышения жесткости коллагена, генетически обусловленных особенностей эластиновых волокон и от уровня артериального давления (АД). В ряде исследований подчеркивается роль воспаления в патогенезе жесткости крупных артерий. Классическим маркером артериальной жесткости/эластичности крупных сосудов является скорость пульсовой волны (СПВ). Величина этого показателя в значительной степени зависит от отношения толщины стенки сосудов к радиусу просвета сосуда и эластичности стенки сосуда. Чем растяжимее сосуд, тем медленнее распространяется и быстрее ослабевает пульсовая волна и наоборот – чем ригиднее и толще сосуд и меньше его радиус, тем выше СПВ. В норме СПВ в аорте равна 4–6 м/с, в менее эластичных артериях мышечного типа, в частности лучевой, – 8–12 м/с. «Золотым стандартом» оценки ригидности аорты считается СПВ между сонной и бедренной артерией.
Центральное (аортальное) и периферическое артериальное давление
В нормальной артериальной системе после сокращения желудочка в систолу пульсовая волна направляется из места возникновения (аорта) в крупные средние, а затем мелкие сосуды с определенной скоростью. По пути прохождения пульсовая волна встречается с разными препятствиями (например, бифуркации, резистивные сосуды, стенозы), приводящими к появлению отраженных пульсовых волн, направляющихся к аорте. При достаточной эластичности крупных сосудов, прежде всего аорты, отраженная волна абсорбируется. Сумма прямой и отраженных пульсовых волн отличается на разных сосудах, в результате АД, в первую очередь – систолическое АД (САД), отличается в различных магистральных сосудах и не совпадает с измеренным на плече. Степень увеличения САД в периферических артериях относительно САД в аорте сильно варьирует у разных субъектов и определяется модулем эластичности изучаемых артерий и удаленностью места измерения. В силу этого манжеточное давление в плечевой артерии далеко не всегда соответствует давлению в нисходящей аорте. Определенный вклад в повышение АД в плечевой артерии относительно АД в аорте вносит повышение жесткости ее стенки, значит – необходимость создания большей компрессии в манжете. В отличие от периферического АД, уровень центрального АД модулируется эластическими характеристиками крупных артерий, а также структурно-функциональным состоянием артерий среднего калибра и микроциркуляторного русла и, таким образом, является показателем, косвенно отражающим состояние всего сердечно-сосудистого русла. Наибольшее прогностическое значение имеет АД в восходящей и центральной частях аорты, или центральное АД. В случае увеличения жесткости (снижении эластичности) аорты отраженная волна не абсорбируется в достаточной мере и, как правило, в связи с более высокой СПВ возвращается в период систолы, что приводит к увеличению центрального САД. Последствием усилившейся ригидности и повышения центрального АД является изменение посленагрузки на левый желудочек и нарушение коронарной перфузии, что приводит к гипертрофии левого желудочка, повышению потребности миокарда в кислороде.
В последние годы появились специальные методики (например, аппланационная тонометрия лучевой или сонной артерий), позволяющие зафиксировать такие детерминанты пульсового давления, как пульсовая (колебания артериальной стенки от сердца к резистивным сосудам) и отраженная (колебания артериальной стенки от резистивных сосудов к сердцу) волны, и с помощью компьютерной обработки при регистрации колебаний лучевой артерии рассчитать значения центрального давления в аорте (рис. 1). В течение 10 секунд выполняется регистрация кривой давления в лучевой артерии верхней конечности с помощью аппланационного тонометра. Данные обрабатываются с помощью программного обеспечения: вычисляется усредненная форма кривой, которая принятым математическим способом трансформируется в график центральное давление в аорте (ЦДА). Компьютерная обработка полученных кривых центрального давления позволяет определить параметры ЦДА: время до первого (Т1) и второго (Т2) систолических пиков волны. Давление на первом пике/изломе (Р1) принимается за давление выброса, дальнейший прирост до второго пика (ΔР) означает отраженное давление, их сумма (максимальное давление во время систолы) – систолическое ЦДА (ЦДАс) Помимо величины центрального АД существует показатель прироста давления, индекс аугментации (усиления, AIx) выражающийся в процентах, который определяется как разница давлений между первым, ранним пиком (вызванным сердечной систолой) и вторым, поздним (появляющимся в результате отражения первой пульсовой волны) систолическим пиком, деленная на центральное пульсовое давление. Таким образом, центральное аортальное давление является расчетным параметром гемодинамики, зависящим не только от сердечного выброса, периферического сосудистого сопротивления, но и от структурно-функциональных характеристик магистральных артерий (их эластических свойств). Различия между уровнем центрального и периферического САД наиболее отчетливо выражены в молодом возрасте и снижаются у пожилых людей. Показано, что центральное АД, особенно центральное пульсовое давление, и индекс аугментации коррелируют со степенью ремоделирования крупных артерий и СПВ как классического показателя жесткости сосудистой стенки.
Артериальная жесткость как фактор кардиоваскулярного риска
Изменение механических свойств крупных артерий имеет четкую патофизиологическую связь с клиническими исходами. Результаты исследований свидетельствуют о том, что СПВ – показатель артериальной жесткости – может быть лучшим предиктором последующих сердечно-сосудистых событий по сравнению с известными факторами риска, такими как возраст, уровень АД, гиперхолестеринемия и сахарный диабет. Исследования с оценкой СПВ позволили установить, что увеличение артериальной жесткости является предиктором кардиоваскулярного риска у практически здоровых лиц, пациентов с сахарным диабетом, конечной стадией почечной недостаточности и пожилых людей. Продемонстрировано, что артериальная жесткость является предиктором смертности у больных АГ. Так, в популяционном исследовании Copenhagen County population продемонстрировано, что увеличение СПВ (>12 м/с) ассоциируется с 50% увеличением риска сердечно-сосудистых событий. Кроме того, прогностическое значение СПВ выявлено в японском исследовании с периодом наблюдения в среднем 8,2 года. Установлено, что косвенные индексы аортальной жесткости и отраженной волны, такие как центральное аортальное давление и индекс аугментации, являются независимыми предикторами сердечно-сосудистых событий и смертности. Так, в исследовании, включавшем 1272 нормотензивных и нелеченных пациента с АГ, продемонстрировано, что центральное САД было независимым предиктором сердечно-сосудистой смертности после поправки на различные факторы сердечно-сосудистого риска, включая массу миокарда левого желудочка и определение толщины комплекса «интима-медиа» при ультразвуковом исследовании сонных артерий. Более того, больные с высоким аортальным давлением имеют худший кардиоваскулярный прогноз, чем больные с более эффективным контролем центрального аортального давления.
Увеличение жесткости аорты также является независимым предиктором диастолической дисфункции у пациентов с АГ (рис. 2), а также может ограничивать толерантность к физической нагрузке при дилатационной кардиомиопатии. У пациентов с сердечной недостаточностью с сохраненной фракцией выброса левого желудочка систолическая дисфункция и артериальная жесткость появляются с возрастом и/или с прогрессией АГ. Повышенная артериальная жесткость связана с дисфункцией эндотелия и снижением биодоступности оксида азота (NO). Эндотелиальная дисфункция у пациентов с высоким кардиоваскулярным риском может объяснить, почему эти состояния ассоциируются с повышенной артериальной жесткостью на ранних стадиях до манифестации атеромы. Следовательно, препараты, такие как небиволол, увеличивающие образование NO, позволяют уменьшить жесткость крупных артерий, что, в свою очередь, может вести к снижению сердечно-сосудистого риска. Таким образом, значение артериальной ригидности, оцененной по СПВ, для риска сердечно-сосудистых исходов продемонстрировано в ряде проспективных исследований как у больных АГ, так и в общей популяции. Начиная с 2007 года, оценка СПВ на каротидно-феморальном сегменте рекомендуется в качестве дополнительного метода исследования по выявлению поражения органов-мишеней при АГ.
Авторы
А.Н. Беловол, доктор медицинских наук, профессор, член-корреспондент НАМН Украины;
И.И. Ккнязькова, доктор медицинских наук, доцент
Харьковский национальный медицинский университет
Статья предоставлена WEB-сайтом «Страна Врачей»